Clear Sky Science · pl
KDM5B współdziała z kompleksem CRL4B, aby sprzyjać nowotworzeniu raka piersi z receptorem estrogenowym (ER+) poprzez regulację metabolizmu cholesterolu
Dlaczego to badanie ma znaczenie dla zdrowia codziennego
Rak piersi jest najczęstszym nowotworem u kobiet, a wiele guzów rośnie w odpowiedzi na hormon estrogen. Te nowotwory nie tylko szybko dzielą się — przebudowują także sposób wykorzystania tłuszczów, takich jak cholesterol. Badanie ujawnia, w jaki sposób białko regulujące geny, KDM5B, współpracuje z innym kompleksem białkowym, CRL4B, aby zwiększyć poziom cholesterolu w komórkach raka piersi z dodatnim receptorem estrogenowym (ER+). Zrozumienie tego ukrytego partnerstwa może pomóc naukowcom w znalezieniu nowych sposobów spowolnienia wzrostu guza i udoskonalenia istniejących terapii, takich jak leczenie hormonalne czy leki obniżające poziom cholesterolu.
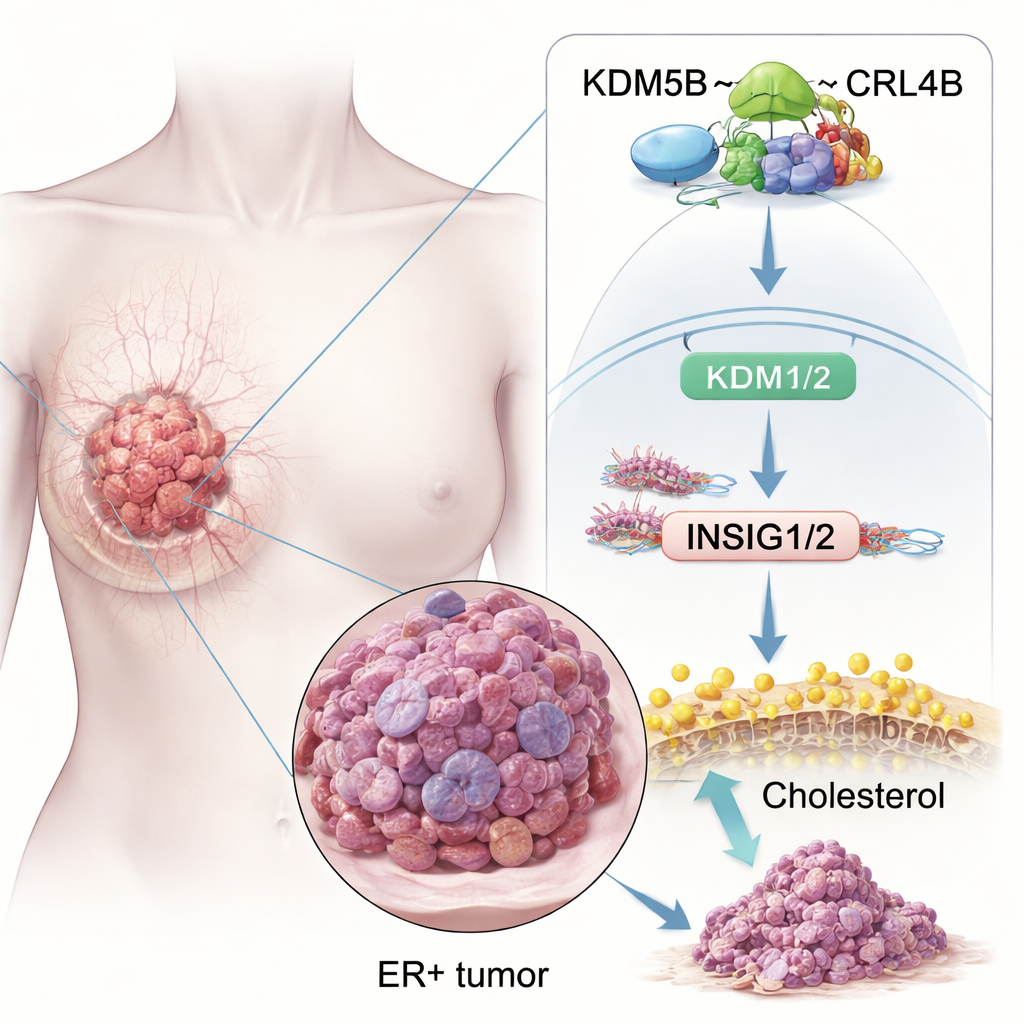
Białko, które przechyla równowagę na korzyść nowotworu
Naukowcy najpierw sprawdzili, czy KDM5B jest po prostu obecny w rakach ER+ czy rzeczywiście je napędza. Analiza dużych baz danych nowotworowych i próbek tkankowych wykazała, że poziomy KDM5B są wyższe w guzach piersi niż w prawidłowej tkance piersi, a szczególnie podwyższone w nowotworach ER+. Pacjentki, których nowotwory produkują więcej KDM5B, mają zwykle gorsze przeżycie, nawet przy stosowaniu standardowej chemioterapii lub terapii hormonalnej. W eksperymentach na hodowlach komórkowych zwiększenie ekspresji KDM5B powodowało szybszy wzrost komórek raka piersi ER+, łatwiejszą inwazję tkanek otaczających oraz powstawanie większej liczby klasterów o cechach komórek macierzystych, które uważa się za źródła nowych guzów. Zredukowanie KDM5B przynosiło odwrotny efekt — zmniejszało tworzenie kolonii in vitro i hamowało wzrost guzów u myszy.
Silne partnerstwo wewnątrz komórek nowotworowych
Aby zrozumieć mechanizm działania KDM5B, zespół poszukiwał jego białkowych partnerów. Odkryli, że KDM5B fizycznie wiąże się z elementami maszyny molekularnej zwanej kompleksem CRL4B — układem enzymatycznym, który znakuję białka i wpływa na pakowanie DNA. Szczegółowe testy biochemiczne wykazały, że KDM5B bezpośrednio oddziałuje z dwoma komponentami CRL4B, CUL4B i DDB1, poprzez specyficzne regiony każdego z tych białek. W komórkach raka piersi ER+ kompleks KDM5B–CRL4B działa na wiele genów przy ich przełącznikach włącz/wyłącz. Mapowanie genomowe wykazało, że KDM5B i CUL4B często występują razem na promotorach genów, gdzie modyfikują chemiczne znaczniki na histonach — bębenkach wokół których owinięte jest DNA — prowadząc do ich represji.
Zdejmowanie hamulców z metabolizmu cholesterolu
Wśród wielu dotkniętych szlaków wyróżnił się metabolizm cholesterolu. Komórki nowotworowe potrzebują dodatkowego cholesterolu do budowy błon i przetrwania stresu, a guzy ER+ wykorzystują też pochodne cholesterolu do naśladowania działania estrogenu. Badanie pokazuje, że kompleks KDM5B–CRL4B wiąże się bezpośrednio z regionami kontrolnymi dwóch kluczowych genów „hamujących”, INSIG1 i INSIG2. Geny te normalnie pomagają utrzymać w ryzach główny regulator cholesterolu, SREBP2. KDM5B–CRL4B dodaje represyjny znacznik (H2AK119ub1) i usuwa aktywujący znacznik (H3K4me3) z histonów na promotorach INSIG1/2, osłabiając ich ekspresję. Przy niższych poziomach białek INSIG1/2, SREBP2 zostaje uwolniony i włącza geny syntezy cholesterolu, co zwiększa stężenie cholesterolu w komórkach raka piersi ER+ i potęguje ich inwazyjne zachowanie. Gdy badacze zaburzyli funkcję KDM5B lub CRL4B, poziomy INSIG1/2 wzrosły, aktywność SREBP2 spadła, a całkowita zawartość cholesterolu w komórkach zmalała.
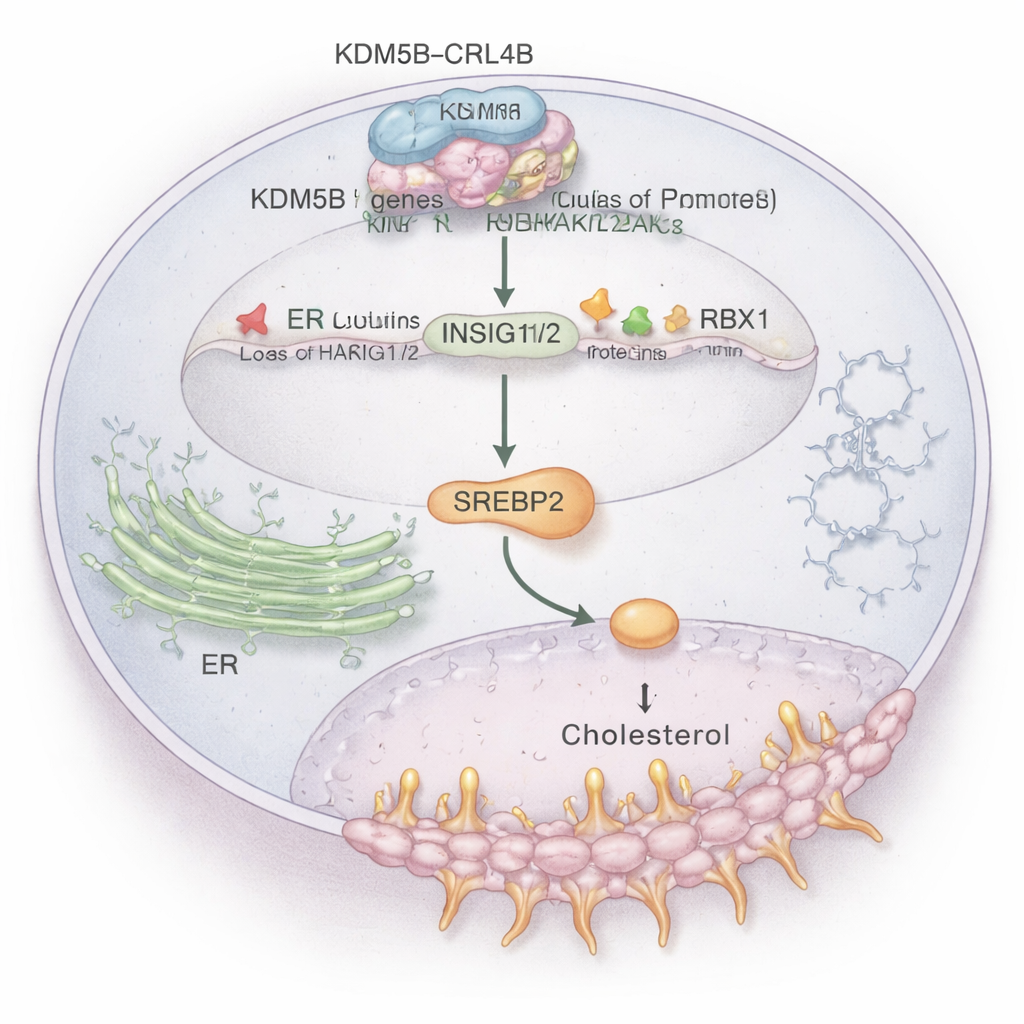
Krzyżowanie sygnałów cholesterolu i sygnałów nowotworowych
Praca łączy także ten szlak z sygnałem pochodzącym z cholesterolu, 27‑hydroksycholesterolem (27‑HC) — molekułą już znaną ze wspierania raka piersi ER+. Leczenie komórek ER+ 27‑HC zwiększało poziom KDM5B i dodatkowo tłumiło INSIG1/2, popychając komórki w stronę większego wzrostu i inwazji. Co istotne, blokowanie KDM5B lub CRL4B osłabiało te agresywne efekty, sugerując, że 27‑HC działa częściowo poprzez osie KDM5B–CRL4B. Naukowcy wykazali również, że symwastatyna, powszechnie stosowany statyna obniżająca poziom cholesterolu, spowalniała wzrost komórek raka piersi, a w połączeniu z inhibitorem KDM5B efekt przeciwnowotworowy był silniejszy. Wskazuje to, że łączenie leków hamujących syntezę cholesterolu z lekami celującymi aktywność genową KDM5B może być obiecującą strategią terapeutyczną.
Co to oznacza dla pacjentów i przyszłych terapii
Badanie ujawnia nowy łańcuch zdarzeń w komórkach raka piersi ER+: sygnał związany z cholesterolem (27‑HC) zwiększa KDM5B; KDM5B łączy siły z kompleksem CRL4B, aby wyciszyć INSIG1 i INSIG2; to uwalnia SREBP2, nasilając produkcję cholesterolu i wspierając wzrost, inwazję oraz utrzymanie komórek o cechach macierzystych. Ponieważ KDM5B jest podwyższone i związane z gorszym rokowaniem także w kilku innych nowotworach, zahamowanie tego białka — lub przywrócenie działania hamulców INSIG1/2 — może otworzyć nowe możliwości kontroli wzrostu guza. Choć potrzebne są dalsze badania, zanim wyniki te znajdą zastosowanie w codziennej praktyce, odkrycia podkreślają, jak blisko powiązane jest zachowanie nowotworów z powszechnymi cząsteczkami, takimi jak cholesterol, oraz że istniejące leki, np. statyny, mogą pewnego dnia być łączone z terapiami epigenetycznymi w celu poprawy wyników leczenia.
Cytowanie: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
Słowa kluczowe: Rak piersi z dodatnim receptorem estrogenowym, metabolizm cholesterolu, KDM5B, INSIG1/INSIG2, terapia epigenetyczna