Clear Sky Science · pl
Mutantny TDP-43 powoduje zaburzenia transportu aksonalnego i glikolizy w modelu motoneuronu mysiego pochodzącego z komórek macierzystych schorzenia stwardnienia zanikowego bocznego (ALS)
Dlaczego te badania mają znaczenie dla osób z ALS
Stwardnienie zanikowe boczne (ALS) to śmiertelna choroba, która stopniowo prowadzi do paraliżu przez niszczenie komórek nerwowych kontrolujących mięśnie. U większości pacjentów obserwuje się uszkodzenia związane z białkiem zwanym TDP-43, ale naukowcy wciąż nie znają w pełni mechanizmów, dzięki którym te uszkodzenia ranią neurony ruchowe. W tym badaniu wykorzystano precyzyjnie zmodyfikowany myszy model z komórek macierzystych, aby zidentyfikować niektóre z najwcześniejszych problemów wywołanych przez chorobowo powiązaną wersję TDP-43, dostarczając wskazówek, które mogą pomóc w kształtowaniu przyszłych terapii.
Tworzenie neuronów ruchowych w hodowli
Aby badać ALS w kontrolowanych warunkach, badacze zaczęli od mysich embrionalnych komórek macierzystych i nakłonili je do różnicowania w neurony ruchowe — długie, przypominające kable komórki przekazujące sygnały z rdzenia kręgowego do mięśni. Wprowadzili do tych komórek pojedynczą dodatkową kopię ludzkiego genu TDP-43, w wersji normalnej lub niosącej specyficzną mutację związaną z ALS nazwaną M337V. Fluorescencyjny znacznik pozwolił zespołowi śledzić ludzki białkowy produkt wewnątrz komórek. Do 20. dnia hodowli zarówno komórki z normalnym, jak i zmutowanym białkiem dojrzały do neuronów ruchowych, wykazując typowe markery, tworząc rozgałęzione sieci i synapsopodobne połączenia, co wiernie odtwarzało neurony występujące w układzie nerwowym. 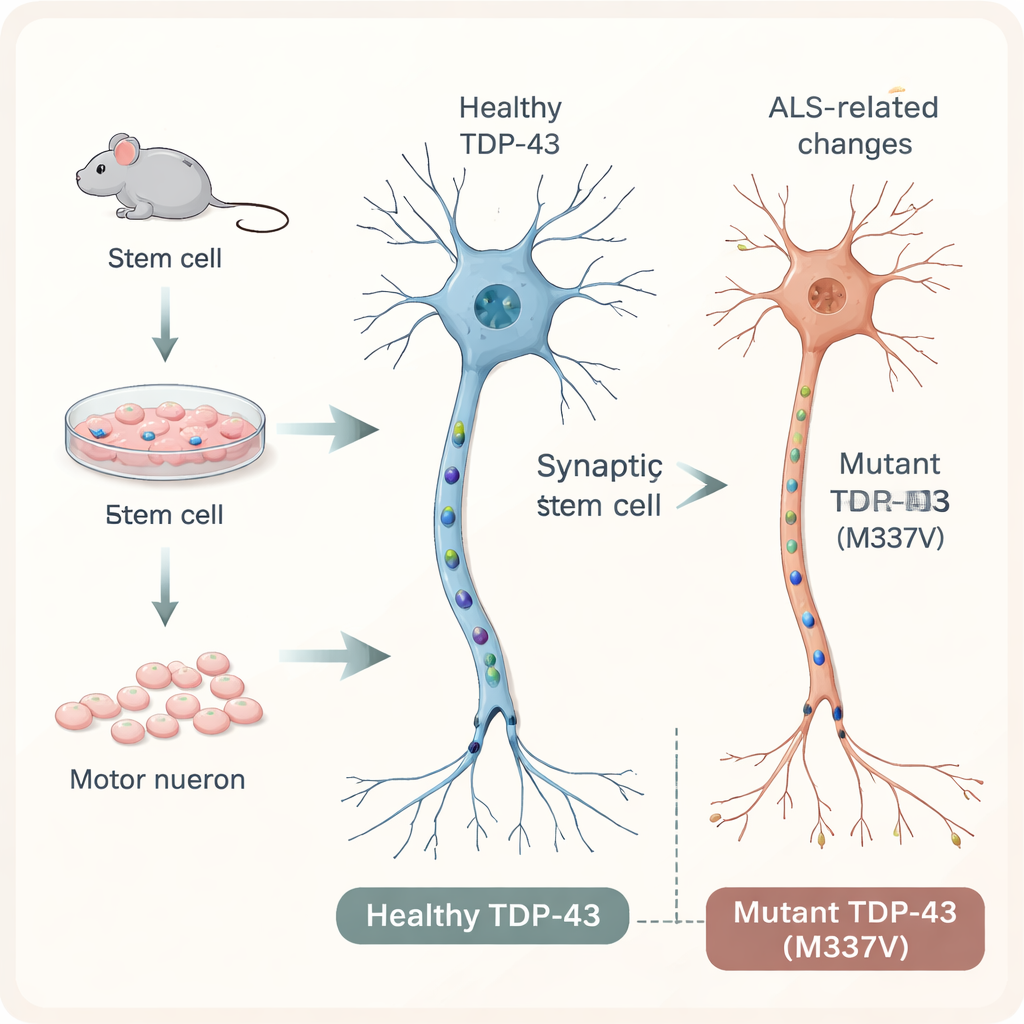
Ukryte uszkodzenia bez widocznych grudek białkowych
U osób z ALS TDP-43 często przemieszcza się z typowej lokalizacji w jądrze do cytoplazmy i tworzy agregaty — klasyczny obraz patologiczny widoczny w mikroskopie. Zaskakująco, w tym modelu z komórek macierzystych zmutowany TDP-43 nie wykazywał zwiększonej nieprawidłowej lokalizacji ani agregacji w porównaniu z wersją normalną. Większość białka pozostawała na swoim miejscu. Mimo to neurony były wyraźnie mniej zdrowe: hodowle z zmutowanym białkiem miały mniej ciał komórkowych, mniejsze sieci włókien nerwowych i obniżoną ogólną przeżywalność. Sugeruje to, że poważne uszkodzenia neuronów ruchowych mogą zachodzić wcześniej, lub nawet bez widocznych, dramatycznych grudek białkowych obserwowanych w mózgach i rdzeniach pacjentów.
Korki na „autostradach” nerwowych
Neurony ruchowe polegają na szybkich, efektywnych systemach transportu, które przesuwają niezbędne ładunki wzdłuż ich długich aksonów. Korzystając z urządzeń mikrofuidycznych izolujących aksony w wąskich kanałach, zespół śledził ruch pęcherzyków sygnalizacyjnych (endosomów) i mitochondriów produkujących energię w żywych komórkach. W neuronach z zmutowanym TDP-43 ładunki wciąż poruszały się w większości w prawidłowych kierunkach, jednak poruszały się wolniej. Endosomy sygnałowe wykazywały obniżone prędkości podczas transportu w kierunku ciała komórkowego, a mitochondria poruszały się wolniej w obu kierunkach, spędzając więcej czasu w stanie zatrzymania. Co ważne, podstawowy sprzęt napędzający ten ruch — białka motoryczne poruszające się po wewnętrznych torach — nie wydawał się zmieniony pod względem ilości, co sugeruje, że problem leży w funkcjonowaniu tego mechanizmu, a nie w jego obfitości.
Braki energetyczne w spalaniu cukru, ale nie w mitochondriach
Ponieważ transport aksonalny wymaga dużo energii, badacze sprawdzili, jak te neurony wytwarzają i wykorzystują energię. Mierzyli dwa główne źródła: oddychanie mitochondrialne, które spala paliwo przy użyciu tlenu, oraz glikolizę, która rozkłada cukier w otaczającym płynie. Mitochondria wyglądały normalnie pod względem liczby, kształtu i potencjału błonowego, a ich ogólna zdolność do wytwarzania energii wydawała się niezmieniona w komórkach z mutacją. W przeciwieństwie do tego neurony z zmutowanym TDP-43 wykazywały wyraźny spadek podstawowej glikolizy. Wcześniejsze prace wykazały, że lokalna glikoliza wzdłuż aksonów może dostarczać „paliwo na pokładzie” niezbędne do szybkiego transportu pęcherzyków. Obniżona zdolność do spalania cukru zaobserwowana tutaj może zatem przyczyniać się do spowolnienia ruchu ładunków, dodając kolejną warstwę obciążenia dla już wrażliwych neuronów ruchowych.
Co to oznacza dla przyszłych terapii ALS
Podsumowując, badanie pokazuje, że nawet niskie poziomy mutacyjnego TDP-43 związanego z ALS wystarczają, by uczynić neurony ruchowe bardziej podatnymi na uszkodzenie, spowolnić transport niezbędnych ładunków wzdłuż ich aksonów i osłabić ich zdolność do pozyskiwania energii z cukru — i to wszystko bez oczywistych grudek białkowych, na które zwykle zwracają uwagę patolodzy. Dla osób niebędących specjalistami kluczowe przesłanie jest takie, że wczesne, subtelne zmiany w „ruchu drogowym” komórek i gospodarce energetycznej mogą przygotowywać grunt pod późniejsze, bardziej dramatyczne uszkodzenia w ALS. Wskazuje to na transport aksonalny i szlaki energetyczne komórek, zwłaszcza glikolizę, jako obiecujące cele terapeutyczne mające chronić neurony ruchowe zanim nastąpi nieodwracalna degeneracja. 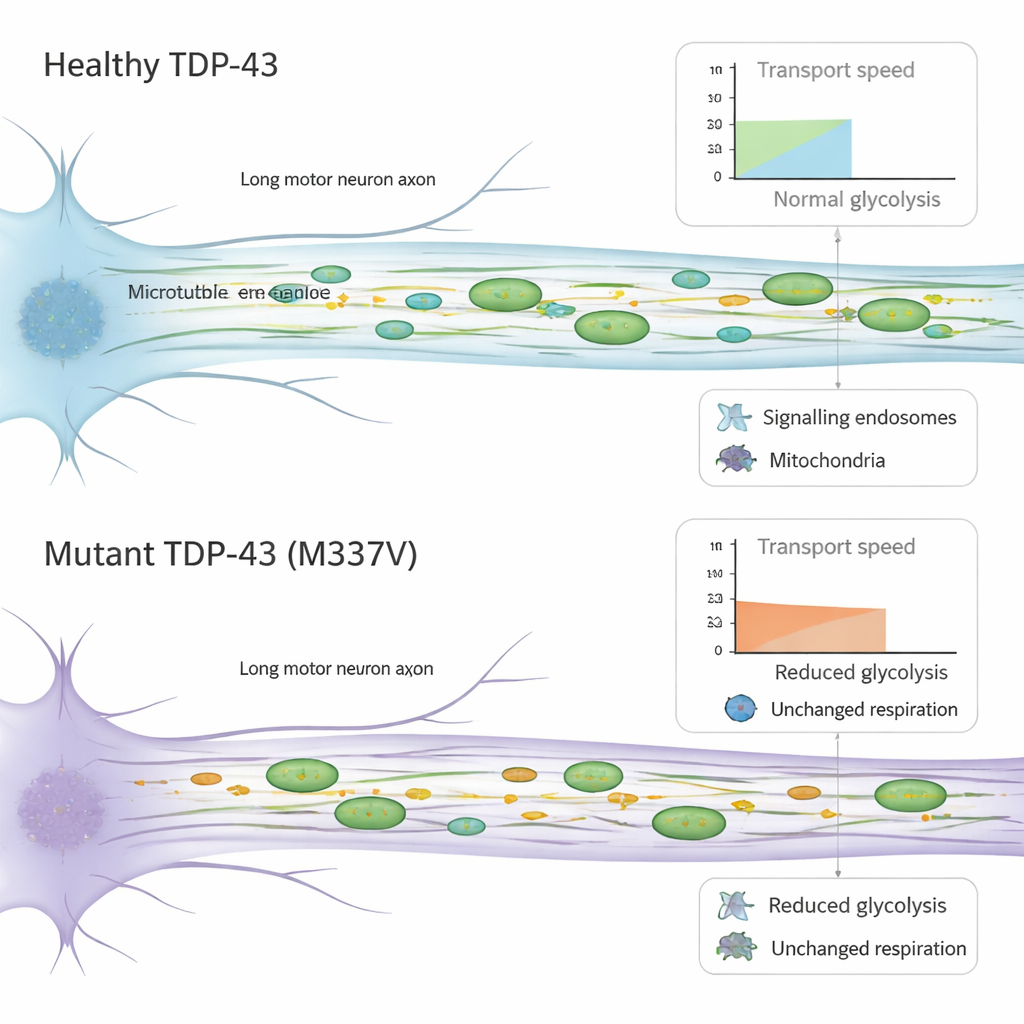
Cytowanie: Carroll, E., Scaber, J., Pasniceanu, IS. et al. Mutant TDP-43 drives impairments in axonal transport and glycolysis in a mouse stem-cell-derived motor neuron model of amyotrophic lateral sclerosis (ALS). Cell Death Dis 17, 193 (2026). https://doi.org/10.1038/s41419-026-08437-2
Słowa kluczowe: stwardnienie zanikowe boczne, TDP-43, neurony ruchowe, transport aksonalny, energia komórkowa