Clear Sky Science · pl
Sygnalizacja TGFβ sprzyja postępowi cyklu komórkowego i oporności na inhibitor CDK4/6 palbocyklib poprzez modulację transkrypcyjną SOX4 w komórkach raka piersi
Kiedy komórki nowotworowe przejmują przyjazny sygnał
Nasz organizm polega na niezliczonych sygnałach chemicznych, które utrzymują podziały komórek wtedy, gdy są potrzebne, i zatrzymują je, gdy powinny. Jeden z tych sygnałów, zwany czynnikiem transformującym beta (TGFβ), zwykle pomaga zapobiegać nowotworom. W tym badaniu pokazano, jak w niektórych nowotworach piersi ten sam sygnał TGFβ może zostać przechwycony i wykorzystany do wspierania wzrostu komórek nowotworowych oraz do oporności na ważny lek – palbocyklib. Zrozumienie tego przełączenia może wskazać lepsze kombinacje terapeutyczne dla pacjentów, których guzy przestały reagować na leczenie.
Od hamulca wzrostu do sygnału o dwojakim działaniu
W zdrowej tkance TGFβ zwykle pełni funkcję hamulca: spowalnia podziały komórek i ogranicza stan zapalny, co pomaga zapobiegać wczesnemu tworzeniu się nowotworów. Jednak w ustalonych nowotworach, szczególnie w guzach piersi, które już zgromadziły mutacje napędzające raka, TGFβ może działać przeciwnie — sprzyjając migracji, inwazji i przerzutom komórek. Aby zbadać to dwoiste zachowanie, badacze użyli trójwymiarowych „mini-guzów” hodowanych z ludzkich komórek piersi. Porównali komórki o cechach zbliżonych do normalnych z komórkami identycznymi, ale niosącymi onkogenną mutację HRAS, która popycha je w stronę nowotworu. To kontrolowane ustawienie pozwoliło im sprawdzić, jak ten sam sygnał TGFβ przebiega w środowisku przednowotworowym w porównaniu z przypominającym nowotwór.
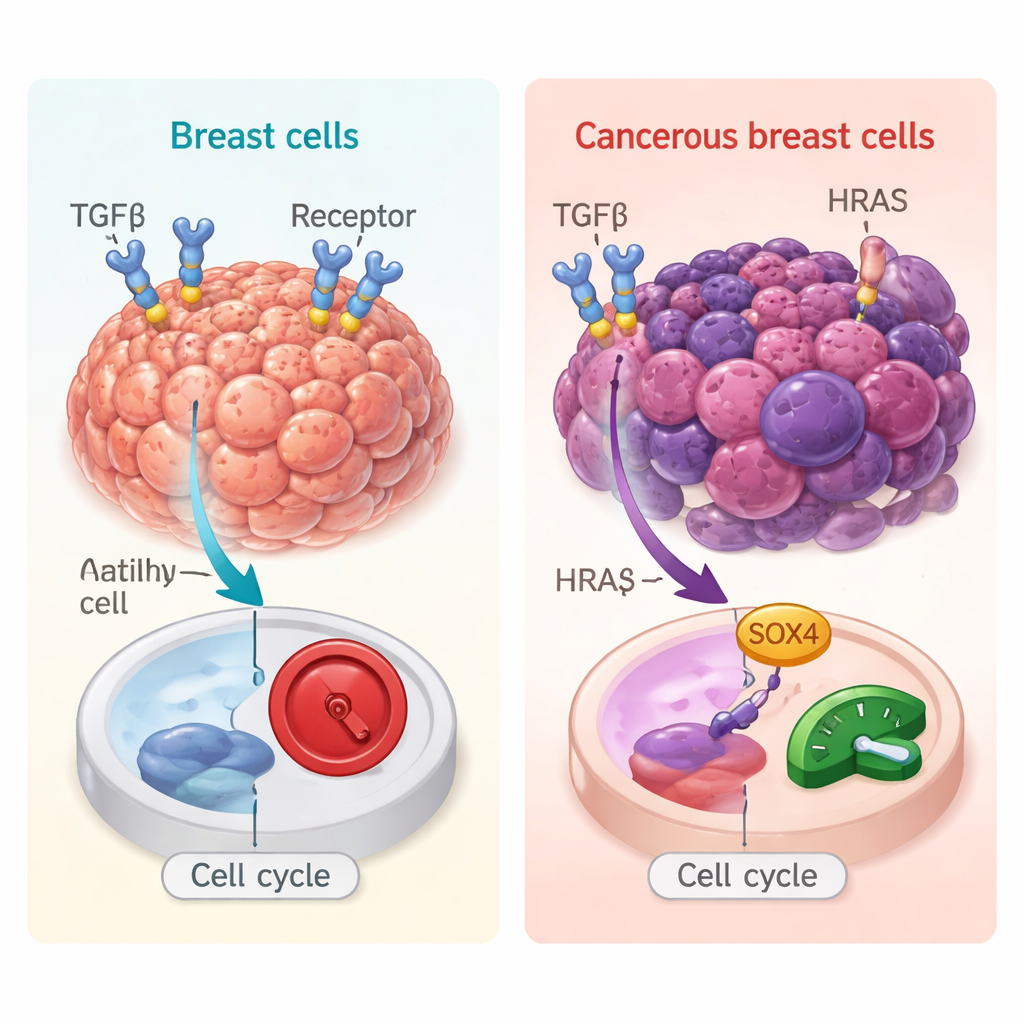
Przebudowa przełączników w genomie
Zespół przyjrzał się chromatynie, opakowaniu DNA i białek, które kontroluje, które geny są dostępne i mogą być włączone. Po traktowaniu trójwymiarowych skupisk komórek TGFβ zaobserwowali rozległe otwieranie chromatyny przy miejscach startu genów oraz w odległych regionach wzmacniających (enhancerach) zarówno w komórkach przypominających normalne, jak i w komórkach z mutacją HRAS. Jednak wzór nowo dostępnych miejsc znacznie różnił się między nimi. W komórkach przypominających nowotworowe szczególnie wzbogacone były miejsca wiązania czynnika transkrypcyjnego nazwanego SOX4. Równocześnie profilowanie ekspresji genów wykazało, że TGFβ nie ogranicza się już tylko do aktywacji znanych programów, takich jak przejście nabłonkowo-mezenchymalne (związane z inwazją) i zmiany metaboliczne; w komórkach z mutacją HRAS TGFβ także wzmacniał geny zaangażowane w replikację DNA, naprawę DNA i przejście przez kluczowe punkty kontrolne cyklu komórkowego.
SOX4 jako molekularny pośrednik
Badając to głębiej, badacze wykazali, że SOX4 stoi w centrum tego przełączenia. Dane z pojedynczych komórek (single-cell RNA sequencing) z pierwotnych guzów piersi ujawniły, że SOX4 jest współekspresjonowany z czynnikami napędzającymi cykl komórkowy, takimi jak CDK4, CDK6 i cyklina D1 (CCND1), szczególnie w aktywnie dzielących się komórkach nowotworowych. W ich trójwymiarowych modelach TGFβ zwiększało poziomy SOX4, a SOX4 stwierdzono związane w pobliżu regionów kontrolnych tych genów cyklu komórkowego, zwłaszcza CDK4. Gdy SOX4 został zmniejszony przy użyciu narzędzi genetycznych, TGFβ nie był już w stanie skutecznie włączać wielu swoich genów docelowych, w tym tych powiązanych z podziałem komórek i przebudową tkanki, a kule nowotworopodobne stały się mniej inwazyjne i bardziej stabilne. Doświadczenia biochemiczne dodatkowo wykazały, że SOX4 współdziała ze SMAD3, kluczowym nośnikiem sygnału TGFβ, tworząc w jądrze moduł kooperatywny, który wzmacnia aktywację genów.
Podważanie leku pierwszego rzutu w raku piersi
Palbocyklib to powszechnie stosowany lek, który blokuje CDK4 i CDK6, białka popychające komórki ze stanu spoczynku do aktywnego podziału. Wielu pacjentów ostatecznie rozwija oporność na to leczenie. Autorzy połączyli obszerne zestawy danych dotyczących odpowiedzi na leki z eksperymentami laboratoryjnymi w wielu liniach komórkowych raka piersi i kulturach 3D. Stwierdzili, że silniejsza aktywność TGFβ, wraz z sygnaturami SOX4 i powiązanymi profilami genowymi, koreluje z wyższymi dawkami palbocyklibu potrzebnymi do zahamowania wzrostu. W warunkach laboratoryjnych dodanie TGFβ zmniejszało wrażliwość komórek nowotworowych na palbocyklib, natomiast blokowanie sygnalizacji TGFβ lub wyciszenie SOX4 przywracało wrażliwość. Długotrwała ekspozycja na palbocyklib prowadziła do powstania linii komórek opornych, które wykazywały nasilone sygnalizowanie TGFβ, więcej SOX4 i silniejsze oznaki aktywnej chromatyny przy samym genie SOX4. W modelach z użyciem ryb danio pręgowanego hamowanie TGFβ istotnie zmniejszało wzrost guzów pochodzących z komórek opornych na palbocyklib.
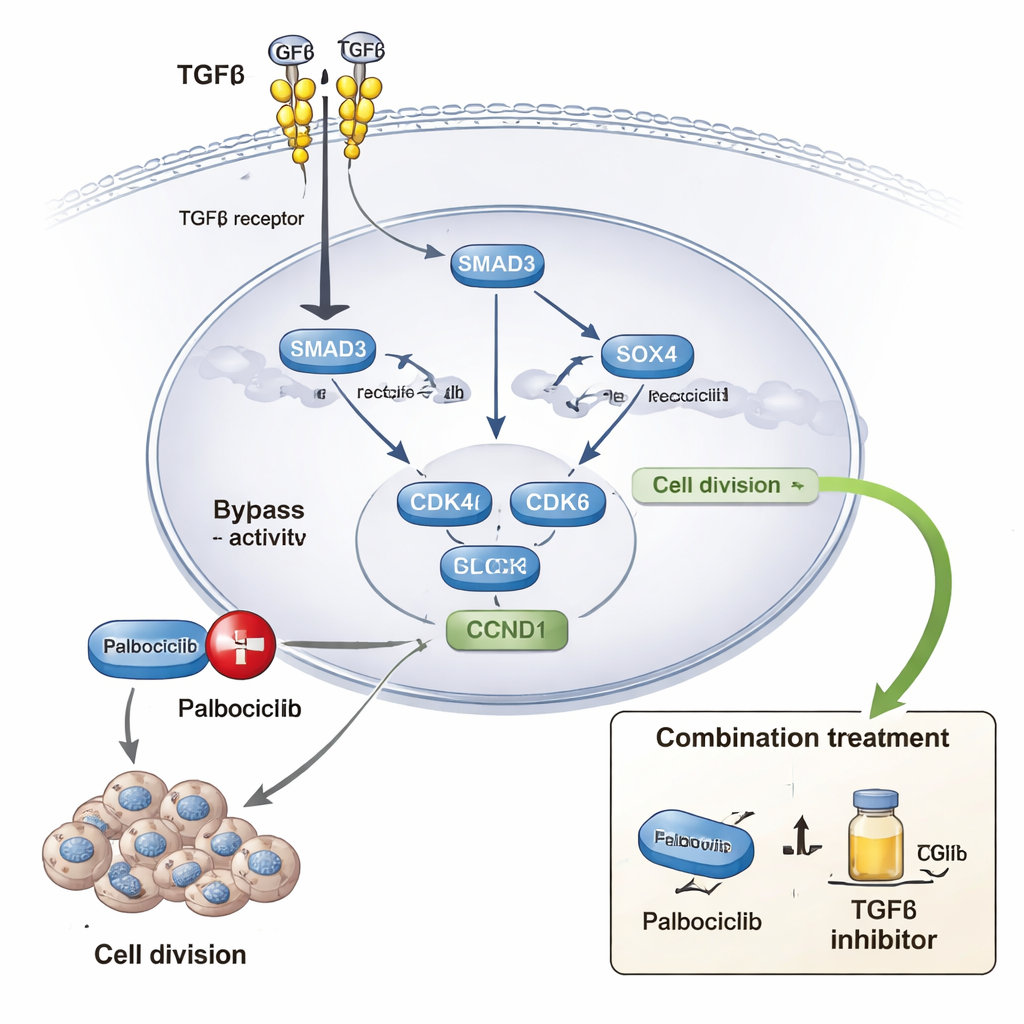
Co to oznacza dla pacjentów i przyszłych terapii
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że sygnał mający nas chronić przed rakiem może, w niewłaściwym kontekście, zostać przejęty, by pomagać guzom przeżyć i przechytrzyć leki. Tutaj TGFβ współpracuje z SOX4, by otworzyć kluczowe regiony genomu, włączyć napędy cyklu komórkowego, takie jak CDK4 i CDK6, i osłabić działanie palbocyklibu. Wyniki sugerują, że w niektórych rakach piersi łączenie inhibitorów CDK4/6 z lekami blokującymi sygnalizację TGFβ — albo celującymi w programy napędzane przez SOX4 — mogłoby opóźnić lub przezwyciężyć oporność. Choć potrzebne są dalsze badania kliniczne, praca ta mapuje szczegółową molekularną drogę ucieczki, z której korzystają komórki nowotworowe, i wskazuje nowe sposoby jej zablokowania.
Cytowanie: Ali, M.M., Itoh, Y., Badji, A.M.P. et al. TGFβ signaling promotes cell cycle progression and resistance to the CDK4/6 inhibitor palbociclib through SOX4 transcriptional modulation in breast cancer cells. Cell Death Dis 17, 209 (2026). https://doi.org/10.1038/s41419-026-08435-4
Słowa kluczowe: rak piersi, sygnalizacja TGF-beta, SOX4, oporność na palbocyklib, cykl komórkowy