Clear Sky Science · pl
BCL-xL jako cel terapeutyczny w raku jelita grubego opornym na cetuksymab
Dlaczego to ma znaczenie dla osób z rakiem jelita
Rak jelita grubego (okrężnicy i odbytnicy) jest jednym z najczęstszych nowotworów na świecie, a wielu pacjentów z zaawansowaną chorobą otrzymuje ukierunkowane przeciwciało terapeutyczne o nazwie cetuksymab. Lek ten może początkowo zmniejszać guzy, ale u większości pacjentów nowotwór po kilku miesiącach znajduje sposoby na obejście terapii, pozostawiając lekarzom niewiele dobrych opcji. To badanie stawia pilne pytanie: gdy guzy jelita przestają reagować na cetuksymab, czy istnieje inne słabe miejsce, które nowe leki mogłyby wykorzystać, aby doprowadzić komórki nowotworowe do śmierci?
Gdy lek ukierunkowany przestaje działać
Cetuksymab działa przez blokowanie anteny powierzchniowej na komórkach nowotworowych zwanej receptorem naskórkowego czynnika wzrostu (EGFR), która napędza ich wzrost. Zespół stworzył laboratoryjny model oporności, wystawiając wrażliwą linię komórek raka jelita grubego (LIM1215) na stopniowo zwiększane dawki cetuksymabu przez sześć miesięcy. Wyłoniły się dwie niezależnie uzyskane populacje oporne, które nadal rosły nawet przy wysokich stężeniach leku, a po usunięciu leku wyglądały równie zdrowo i szybko rosnąco jak komórki wyjściowe. Co istotne, komórki oporne wciąż nosiły docelowy receptor na powierzchni i cetuksymab mógł się do niego wiązać, co sugeruje, że nowotwór nie „ukrył” ani nie zmodyfikował receptorów.
Komórki oporne przekierowują sygnały wzrostu
Aby zrozumieć, jak komórki omijały działanie cetuksymabu, badacze przeanalizowali kluczowe szlaki wzrostu wewnątrz komórki. W komórkach macierzystych cetuksymab zwykle tłumił szlak MAPK, główny mechanizm podziałów komórkowych. W komórkach opornych aktywność MAPK pozostawała wysoka nawet przy zablokowanym EGFR, co pokazuje, że sygnał wzrostu został odłączony od pierwotnego receptora. Sekwencjonowanie RNA komórek ujawniło nowe mutacje aktywujące w innym genie RAS, HRAS, w subpopulacjach komórek opornych, ale nie w innych częstych podejrzanych jak KRAS, NRAS czy BRAF. Próby zablokowania tego przekierowanego sygnalizowania za pomocą inhibitora MEK (działającego poniżej RAS) jedynie umiarkowanie ograniczyły wzrost. To podkreśliło, że zamiast gonić za każdą nową mutacją, efektywniejsze może być zaatakowanie mechanizmów decydujących o życiu i śmierci komórki, wspólnych dla różnych opornych klonów. 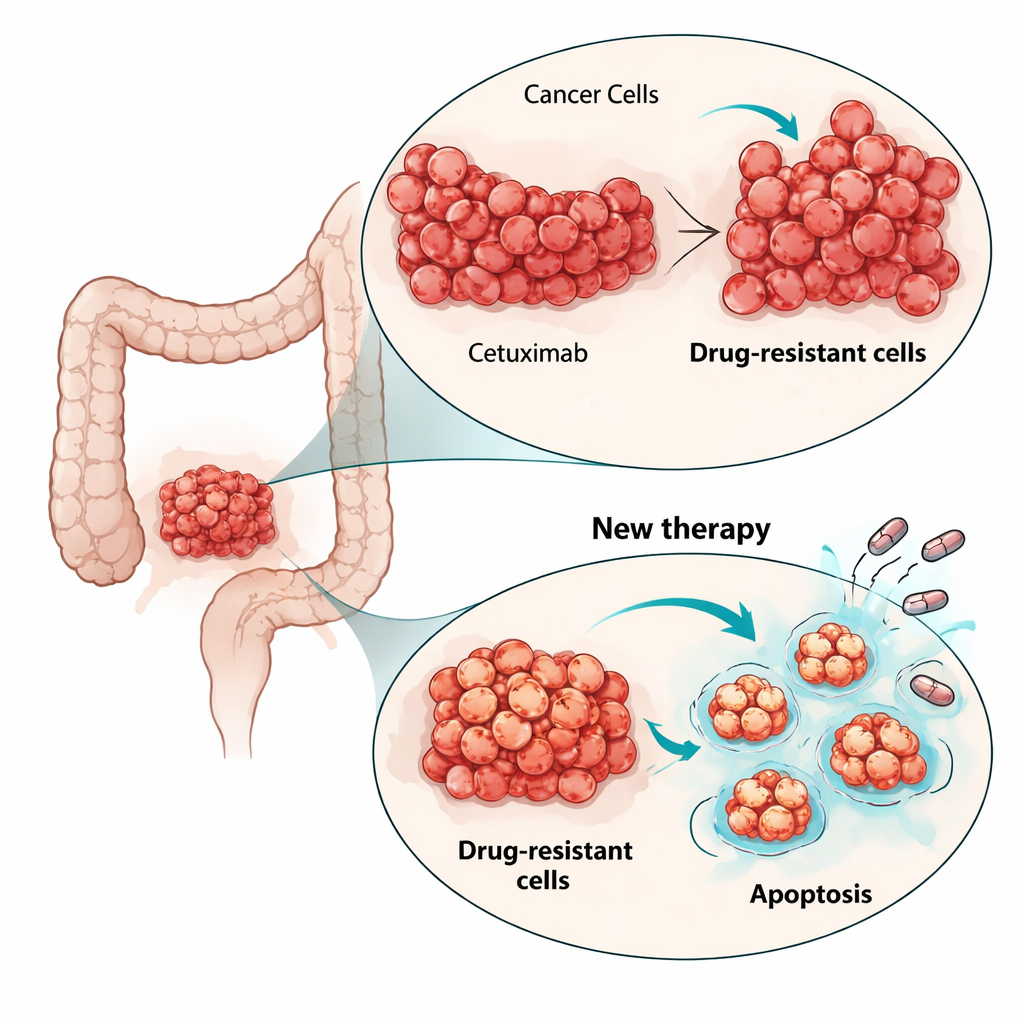
Uderzenie w system podtrzymywania życia nowotworu
Naukowcy zwrócili uwagę na apoptozę, wrodzony program samobójczy komórki, który nowotwory często tłumią. Analiza ekspresji genów wykazała zmiany w szlakach związanych z apoptozą w komórkach opornych. W szczególności antydeatowy białko BCL-xL było podwyższone w jednej populacji opornej i nieco zwiększone w drugiej, podczas gdy inne białko pro-przeżyciowe, MCL-1, także było obecne. Zespół przetestował małocząsteczkowe leki zwane mimetykami BH3, zaprojektowane do blokowania tych białek przeżyciowych i uwalniania machiny śmierci. W hodowlach dwuwymiarowych wszystkie trzy linie komórek — macierzyste i oporne — były wrażliwe na leki blokujące BCL-xL lub MCL-1, ale co zaskakujące, niższe dawki zabijały komórki oporne na cetuksymab skuteczniej. Dodanie niskiej dawki inhibitora proteasomu bortezomibu, który sprzyja akumulacji sygnałów pro-śmierci, dodatkowo zwiększyło efekt, szczególnie w połączeniu z blokadą MCL-1.
Od płaskich naczyń do trójwymiarowych mini-guzów i tkanek pacjentów
Ponieważ płaskie warstwy komórek nie oddają w pełni specyfiki guzów w organizmie, zespół hodował następnie komórki jako trójwymiarowe sferoidy zatopione w żelu, co lepiej odzwierciedla architekturę i problemy z penetracją leków w prawdziwych guzach. Ponownie, blokada BCL-xL lub MCL-1 zmniejszała przeżywalność sferoidów, a łączenie tych leków z bortezomibem powodowało dramatyczne spadki aktywności metabolicznej i wyraźne oznaki śmierci komórek. Aby sprawdzić, czy ta podatność występuje w bardziej realistycznym materiale ludzkim, użyli cienkich placek guzów opornych na cetuksymab, hodowanych w myszach na bazie nowotworów pochodzących od pacjentów (patient-derived xenografts). Modele te były wszystkie typu KRAS dziki, podobnie jak oryginalne komórki LIM1215, ale nosiły różnorodne dodatkowe mutacje, w tym w BRAF i TP53, odzwierciedlając genetyczną różnorodność obserwowaną w klinice. 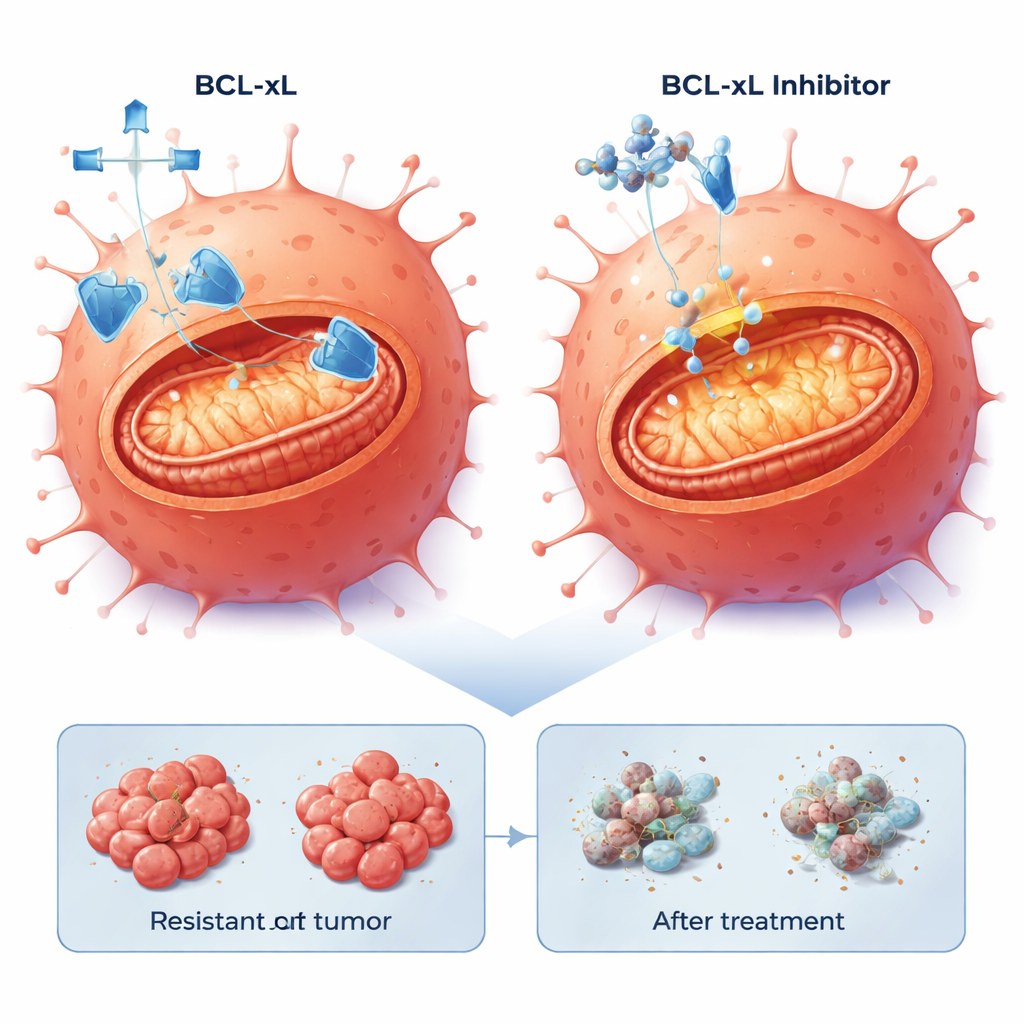
Celowanie w BCL-xL działa w różnych opornych guzach
W tych wycinkach guzów pochodzących od pacjentów, połączenie inhibitora BCL-xL z niską dawką bortezomibu konsekwentnie wywoływało silną śmierć komórek w 20–40% komórek guza w czterech różnych modelach, w tym w tych z agresywnymi mutacjami BRAF. Natomiast blokada MCL-1 z użyciem bortezomibu przynosiła silne efekty tylko w części guzów. Co ważne, zdolność komórek opornych do uruchomienia apoptozy była zachowana: po usunięciu „siatki bezpieczeństwa” BCL-xL wewnętrzny program śmierci mógł zostać aktywowany, niezależnie od tego, jaką genetyczną drogą guz uciekł przed cetuksymabem.
Co to oznacza dla pacjentów
Dla osób, których rak jelita grubego przestał reagować na cetuksymab, to badanie daje powód do ostrożnego optymizmu. Sugeruje, że nawet po rozwoju oporności na terapię ukierunkowaną na EGFR wiele komórek nowotworowych pozostaje gotowych do śmierci, jeśli zablokuje się kluczowe białko przeżyciowe BCL-xL. Chociaż inhibitory BCL-xL mogą powodować działania niepożądane, szczególnie w odniesieniu do płytek krwi, praca ta wskazuje na strategie łączenia leków i optymalizacji dawek, które mogłyby ograniczyć toksyczność, jednocześnie wykorzystując wspólny Achillesowy piętę trudnych do leczenia guzów. W przyszłości leki unieszkodliwiające BCL-xL mogłyby stać się podstawą nowych terapii drugiego rzutu dla raka jelita grubego opornego na cetuksymab, niezbyt zależnych od zmiennego pejzażu mutacyjnego guza.
Cytowanie: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Słowa kluczowe: rak jelita grubego, oporność na leki, cetuksymab, inhibicja BCL-xL, apoptoza