Clear Sky Science · pl
LAP2α napędza rozwój raka piersi poprzez łagodzenie stresu replikacyjnego
Dlaczego to ma znaczenie dla raka piersi
Guzy piersi rosną częściowo dlatego, że komórki nowotworowe znajdują sposoby na przetrwanie stałego stresu podczas kopiowania DNA. To badanie ujawnia, jak mniej znane białko o nazwie LAP2α pomaga komórkom raka piersi chronić DNA w trakcie replikacji, wspierając wzrost guza i utrudniając leczenie. Zrozumienie tego ukrytego systemu wsparcia sugeruje nowe sposoby osłabienia nowotworów i poprawy skuteczności istniejących leków.
Ukryty pomocnik w jądrze komórki nowotworowej
Za każdym razem, gdy komórka dzieli się, musi dokładnie skopiować swoje DNA. W komórkach nowotworowych proces ten jest szczególnie obciążony: sygnały wzrostu są stale „włączone”, a aparat replikacyjny pracuje na granicy możliwości. To przeciążenie, zwane stresem replikacyjnym, odsłania odcinki jednoniciowego DNA, które muszą być szybko pokryte i ustabilizowane przez kompleks białkowy RPA. Autorzy wcześniejszych badań stwierdzili, że LAP2α, białko powiązane ze szkieletowym wnętrzem jądra, może wiązać RPA i pomagać mu docierać do uszkodzonego DNA. W obecnej pracy pytali, czy partnerstwo LAP2α–RPA faktycznie napędza rozwój raka piersi i wpływa na odpowiedź guza na leczenie.
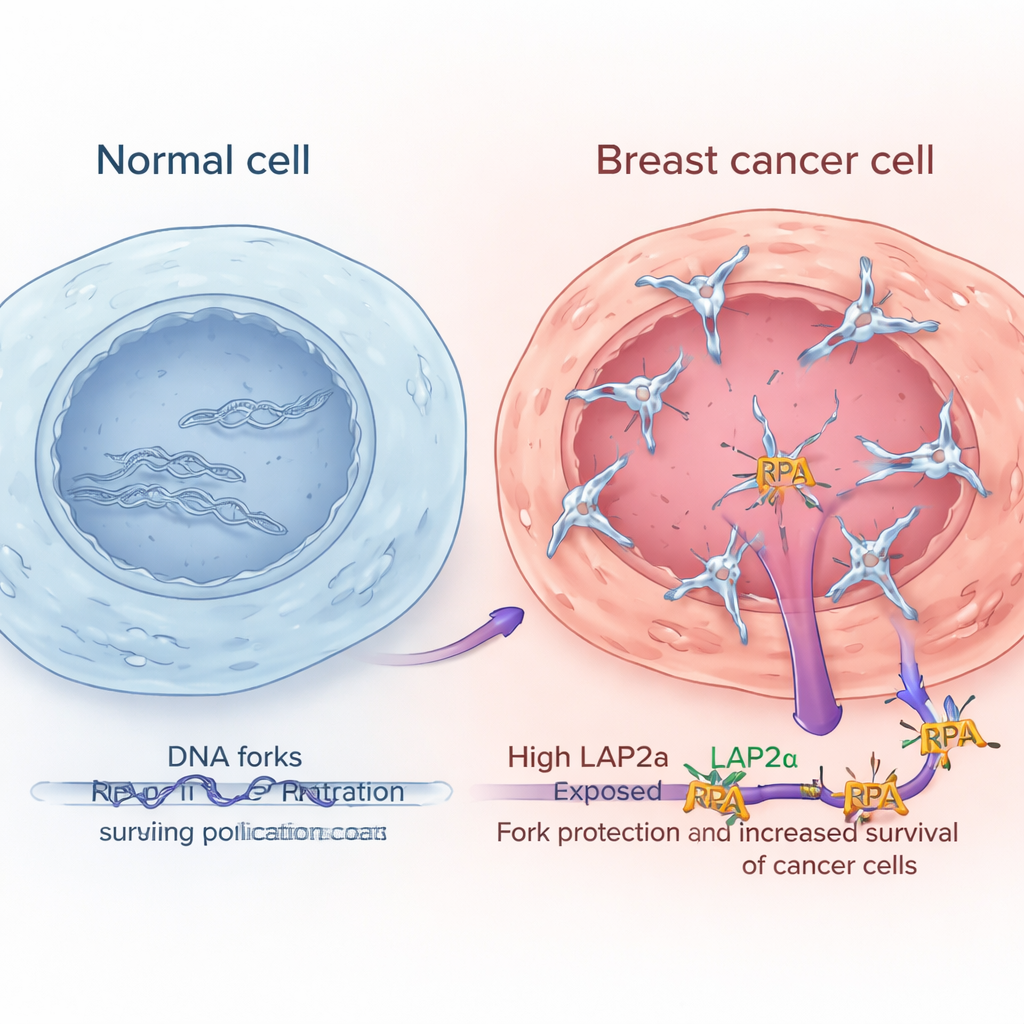
Wysokie poziomy LAP2α oznaczają bardziej agresywne guzy piersi
Analizując duże publiczne zestawy danych ekspresji genów i badając próbki guzów pod mikroskopem, badacze wykazali, że LAP2α jest konsekwentnie podwyższone w tkance raka piersi w porównaniu z sąsiednią prawidłową tkanką piersi. Jego poziomy rosną wraz z stopniem zaawansowania guza, co oznacza, że bardziej nieprawidłowe i agresywne nowotwory mają tendencję do większej zawartości LAP2α. Wzorzec ten pojawiał się w wielu głównych podtypach raka piersi, w tym hormonozależnych, HER2-wzbogaconych i potrójnie ujemnych. Co ważne dla pacjentów, osoby, których guzy miały wysoki poziom LAP2α, częściej miały gorsze przeżycie. Dla porównania, podstawowe składowe kompleksu RPA same w sobie nie wykazywały podobnych zmian ani wyraźnych powiązań z wynikami, co sugeruje, że to wzmocniona funkcja LAP2α, a nie jedynie większa ilość RPA, pomaga komórkom nowotworowym radzić sobie ze stresem replikacyjnym.
Wyłączenie LAP2α hamuje guzy i ujawnia słabe punkty
Aby wyjść poza korelacje, zespół użył modeli mysich raka piersi, w których LAP2α można było selektywnie usunąć. Gdy guzy gruczołu sutkowego już się pojawiły, genetyczne usunięcie LAP2α spowodowało wolniejszy wzrost nowotworów i wydłużyło przeżycie zwierząt. Komórki nowotworowe pozbawione LAP2α dzieliły się rzadziej i wykazywały więcej oznak uszkodzeń DNA, o czym świadczyło zwiększone barwienie markerów pęknięć DNA oraz zmniejszone pokrycie DNA przez RPA. Gdy takie komórki przeniesiono do nowych myszy, ponownie tworzyły mniejsze guzy i wykazywały zwiększoną wrażliwość na chemioterapię uszkadzającą DNA, w tym platynowy lek cisplatynę oraz inhibitor PARP. Podobne eksperymenty na ludzkich liniach komórek raka piersi potwierdziły, że redukcja LAP2α zwiększa podatność komórek na kilka leków genotoksycznych, podczas gdy przywrócenie normalnego LAP2α — ale nie formy mutantowej, która nie może wiązać RPA — przywracało zarówno ochronę DNA, jak i odporność na leki.
Jak LAP2α pomaga chronić kruche nici DNA
Aby rozpracować mechanizm, badacze odtworzyli etapy wiązania DNA w warunkach in vitro. Mieszali oczyszczone RPA, jednoniciowe DNA oraz albo normalne LAP2α, albo wariant niezdolny do interakcji z RPA. Stwierdzili, że LAP2α bezpośrednio zwiększa efektywność, z jaką RPA pokrywa jednoniciowe DNA, i pomaga RPA rozciągać oraz stabilizować te kruche regiony, działając niczym asystent ładujący lub „opiekun”. Gdy obecne było DNA, RPA miało tendencję do odłączania się od LAP2α i pełnego zaangażowania się w wiązanie nici, co pokazuje, że LAP2α nie jest częścią końcowego ochronnego płaszcza, lecz przekazuje RPA DNA. Bez funkcjonalnej interakcji LAP2α–RPA więcej widełek replikacyjnych ulegało załamaniu, kumulowały się pęknięcia DNA, a komórki nowotworowe były bardziej skłonne do śmierci, zwłaszcza gdy dodatkowe uszkodzenia wprowadzano chemioterapią.
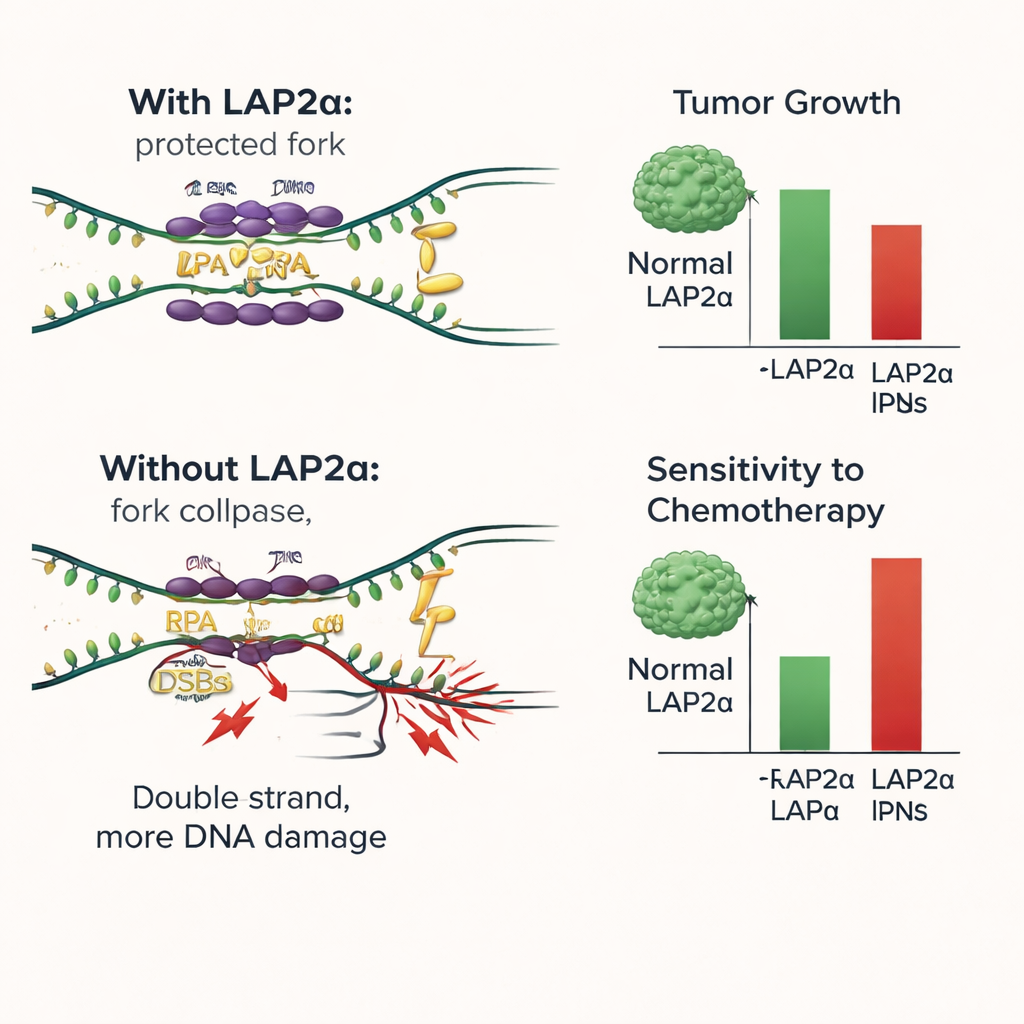
Co to znaczy dla przyszłego leczenia raka piersi
Mówiąc wprost, badanie pokazuje, że LAP2α działa jak pomocnik zza kulis, który pomaga komórkom raka piersi przetrwać obciążenie związane z kopiowaniem DNA. Poprzez wydajne ładowanie RPA na wrażliwe odcinki DNA, LAP2α redukuje uszkodzenia i wspiera dalszy wzrost guza. Usunięcie lub unieruchomienie LAP2α przechyla szalę: uszkodzeń DNA przybywa, komórki przestają się dzielić, a konwencjonalne leki atakujące DNA stają się skuteczniejsze. Wyniki te sugerują, że LAP2α może służyć jako marker złego rokowania oraz jako nowy cel terapeutyczny. Leki blokujące LAP2α lub jego wiązanie z RPA mogłyby poprawić działanie istniejących terapii, takich jak środki platynowe i inhibitory PARP, szczególnie w guzach silnie polegających na tym systemie buforowania stresu.
Cytowanie: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Słowa kluczowe: rak piersi, stres replikacyjny DNA, LAP2 alfa, białko replikacyjne A, wrażliwość na chemioterapię