Clear Sky Science · pl
Celowanie w biosyntezę glicerofosfolipidów przezwycięża oporność na chemioterapię wynikającą z utraty SLFN11 w mięsaku Ewinga
Dlaczego te badania są ważne dla nowotworów wieku dziecięcego
Mięsak Ewinga to rzadki, lecz agresywny nowotwór, który głównie dotyka dzieci i nastolatków. Wielu pacjentów początkowo dobrze reaguje na chemioterapię, ale u tych, u których choroba nawraca, obecne leczenie często zawodzi. W badaniu zadano pilne pytanie: kiedy komórki mięsaka Ewinga stają się oporne na chemioterapię, jakie zmiany wewnątrz nich pozwalają im przetrwać — i czy te zmiany można wykorzystać jako nowe słabe punkty do zaatakowania przez terapię?
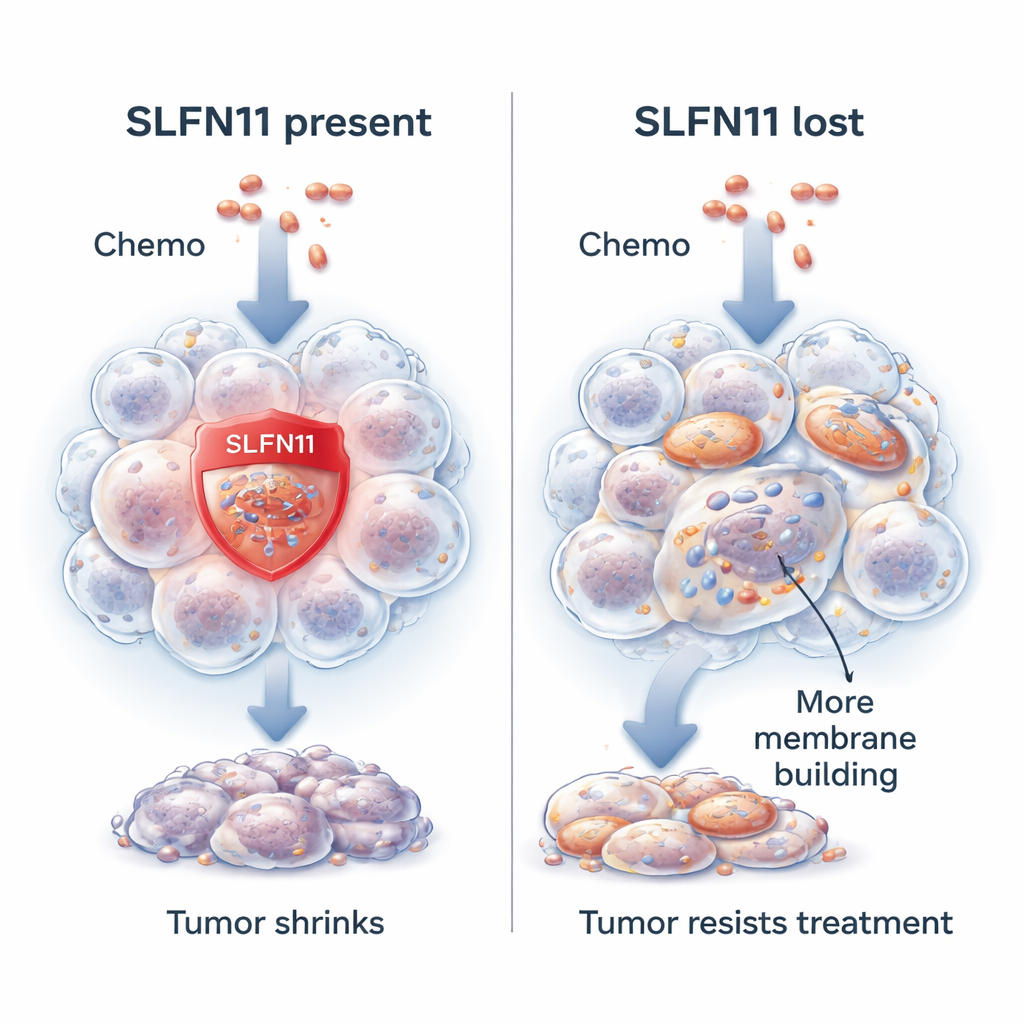
Gen, który ułatwia zabijanie komórek nowotworowych
Naukowcy skupili się na genie o nazwie SLFN11. W wielu guzach mięsaka Ewinga SLFN11 jest silnie aktywny i sprawia, że komórki nowotworowe są znacznie bardziej wrażliwe na leki uszkadzające DNA, czyli plan genetyczny komórki. Podawane leki w obecności SLFN11 utrudniają naprawę DNA i skłaniają komórkę nowotworową do śmierci. Pacjenci, których guzy mają wyższy poziom SLFN11, zwykle żyją dłużej i lepiej reagują na leczenie. Jednak około jednej na dziesięć zmian rozwija się z niewielką lub żadną ekspresją SLFN11 albo traci ją w trakcie terapii. W takiej sytuacji ta sama chemioterapia jest znacznie mniej skuteczna, mimo że komórki nowotworowe dalej potrafią się intensywnie dzielić.
Jak komórki nowotworowe przebudowują wykorzystanie paliwa i tłuszczów
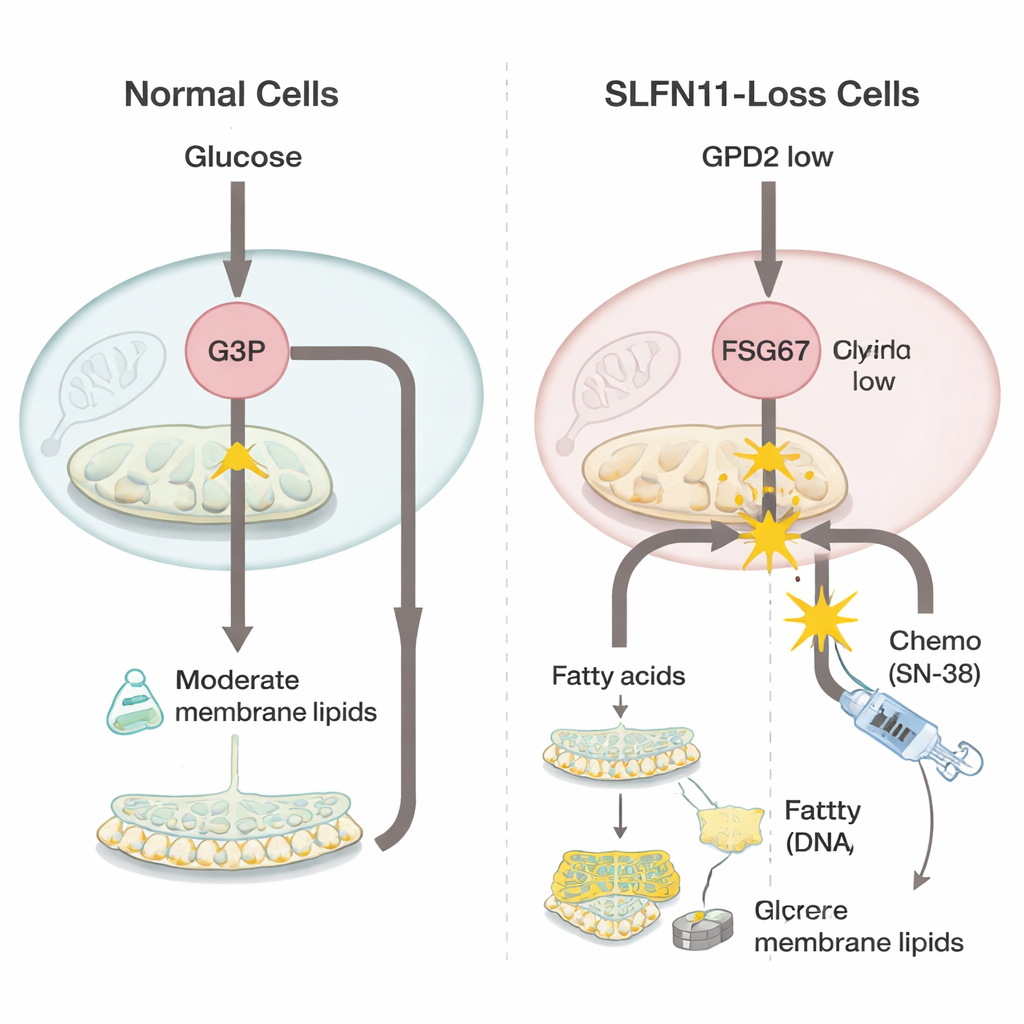
Aby zrozumieć zmiany po utracie SLFN11, zespół porównał komórki mięsaka Ewinga z aktywnym i bez aktywnego tego genu, korzystając z zaawansowanych narzędzi „omics”, które mierzą jednocześnie tysiące genów i małych cząsteczek. Odkryli, że komórki pozbawione SLFN11 obniżają poziom enzymu w mitochondriach nazwanego GPD2, który normalnie pomaga utleniać glicerolo‑3‑fosforan w procesie produkcji energii. Gdy GPD2 jest zredukowany, glicerolo‑3‑fosforan się kumuluje. Zamiast być marnotrawiony, nadmiar tego prekursoru zostaje skierowany do produkcji większej ilości cząsteczek tłuszczowych tworzących błony komórkowe — grupy znanej jako glicerofosfolipidy. Komórki wykazywały też oznaki zwiększonego tworzenia bardziej płynnych, nienasyconych kwasów tłuszczowych, co może pomagać szybko rosnącym nowotworom przystosować się do stresu.
Przekształcenie triku przetrwania w punkt wrażliwy
Ponieważ te komórki z niedoborem SLFN11 silniej polegają na budowie błon, naukowcy sprawdzili, czy zablokowanie tego procesu może przywrócić wrażliwość na chemioterapię. Użyli związku o nazwie FSG67, który hamuje kluczowy etap produkcji glicerofosfolipidów. Sam lek DNA‑uszkadzający SN‑38 stał się w komórkach pozbawionych SLFN11 znacznie mniej skuteczny, odzwierciedlając kliniczny problem oporności. Jednak gdy SN‑38 połączono z FSG67, wcześniej oporne komórki były znacznie mocniej atakowane, a oba leki działały razem lepiej niż można by się spodziewać po ich indywidualnych efektach. Natomiast w komórkach z zachowanym SLFN11, które już były bardzo wrażliwe na SN‑38, dodanie FSG67 przynosiło niewielką korzyść, a czasem mogło być nieco niekorzystne. Ten wzorzec sugeruje, że nowo nabyta zależność od produkcji tłuszczów i błon jest specyficzna dla stanu odpornego z niskim SLFN11.
Potencjalny nieinwazyjny sygnał trudnych do leczenia guzów
Naukowcy zapytali następnie, czy tę metaboliczną przebudowę można wykryć w rzeczywistych guzach, a nie tylko w komórkach w laboratorium. Hodowali guzy mięsaka Ewinga u myszy, z i bez SLFN11, i użyli magnetycznego rezonansu jądrowego (NMR), aby zbadać skład chemiczny ekstraktów guzów. Guzy pozbawione SLFN11 wykazywały wyższy stosunek dwóch cząsteczek zawierających cholinę związanych z obrotem błon: fosfocholiny i glicerofosfocholiny. Wysoki stosunek fosfocholiny do glicerofosfocholiny był w innych nowotworach powiązany z bardziej agresywnym zachowaniem i gorszą odpowiedzią na leczenie. Ponieważ sygnały choliny można mierzyć za pomocą zaawansowanych technik obrazowania, taki przesunięty profil może w przyszłości posłużyć jako nieinwazyjny marker wskazujący na guzy mięsaka Ewinga, które przyjęły ten oporny, zorientowany na budowę błon tryb.
Co to może oznaczać dla przyszłych terapii
Podsumowując, badanie pokazuje, że gdy komórki mięsaka Ewinga tracą SLFN11 i stają się mniej wrażliwe na chemioterapię uszkadzającą DNA, rekompensują to przebudowując metabolizm w stronę zwiększonej produkcji tłuszczów błonowych. Ta zmiana nie tylko pomaga komórkom przetrwać; tworzy też nową piętę Achillesa. Zablokowanie produkcji glicerofosfolipidów za pomocą leku podobnego do FSG67 może częściowo przywrócić skuteczność chemioterapii w tych opornych komórkach. Chociaż sam FSG67 nie jest jeszcze lekiem klinicznym, praca wskazuje strategię, w której lekarze mogli by w przyszłości dopasowywać leczenie do statusu SLFN11 i cech metabolicznych guza, łącząc terapie uszkadzające DNA z ukierunkowanymi inhibitorami syntezy tłuszczów i błon, aby pokonać oporność.
Cytowanie: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Słowa kluczowe: mięsak Ewinga, oporność na chemioterapię, SLFN11, metabolizm nowotworowy, biosynteza lipidów