Clear Sky Science · pl
Celowanie w egzosomalne IGFBP2 wywołane hipoksją pokonuje ucieczkę przed układem odpornościowym zależną od CD47 w glejaku
Dlaczego pozbawianie guza tlenu może się obrócić przeciwko nam
Lekarze od dawna wiedzą, że glejak, śmiertelny nowotwór mózgu, często rozwija się w obszarach pozbawionych tlenu. Te hipoksyczne kieszenie utrudniają leczenie guza. Badanie ujawnia, w jaki sposób niski poziom tlenu pomaga komórkom nowotworowym ukryć się przed układem odpornościowym i proponuje nowe skojarzone podejście terapeutyczne, które może uczynić je bardziej podatnymi na atak ze strony organizmu.
Śmiertelny guz mózgu, który omija nasze obrony
Glejak jest najagresywniejszym powszechnym nowotworem mózgu u dorosłych, a typowy czas przeżycia liczy się w miesiącach. Mimo że komórki odpornościowe infiltrują te guzy, komórki nowotworowe często unikają zniszczenia. Jedną z kluczowych dróg ucieczki jest białko powierzchniowe o nazwie CD47, nazywane czasem sygnałem „nie zjadaj mnie”, które informuje pobliskie komórki odpornościowe, takie jak makrofagi, by nie pochłaniały i nie niszczyły komórki nowotworowej. Leki blokujące CD47 są już testowane, ale wyniki w guzach litych, takich jak glejak, były mieszane, co sugeruje, że inne czynniki w mikrośrodowisku guza mogą osłabiać skuteczność tych terapii.
Strefy hipoksji i maleńkie paczuszki nowotworowe
Wykorzystując sekwencjonowanie RNA pojedynczych komórek, badacze zmapowali tysiące komórek z różnych regionów próbek glejaka, porównując nisko-tlenowe jądro guza z jego obwodem. Odkryli szczególnie agresywny podtyp komórek w hipoksycznym jądrze, określany jako komórki GBM o cechach mezenchymalnych, który silnie ekspresjonował CD47 i białko IGFBP2. Jednocześnie zauważyli, że komórki z jądra uwalniały dużą liczbę nano-wielkości pęcherzyków zwanych egzosomami, które niosły IGFBP2 na swojej powierzchni. Ponieważ egzosomy mogą przemieszczać się przez mózg, a nawet dostać się do krwiobiegu, mogą rozsiewać sygnały daleko poza miejsce powstania. 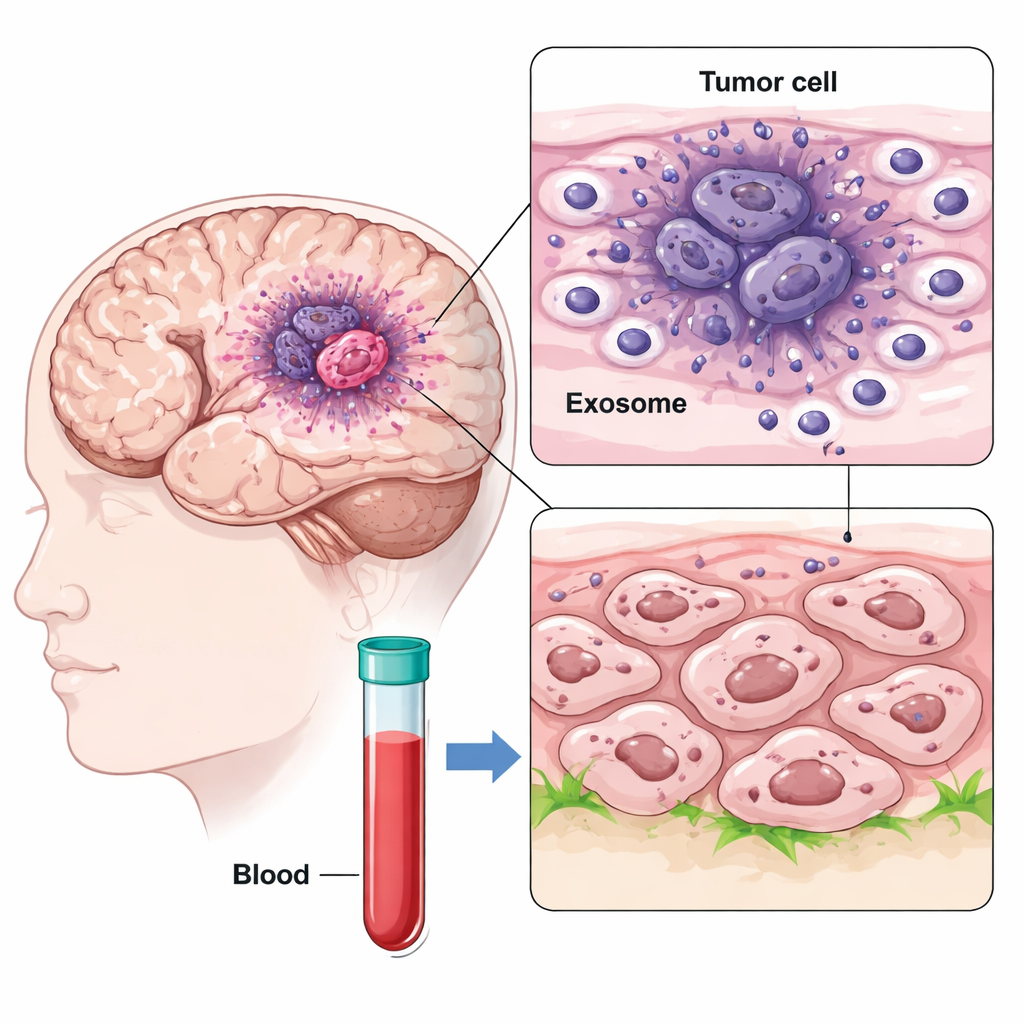
Jak białko partnerujące wzmacnia sygnał „nie zjadaj mnie”
Zespół następnie zbadał rolę IGFBP2. Wykazali, że przy niskim poziomie tlenu czujnik hipoksji, białko HIF-2α, włącza gen IGFBP2 w komórkach nowotworowych. IGFBP2 wiąże się wtedy z określonymi receptorami o nazwie integryny na powierzchni egzosomów, ozdabiając ich zewnętrzną błonę. Kiedy te egzosomy pokryte IGFBP2 łączą się z innymi komórkami nowotworowymi, aktywują kaskadę sygnałową wewnątrz komórki obejmującą białka znane jako FAK i STAT3. Ten łańcuch zdarzeń ostatecznie zwiększa ilość CD47 na powierzchni komórki nowotworowej, wzmacniając komunikat „nie zjadaj mnie” do makrofagów i jeszcze bardziej chroniąc komórki nowotworowe przed atakiem immunologicznym. 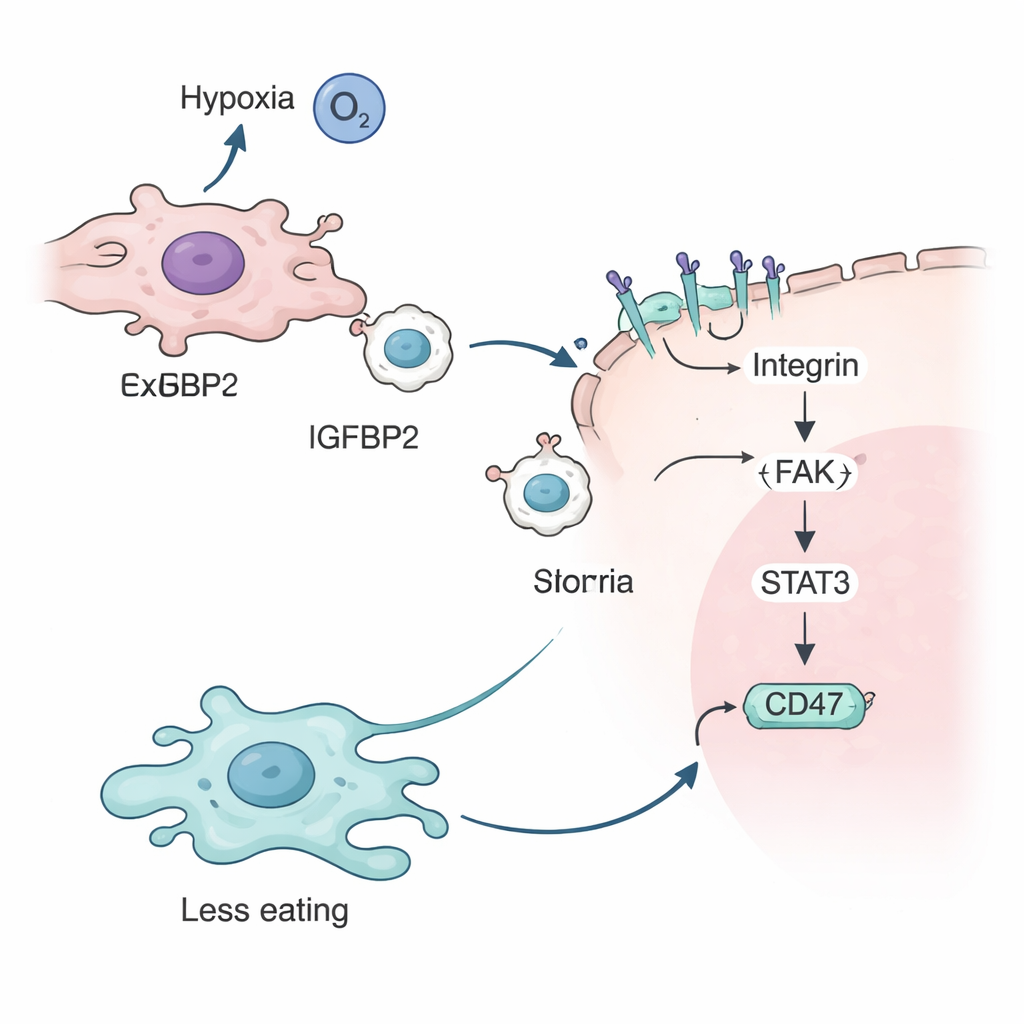
Dowody z próbek pacjentów i modeli zwierzęcych
Aby powiązać te odkrycia z rzeczywistą chorobą, badacze zbadali tkankę nowotworową i krew osób z glejakiem. Stwierdzili, że poziomy IGFBP2 były wyższe zarówno w guzach, jak i w egzosomach z krwi pacjentów z bardziej zaawansowaną chorobą, co sugeruje, że egzosomy zawierające IGFBP2 mogą służyć jako marker stopnia zaawansowania guza wykrywalny we krwi. W modelach mysi obniżenie IGFBP2 w komórkach glejaka uczyniło je bardziej podatnymi na pochłanianie przez makrofagi, spowolniło wzrost guza i wydłużyło przeżycie. Odwrotnie, dodanie dodatkowych egzosomów bogatych w IGFBP2 zwiększało poziomy CD47, ograniczało fagocytozę przez komórki odpornościowe i przyspieszało postęp guza.
Obiecujący cios terapeutyczny z dwóch stron
Wreszcie zespół sprawdził, czy zablokowanie IGFBP2 może zwiększyć skuteczność terapii ukierunkowanej na CD47. U myszy z guzami mózgu leczenie przeciwciałami przeciwko zarówno IGFBP2, jak i CD47 prowadziło do silniejszej aktywności makrofagów, mniejszych guzów i dłuższego przeżycia niż każde z leczeń osobno. Przez odcięcie napędu IGFBP2 wywołanego hipoksją i jednoczesne bezpośrednie zablokowanie sygnału CD47 „nie zjadaj mnie”, ta terapia skojarzona atakowała immunologiczną kamuflaż guza z dwóch stron. Dla pacjentów wyniki te sugerują, że pomiar IGFBP2 w egzosomach krwi może pomóc zidentyfikować tych, którzy najprawdopodobniej skorzystają na immunoterapii skierowanej przeciwko CD47, a łączenie inhibitorów IGFBP2 i CD47 może być silniejszą strategią przeciwko glejakowi niż stosowanie któregokolwiek z tych leków osobno.
Cytowanie: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Słowa kluczowe: glejak, egzosomy, ucieczka przed układem odpornościowym, CD47, hipoksja