Clear Sky Science · pl
HSPA5 promuje stabilność YAP/TAZ niezależnie od szlaku Hippo i indukuje przejście proneural‑to‑mesenchymal w glejakomie
Dlaczego to badanie raka mózgu ma znaczenie
Glejak (glioblastoma) jest jednym z najbardziej śmiertelnych nowotworów mózgu, częściowo dlatego, że wiele guzów z czasem przechodzi w bardziej oporny na leczenie stan. To badanie ujawnia, jak powszechny białkowy mechanizm odpowiedzi na stres, HSPA5, pomaga napędzać tę przemianę i wydłuża czas działania molekuł sprzyjających nowotworowi. Zrozumienie tego „triku przeżyciowego” wskazuje nowe sposoby, by uczynić glejaka mniej agresywnym i bardziej podatnym na istniejące terapie.
Guz, który zmienia swoją „osobowość”
Lekarze i naukowcy rozpoznają dziś, że glejak nie jest jedną chorobą, lecz zbiorem podtypów molekularnych. Dwa główne warianty to forma „proneuralna”, zwykle nieco mniej agresywna, oraz forma „mezenchymalna”, bardziej inwazyjna, oporna na leczenie i związana z wcześniejszym nawrotem. Guzy mogą ewoluować z fenotypu proneuralnego w mezenchymalny — proces, który autorzy nazywają przejściem proneural‑to‑mesenchymal (PMT). Zespół postanowił odnaleźć białka odpowiedzi na stres, które mogłyby popychać guzy w tym niebezpiecznym kierunku.
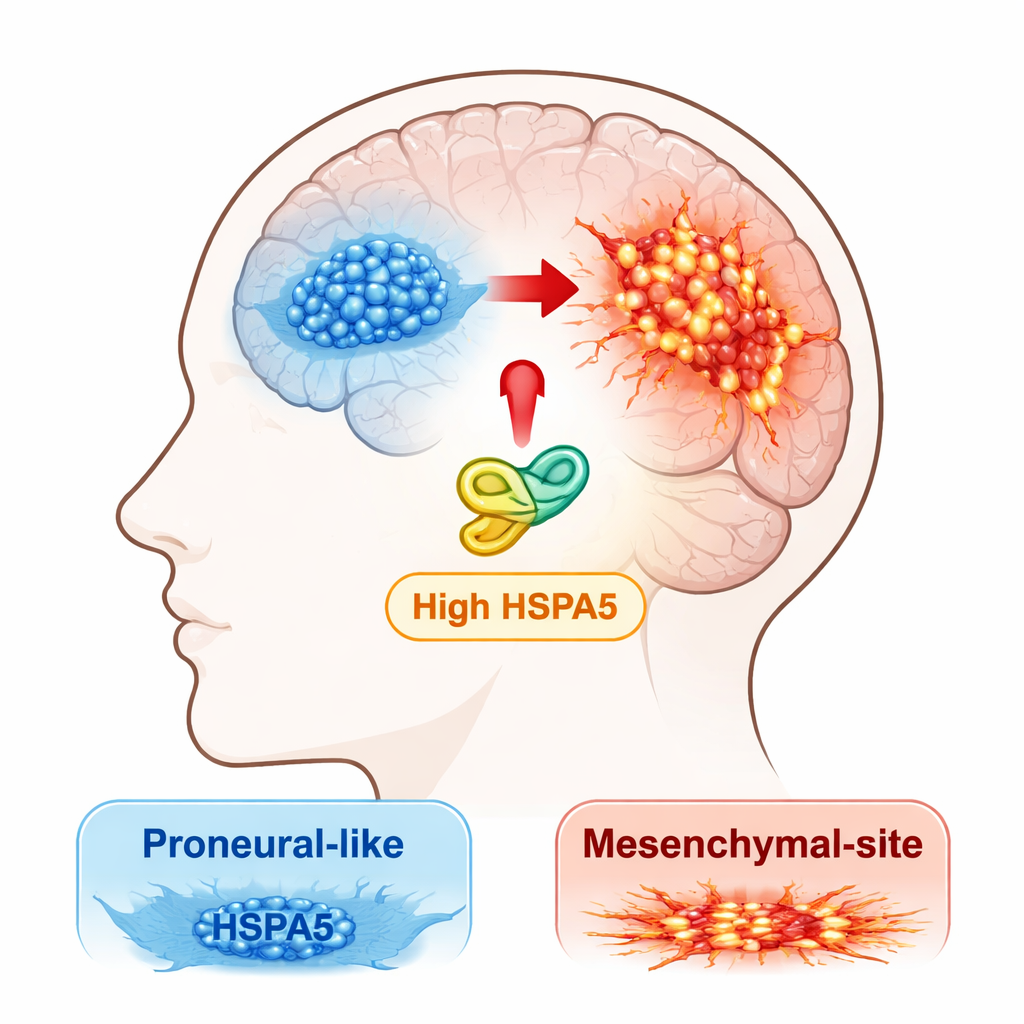
Białko pomocnicze w centrum uwagi
Badacze rozpoczęli od przeszukania dużych publicznych baz danych nowotworowych i własnych próbek pacjentów w poszukiwaniu członków rodziny HSP70, grupy białek „opiekunów” (chaperonów), które pomagają innym białkom poprawnie się fałdować i przetrwać stres. Jednym z wyróżniających się chaperonów był HSPA5. Jego aktywność była najwyższa w podtypie mezenchymalnym glejaka i zdecydowanie wyższa w guzach niż w normalnej tkance mózgowej. Pacjenci z guzami o podwyższonym poziomie HSPA5 mieli gorsze przeżycie ogólne, co wskazuje, że może on być czynnikiem napędzającym agresywną chorobę, a nie tylko biernym obserwatorem.
Wymuszanie bardziej agresywnego fenotypu
Aby zbadać, co HSPA5 robi w komórkach nowotworowych, zespół hodował pierwotne komórki glejaka pobrane bezpośrednio od pacjentów i podzielił je na grupy przypominające fenotyp proneuralny i mezenchymalny. Gdy zmuszono komórki proneuralne do wytwarzania dodatkowego HSPA5, zaczęły one zachowywać się jak komórki mezenchymalne: dzieliły się szybciej, bardziej migrowały i inwadowały oraz włączały charakterystyczne markery mezenchymalne, takie jak CD44 i c‑MET, przy jednoczesnym osłabieniu markerów proneuralnych, jak SOX2 i OLIG2. Odwrotny efekt też występował — obniżenie poziomu HSPA5 w komórkach mezenchymalnych zmniejszało ich wzrost i inwazyjność oraz częściowo przesuwało je z powrotem ku mniej agresywnemu profilowi.
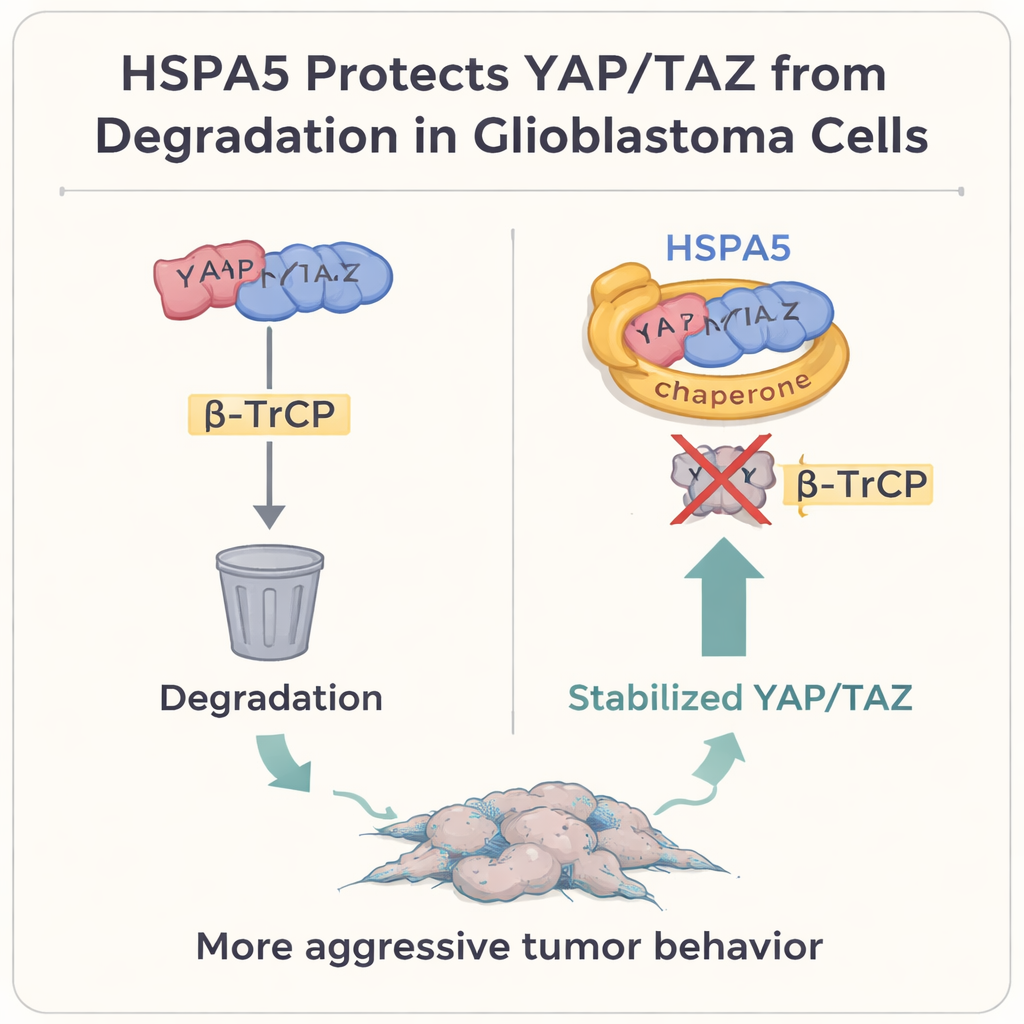
Chroniąc kluczowe przełączniki wzrostu przed komórkową „koszem na śmieci”
Zagłębiając się dalej, autorzy skupili się na dwóch silnych regulatorach wzrostu, YAP i TAZ, które znajdują się w centrum szlaku sygnałowego Hippo. W wielu nowotworach litych, w tym w glejaku, białka te działają jak główne przełączniki promujące wzrost komórek, plastyczność i stan mezenchymalny. Zwykle, gdy komórka chce zdusić ten program, oznacza YAP i TAZ do zniszczenia poprzez białko β‑TrCP, które odprowadza je do „kosza na śmieci” komórki — proteasomu. Badanie pokazuje, że HSPA5 fizycznie wiąże się z YAP i TAZ, używając swojej domeny wiążącej substrat jak ochronnej rękawicy. W ten sposób blokuje przyłączanie β‑TrCP, zapobiega ubikwitynacji i degradacji YAP/TAZ oraz pozwala im gromadzić się w jądrze, gdzie włączają geny mezenchymalne, w tym CD44 i c‑MET.
Z płyt i myszy do guzów pacjentów
Zespół potwierdził ten mechanizm na kilka sposobów. Zablokowanie HSPA5 powodowało szybsze znikanie białek YAP i TAZ, chyba że proteasom był chemicznie zahamowany, i zwiększało sygnały „znaczków na śmieci” (ubikwitynację) na nich. Ponowne uaktywnienie YAP i TAZ ratowało utratę wzrostu i inwazyjności obserwowaną po obniżeniu HSPA5, podczas gdy wyciszenie YAP/TAZ usuwało pro‑nowotworowe skutki nadekspresji HSPA5. W modelach mysich, gdzie ludzkie komórki glejaka wszczepiano do mózgu, guzy z wysokim HSPA5 rosły szybciej i zabijały zwierzęta wcześniej; zmniejszenie HSPA5 lub przerwanie jego wsparcia dla YAP/TAZ spowalniało wzrost i wydłużało przeżycie. Wreszcie, w sparowanych próbkach ludzkich pobranych od tych samych pacjentów przed i po nawrocie, nawrotowe, bardziej mezenchymalne guzy miały wyższe poziomy HSPA5, YAP, TAZ i markerów mezenchymalnych niż pierwotne guzy przypominające fenotyp proneuralny.
Co to oznacza dla przyszłego leczenia raka mózgu
Mówiąc prosto, praca ta sugeruje, że komórki glejaka wykorzystują pomocnika odpowiedzi na stres, HSPA5, aby osłaniać kluczowe przełączniki wzrostu (YAP i TAZ) przed degradacją. Ta ochrona pomaga guzom przejść w bardziej agresywny, odporny na leczenie stan i go utrzymać. Ponieważ istnieją już drobnocząsteczkowe inhibitory HSPA5, a komórki nowotworowe mogą być bardziej zależne od tego chaperonu niż komórki prawidłowe, oś HSPA5–YAP/TAZ stanowi obiecujący cel terapeutyczny. Terapie osłabiające tę ochronną tarczę mogłyby uczynić komórki glejaka mniej elastycznymi, mniej inwazyjnymi i bardziej podatnymi na standardowe leczenie, takie jak chemioterapia i radioterapia.
Cytowanie: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Słowa kluczowe: glejak, HSPA5, YAP/TAZ, plastyczność guza, przejście mezenchymalne