Clear Sky Science · pl
TRPA1 sprzyja postępowi zespołu nadreaktywnego pęcherza poprzez aktywację inflamasomu NLRP3 i wywoływanie pizroptozy
Dlaczego drażliwy pęcherz ma znaczenie
Potrzeba nagłego skorzystania z łazienki, wstawanie kilka razy w nocy czy obawa przed niespodziewanym przeciekiem to częste problemy zaliczane do „nadreaktywnego pęcherza”. Schorzenie to dotyka około jednej na pięć osób na świecie i może stopniowo podkopywać sen, pracę, podróże i życie towarzyskie. Tymczasem większość obecnych leków daje tylko umiarkowaną ulgę i może powodować uciążliwe skutki uboczne. W tym badaniu zbadano nowo odkryty łańcuch zdarzeń wewnątrz pęcherza, który może wyjaśniać, dlaczego staje się on tak nadwrażliwy — i wskazuje na nowe opcje leczenia wykraczające poza zwykłe rozluźnianie mięśni.
Ukryty czynnik wyzwalający w ścianie pęcherza
Głęboko w wyściółce pęcherza komórki posiadają białkowy czujnik o nazwie TRPA1, reagujący na stres fizyczny i chemiczny. Badacze analizowali komórki z moczu kobiet z nadreaktywnym pęcherzem oraz tkankę pęcherza z modeli zwierzęcych odzwierciedlających zarówno krótkotrwałą, jak i długotrwałą postać choroby. Stwierdzili, że poziomy TRPA1 były konsekwentnie wyższe w nadreaktywnym pęcherzu niż u zdrowych kontrol, a im więcej TRPA1 produkowały komórki danej osoby, tym gorsze były jej oceny objawów. U zwierząt podwyższony TRPA1 korelował z nadwrażliwym pęcherzem, który kurczył się częściej, wymagał mniejszej objętości moczu, by wywołać opróżnienie, i wykazywał obrzęk oraz zmiany strukturalne w ścianie.
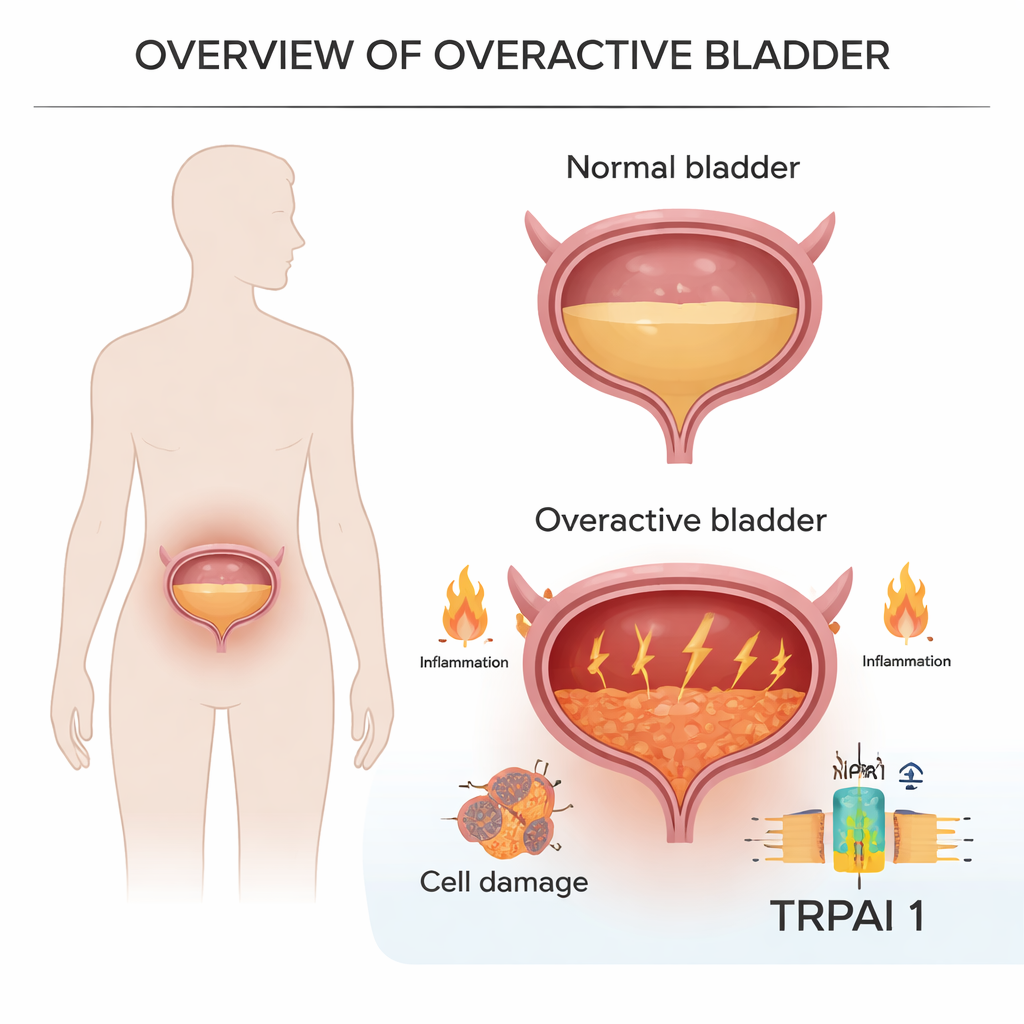
Zapalenie łączy nerwy, uszkodzenie i naglące parcie
Zespół przyjrzał się następnie, które geny są włączone w nadreaktywnym pęcherzu. Wiele z nich wiązało się z zapaleniem — chemicznym systemem alarmowym organizmu — w tym znanymi mediatorami takimi jak IL-6 i TNF. Zmiany te zaobserwowano nie tylko w ich własnych modelach mysich, lecz także w publicznych zestawach danych od pacjentów z zaburzeniami pęcherza. Zarówno u myszy, jak i szczurów z nadreaktywnym pęcherzem geny zapalne były wyraźnie podwyższone w tkance pęcherza, co sugeruje, że choroba nie jest jedynie problemem mechanicznym mięśni, lecz także zapalnym schorzeniem, w którym komórki wyściółki są zestresowane, uszkodzone i wysyłają stałe sygnały alarmowe.
Płonąca forma śmierci komórkowej
Wyraźnie wyróżniła się jedna ścieżka: molekularny mechanizm zwany inflamasomem NLRP3. Po aktywacji NLRP3 uruchamia enzym (kaspazę-1), który rozcina inne białko, Gasdermin D, do formy tworzącej otwory w błonach komórkowych. Proces ten, znany jako piroptoza, powoduje pęcznienie i rozpad komórek, uwalniając do otaczającej tkanki molekuły zapalne, takie jak IL-1β i IL-18. Badanie wykazało, że w modelach nadreaktywnego pęcherza poziomy NLRP3, aktywnej kaspazy-1 i pociętego Gasderminu D były podwyższone, zwłaszcza w wewnętrznej wyściółce pęcherza. Mówiąc prosto: zestresowane komórki pęcherza nie tylko źle funkcjonowały — umierały gwałtownie, podtrzymując cykl podrażnienia i nadaktywności.
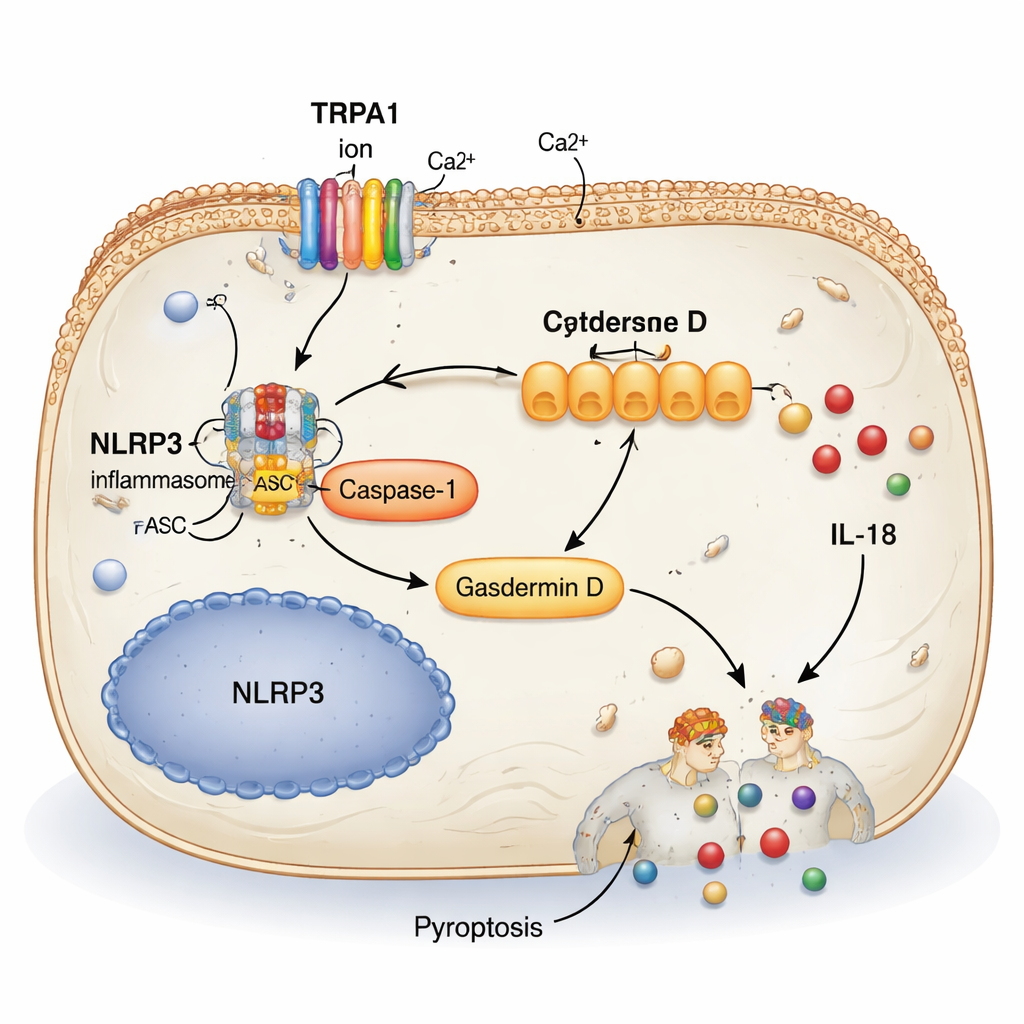
Wyłączanie reakcji łańcuchowej
Aby sprawdzić, czy TRPA1 napędza tę szkodliwą kaskadę, badacze zastosowali lek HC-030031, który blokuje kanały TRPA1. W komórkach pęcherza narażonych na działanie szkodliwego związku blokada zmniejszyła poziomy TRPA1, stłumiła geny zapalne i poprawiła przeżywalność komórek. U myszy z nadreaktywnym pęcherzem ten sam środek złagodził zapalenie, obniżył markery piroptozy i znacząco poprawił zachowanie pęcherza — mniej miejsc z moczem, dłuższe odstępy między mikcjami i lepsza elastyczność pęcherza. Gdy zespół sztucznie podniósł poziomy NLRP3 w pęcherzu, korzyści te w dużej mierze zniknęły, co dowodzi, że szkodliwe efekty TRPA1 przebiegają głównie przez szlak NLRP3–piroptoza. Odkryli też, że TRPA1 zwiększa produkcję NLRP3 współdziałając z dwoma białkami wiążącymi DNA, MAZ i SMAD3, które pomagają w włączaniu genu NLRP3.
Co to oznacza dla osób z naglącym parciem
Mówiąc krótko, badanie sugeruje, że nadreaktywny pęcherz jest częściowo napędzany przez nadwrażliwy czujnik (TRPA1) na komórkach wyściółki pęcherza, który uruchamia zapalny program śmierci komórkowej (inflamasom NLRP3 i piroptozę). To sprawia, że ściana pęcherza staje się przepuszczalna, zapalna i nadmiernie reaktywna, wysyłając sygnał „teraz” nawet przy niewielkiej objętości moczu. Blokowanie TRPA1 lub przerywanie szlaku NLRP3 może pozwolić uspokoić ten wewnętrzny system alarmowy, chronić wyściółkę pęcherza i zmniejszyć nagłość oraz częstotliwość oddawania moczu. Choć prace są wciąż na etapie eksperymentalnym, otwierają drzwi do nowej klasy terapii celujących w podstawowe obwody zapalne nadreaktywnego pęcherza, a nie tylko w skurcze mięśni.
Cytowanie: Rao, Y., Wang, Y., Gao, J. et al. TRPA1 promotes overactive bladder progression by activating the NLRP3 inflammasome and driving pyroptosis. Cell Death Dis 17, 226 (2026). https://doi.org/10.1038/s41419-026-08426-5
Słowa kluczowe: nadreaktywny pęcherz, TRPA1, zapalenie, inflamasom NLRP3, piroptoza