Clear Sky Science · pl
Hamowanie cyklu komórkowego w fazie G0/G1 przez p16 prowadzi do SASP i włóknienia w dystrofii śródbłonka rogówki typu Fuchsa
Dlaczego ta choroba oka ma znaczenie
W miarę starzenia się ludzi jednym z mniej znanych zagrożeń dla widzenia jest schorzenie zwane dystrofią śródbłonka rogówki typu Fuchsa (FECD), które stopniowo mętnieje normalnie przejrzyste przednie „okno” oka. W artykule zbadano, dlaczego niektóre komórki na wewnętrznej powierzchni rogówki z czasem się wyczerpują i bliznowacieją oraz dlaczego kobiety są dotknięte częściej. Zrozumienie tych ukrytych zmian może otworzyć drogę do leków, które opóźnią lub nawet zapobiegną konieczności przeszczepu rogówki.
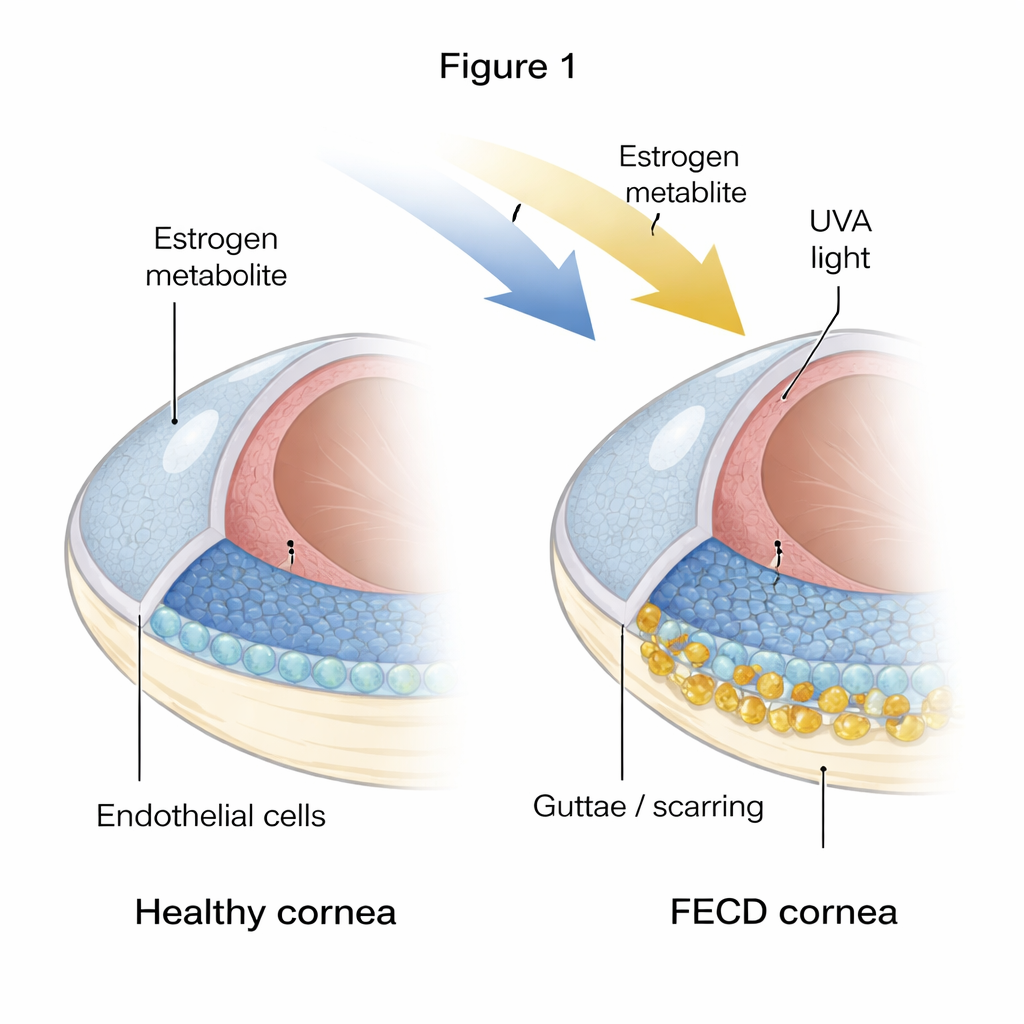
Delikatna wewnętrzna wyściółka rogówki
Rogówka musi być utrzymana w precyzyjnym stanie odwodnienia, aby zachować przejrzystość; zadanie to pełni pojedyncza warstwa heksagonalnych komórek zwanych komórkami śródbłonka rogówki. W FECD wiele z tych komórek obumiera, a warstwa staje się łata i nieregularna. Jednocześnie na wewnętrznej powierzchni pojawiają się twarde guzki i pogrubiony materiał, znane jako guttae i nadmiar macierzy zewnątrzkomórkowej. Autorzy porównali zdrowe rogówki dawców z rogówkami pacjentów z FECD i stwierdzili wyraźne oznaki, że tkanka chorobowa jest zarówno „zeszła na starość”, jak i włókniejąca: komórki wykazywały markery senescencji (trwałego zatrzymania) oraz włóknienia (zachowanie przypominające komórki tworzące blizny i odkładanie dodatkowej tkanki).
Przewlekły stres świetlny i hormonalny wypychają komórki w ślepy zaułek
Aby sprawdzić, jak zaczyna się uszkodzenie, badacze odtworzyli w laboratorium stres przypominający FECD. Eksponowali zdrowe komórki śródbłonka rogówki na światło ultrafioletowe A (UVA) oraz na 4‑hydroksyestradiol, utleniony produkt przemiany estrogenu powiązany z uszkodzeniami DNA. Krótkie, jednorazowe uderzenie stresu spowodowało tymczasowe zatrzymanie komórek w późnym etapie cyklu komórkowego i rozpoczęcie wczesnej transformacji w kierunku stanu bardziej przypominającego fibroblasty, przy zachowaniu pewnej zdolności do regeneracji. Natomiast powtarzane, przewlekłe narażenie wprowadzało komórki w inny stan: kumulowały się w wczesnym etapie cyklu zwanego G0/G1 i włączały gen p16, który z partnerem białkowym pRB blokuje cykl komórkowy. Te komórki stawały się duże, spłaszczone i wyraźnie senescentne, a jednocześnie silnie ekspresjonowały markery włóknienia i białka tworzące pogrubione guttae w FECD.
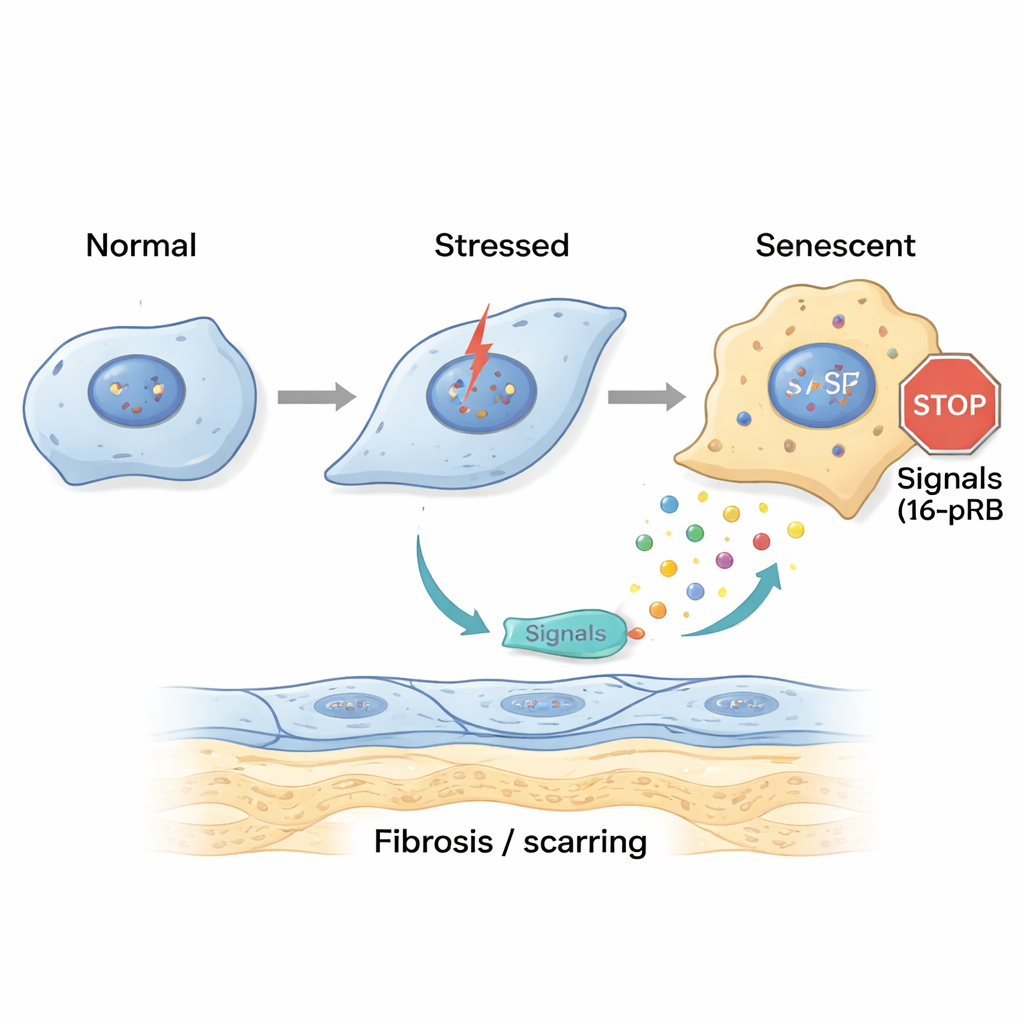
Komórki senescentne wysyłają szkodliwe sygnały i rozsiewają bliznowacenie
Komórki senescentne nie siedzą cicho; wydzielają mieszaninę cząsteczek sygnalizacyjnych znaną jako fenotyp wydzielniczy związany z senescencją (SASP). Zespół zebrał płyn z zestresowanych komórek rogówki i zastosował go na świeże komórki oraz na zdrowe rogówki dawców. „Ostry” SASP powodował wczesne zmiany kształtu komórek, podczas gdy „przewlekły” SASP popychał wiele komórek w stan senescencji i zwiększał ekspresję genów związanych z włóknieniem oraz odkładaniem dodatkowej macierzy. Szczegółowe badania wykazały, że przewlekły SASP był bogaty w prozapalne mediatory takie jak IL‑8 i IL‑17, które są znane z promowania starzenia komórek, bliznowacenia i rekrutacji komórek układu odpornościowego. Gdy badacze zablokowali szlak IL‑17 lub receptor IL‑8 CXCR2, komórki eksponowane na przewlekły SASP wykazywały mniej markerów senescencji i mniejsze włóknienie, co sugeruje, że te sygnały są kluczowymi napędami choroby.
Usuwanie zużytych komórek dla ochrony wzroku
Ponieważ komórki p16‑dodatnie były ściśle związane z bliznowaceniem, autorzy sprawdzili, czy ich eliminacja może chronić rogówkę. W modelu myszy, w którym światło UVA wywołuje zmiany przypominające FECD, leczono zwierzęta kombinacją leku senolitycznego, dasatinibu i kwercetyny, która selektywnie zabija komórki senescentne. W porównaniu z myszami bez leczenia, myszy leczone senolitykami zachowały bardziej regularny mozaikowy układ komórek śródbłonka, zachowały więcej komórek ogółem i wykazywały mniej markerów senescencji, włóknienia i nadmiaru macierzy. Innymi słowy, oczyszczenie najbardziej uszkodzonych komórek zmniejszyło obciążenie szkodliwych wydzielin i pomogło utrzymać zdrowszą powierzchnię rogówki.
Co to oznacza dla osób z FECD
Dla pacjentów FECD często kończy się przeszczepem rogówki, gdy widzenie staje się zbyt zamglone. Badanie sugeruje inną ścieżkę: choroba może być napędzana przez powolne gromadzenie się zestresowanych, nie dzielących się komórek, które zarówno nie wykonują swojej pracy, jak i aktywnie zatruwają sąsiedztwo sygnałami zapalnymi i fibroticznymi. Celowanie w te sygnały lekami przeciw szlakom IL‑17 lub IL‑8, albo użycie terapii senolitycznych do selektywnego usunięcia najbardziej uszkodzonych komórek, mogłoby pewnego dnia opóźnić bliznowacenie, zachować więcej naturalnej tkanki oka i odroczyć lub zmniejszyć potrzebę operacji.
Cytowanie: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Słowa kluczowe: dystrofia Fuchsa, śródbłonek rogówki, senescencja komórkowa, włóknienie, terapia senolityczna