Clear Sky Science · pl
DNA mitochondrialne aktywuje oś NLRP3-IL-1β w mikrogleju poprzez wiązanie z NLRP3, prowadząc do neurodegeneracji w modelach choroby Parkinsona
Dlaczego to ma znaczenie dla choroby Parkinsona
Choroba Parkinsona jest najbardziej znana z drżeń i spowolnionych ruchów, ale pod tymi objawami toczy się złożona walka w wnętrzu mózgu. Badanie to ujawnia, jak drobne fragmenty materiału genetycznego pochodzące z uszkodzonych mitochondriów w komórkach odpornościowych mózgu mogą zapoczątkować stan zapalny, który stopniowo zabija neurony produkujące dopaminę niezbędne do płynnych ruchów. Zrozumienie tego łańcucha zdarzeń otwiera nowe, bardzo konkretne cele dla leków, które mogłyby spowolnić lub zapobiec uszkodzeniom przypominającym Parkinsona.
Komórki odpornościowe mózgu i elektrownie pod stresem
Mózg zawiera nie tylko neurony, ale także mikroglej — jego rezydujące komórki odpornościowe. W chorobie Parkinsona mikroglej często ulega nadmiernej aktywacji, uwalniając toksyczne cząsteczki i sygnały zapalne, które szkodzą pobliskim neuronom. Autorzy skupili się na mitochondriach, „elektrowniach” komórek, które mają własne DNA. Gdy mitochondria są uszkadzane — przez toksyny, starzenie lub inne stresy — ich DNA może ulegać oksydacji, rodzajowi uszkodzenia chemicznego wywołanego przez reaktywne formy tlenu. Ponieważ DNA mitochondrialne przypomina DNA bakteryjne, te uszkodzone fragmenty mogą działać jak sygnały alarmowe w mózgu, aktywując układ odpornościowy i potencjalnie napędzając przewlekłe zapalenie.
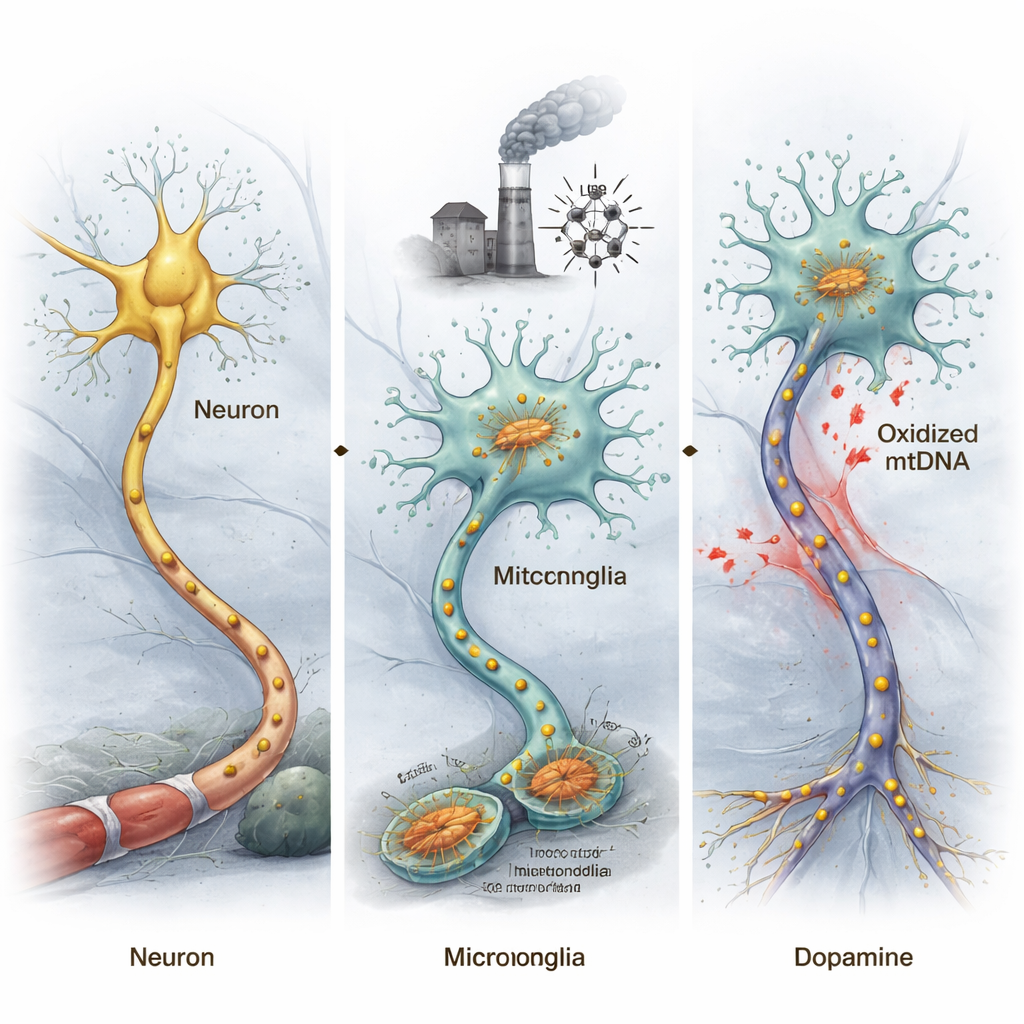
Uszkodzone DNA mitochondrialne może popychać myszy w stronę choroby podobnej do Parkinsona
Aby sprawdzić, czy oksydowane DNA mitochondrialne (ox-mtDNA) może faktycznie wywołać zmiany przypominające Parkinsona, badacze wyizolowali ox-mtDNA z zestresowanych komórek mikrogleju i wstrzyknęli go bezpośrednio do regionu mózgu, który normalnie zawiera neurony produkujące dopaminę ważne dla ruchu. Myszy poddane działaniu tego ox-mtDNA wykazywały zmniejszoną aktywność ruchową w testach behawioralnych oraz utratę tych neuronów dopaminowych, odzwierciedlając kluczowe cechy choroby Parkinsona. Sortując neurony i mikroglej z śródmózgowia i analizując ich aktywność genową, zespół stwierdził, że geny powiązane z chorobą Parkinsona stały się bardziej zaburzone w neuronach, podczas gdy geny związane z zapaleniem były silnie aktywowane w mikrogleju.
Molekularny przełącznik alarmowy w mikrogleju
Badanie skoncentrowało się na kompleksie białkowym w mikrogleju zwanym NLRP3, będącym częścią większego zespołu znanego jako inflammasom. Po jego uruchomieniu NLRP3 pomaga aktywować kaspazę-1, enzym tnący cząsteczkę zapalną IL-1β do jej aktywnej, szkodliwej postaci. Zarówno u myszy, jak i w hodowlach komórkowych, połączenie sygnału przygotowującego zapalenie (LPS, składnik bakteryjny) i toksyny podobnej do pestycydu — rotenonu — spowodowało, że mitochondria w mikrogleju uwalniały oksydowane mtDNA do płynu komórkowego. To uwolnienie zbiegło się z silniejszą aktywacją NLRP3, większą ilością aktywowanej (pociętej) kaspazy-1 i wyższymi poziomami IL-1β. Medium pobrane z tych nadaktywowanych mikroglejów było bezpośrednio toksyczne dla neuronów podobnych do dopaminowych hodowanych na szalce, obniżając ich przeżywalność i poziom ich kluczowego markera, hydroksylazy tyrozynowej.
Bezpośrednie wiązanie: jak oksydowane DNA przełącza NLRP3
Ponad prostą korelacją, autorzy wykazali, że ox-mtDNA nie tylko występuje podczas zapalenia — wydaje się fizycznie wiązać z NLRP3 i go uruchamiać. Gdy zablokowali uwalnianie DNA mitochondrialnego za pomocą leku, aktywacja kaspazy-1 i IL-1β spadła. Odwrotnie, bezpośrednie dostarczenie oksydowanego mtDNA do mikrogleju silnie zwiększyło sygnalizację NLRP3, bardziej niż nieoksydowane mtDNA. W eksperymentach biochemicznych typu pull-down wykryto mtDNA, bogate w markery uszkodzeń oksydacyjnych, związane z NLRP3. Modelowanie komputerowe i chemia białek ujawniły, że ox-mtDNA wiąże dodatnio naładowany, elastyczny fragment NLRP3 (tzw. „wewnętrznie nieuporządkowany region”) obejmujący aminokwasy 180–187. Gdy usunięto ten krytyczny odcinek z NLRP3, jego zdolność do wiązania ox-mtDNA i aktywowania kaspazy-1 była znacznie osłabiona.
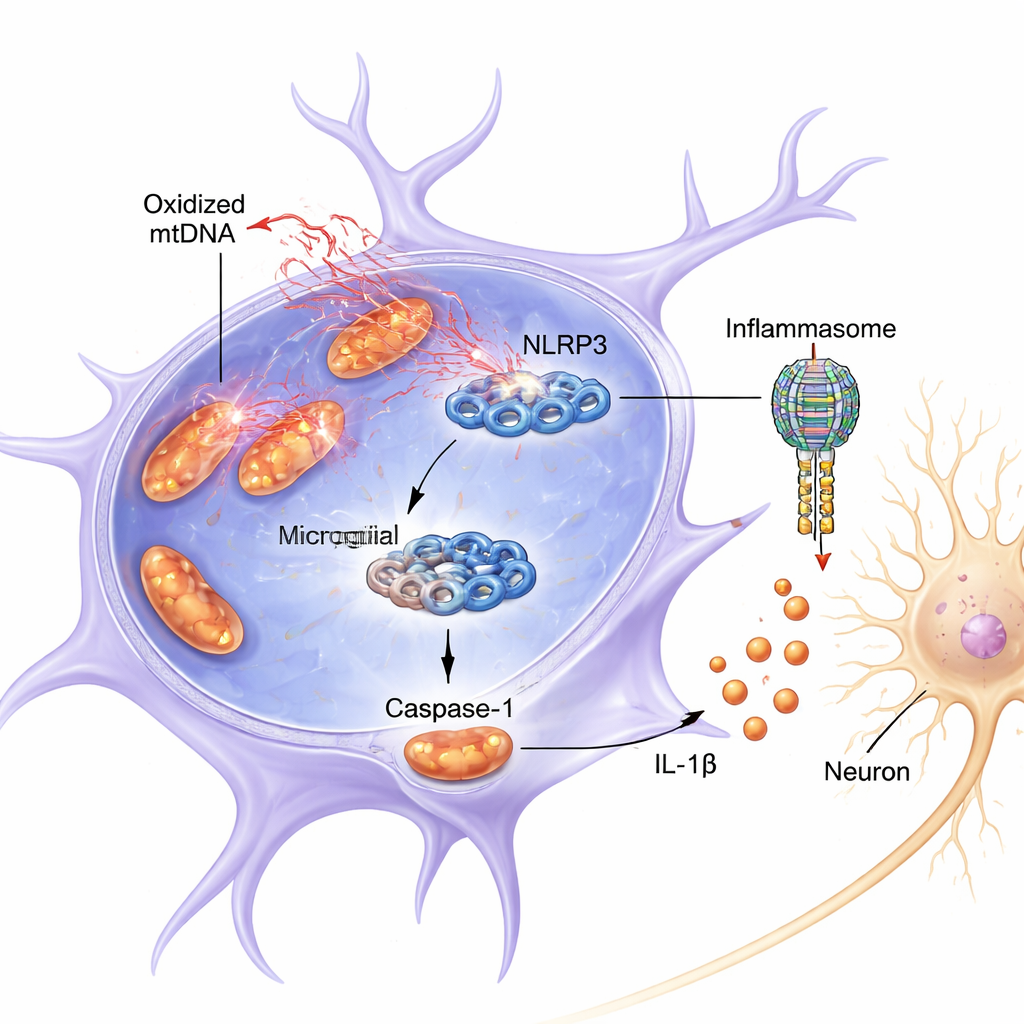
Wyłączenie inflammasomu oszczędza neurony
Następnie badacze zapytali, czy zakłócenie działania NLRP3 może chronić neurony. W hodowanych mikroglejach genetyczne obniżenie poziomu NLRP3 znacznie zmniejszyło aktywację kaspazy-1 i IL-1β po leczeniu LPS i rotenonem, a medium warunkowane od tych komórek było znacznie mniej toksyczne dla neuronów podobnych do dopaminowych. U myszy selektywny inhibitor NLRP3 (MCC950) zmniejszył aktywację mikrogleju, zachował neurony dopaminowe i obniżył poziomy białek związanych z inflammasomem w modelach wywołanych LPS plus rotenon lub przez wstrzyknięte mtDNA. Razem te eksperymenty pokazują, że łańcuch ox-mtDNA–NLRP3–IL-1β nie jest tylko powiązaniem z uszkodzeniem; jest wymagany dla dużej części obserwowanej utraty neuronów.
Co to oznacza dla przyszłych terapii choroby Parkinsona
Dla osób niezajmujących się na co dzień tym zagadnieniem kluczowy przekaz jest taki: uszkodzone DNA mitochondrialne wydostające się z komórek odpornościowych mózgu może bezpośrednio przyczepiać się do wewnętrznego „przełącznika alarmowego” (NLRP3), wywołując falę zapalenia, która uszkadza neurony dopaminowe i powoduje w modelach chorobę podobną do Parkinsona. Ponieważ ta interakcja zależy od krótkiego, zdefiniowanego fragmentu białka NLRP3 oraz od oksydowanego charakteru mitochondrialnego DNA, oferuje precyzyjne nowe cele terapeutyczne. Terapie zapobiegające uszkodzeniu lub ucieczce DNA mitochondrialnego, blokujące jego wiązanie z NLRP3 lub hamujące sam NLRP3 mogłyby w praktyce stłumić tę kaskadę zapalną i spowolnić postęp choroby Parkinsona.
Cytowanie: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Słowa kluczowe: choroba Parkinsona, mikroglej, DNA mitochondrialne, inflammasom NLRP3, neurozapalanie