Clear Sky Science · pl
Niedobór SLC46A1 powodujący ograniczenie kwasu foliowego hamuje rozwój raka jelita grubego poprzez epigenetyczno-transkrypcyjne przeprogramowanie
Dlaczego witamina B9 i nowotwory jelita tworzą zaskakującą parę
Wiele osób zna folian, czyli witaminę B9, jako składnik odżywczy ważny w ciąży i dla zdrowia serca. To badanie pokazuje, że folian odgrywa też zaskakującą rolę w raku okrężnicy i odbytnicy. Zwrot akcji polega na tym, że korzystny efekt folianu zależy od obecności jednego białkowego strażnika na komórkach nowotworowych, zwanego SLC46A1, który decyduje, ile folianu trafia faktycznie do wnętrza komórek guza. Zrozumienie tej ukrytej bramy może pomóc wyjaśnić, dlaczego wcześniejsze badania nad folianem i rakiem były tak sprzeczne, i może ukierunkować bezpieczniejsze stosowanie folianu w diecie i terapii.
Brama odżywcza w jelicie
Komórki naszego jelita nie potrafią samodzielnie syntetyzować folianu; muszą pobierać go z otoczenia za pomocą specjalnych białek transportowych. Autorzy wykazali, że SLC46A1 jest głównym transporterem folianu w ludzkim okrężnicy, znacznie bardziej aktywnym niż inne znane nośniki. Analiza dużych publicznych zbiorów danych nowotworowych i próbek tkankowych od pacjentów wykazała, że poziomy SLC46A1 są wyraźnie obniżone w guzach jelita grubego w porównaniu z pobliską zdrową tkanką. Guzy z niższym poziomem SLC46A1 miały tendencję do bycia bardziej zaawansowanymi, częściej się przenosiły i były związane z gorszym przeżyciem pacjentów, co sugeruje, że ten transporter zachowuje się bardziej jak hamulec niż akcelerator w tym nowotworze.
Jak utrata bramy zmienia zachowanie nowotworu
Aby sprawdzić, co SLC46A1 faktycznie robi, badacze regulowali jego poziomy w liniach komórkowych raka jelita grubego. Gdy obniżali SLC46A1, komórki nowotworowe rosły szybciej, łatwiej się przemieszczały i inwazyjnie przechodziły przez sztuczne bariery w laboratorium. Gdy zwiększali SLC46A1 w komórkach, które zaczynały od niskich poziomów, komórki stawały się mniej inwazyjne. Podobne wzorce obserwowano u myszy: guzy wyrosłe z komórek pozbawionych SLC46A1 były większe i dawały więcej przerzutów do płuc. Równocześnie guzy i hodowle komórkowe z mniejszą ilością SLC46A1 zawierały mniej folianu wewnątrz, potwierdzając, że to białko rzeczywiście pełni rolę kluczowego punktu wejścia dla tej witaminy.
Od niedoboru witaminy do zaburzonej kontroli genów
Folian robi więcej niż pomaga w syntezie bloków budulcowych DNA; zasila też chemiczny system nakładający drobne metylowe „znaczki” na DNA, które pomagają wyłączać lub włączać geny. Zespół wykazał, że gdy SLC46A1 zostaje utracony i wewnątrzkomórkowy poziom folianu spada, ogólna zdolność do umieszczania tych znaczników maleje. To z kolei selektywnie usuwa metylację z regionu kontrolnego genu nazwanego FOS, dobrze znanego regulatora wzrostu komórek. Bez tych znaczków FOS się włącza i aktywuje kilka genów „wspierających wzrost i rozprzestrzenianie”, w tym CCND1, BCL2 i PLAU, które pomagają komórkom nowotworowym dzielić się, unikać śmierci i przenikać przez otaczające tkanki. Zablokowanie FOS lub PLAU w dużej mierze likwidowało dodatkowy wzrost i inwazyjność wywołane utratą SLC46A1, łącząc te zdarzenia w jedną ścieżkę.
Gdy folian pomaga tylko jeśli drzwi są otwarte
Badanie wyjaśnia też, kiedy sam folian jest korzystny, a kiedy nie dla guzów. W hodowlach komórkowych prowadzonych w warunkach ubogich w folian, ponowne dodanie folianu na poziomach zbliżonych do występujących we krwi człowieka spowalniało wzrost i ruch komórek nowotworowych — ale tylko wtedy, gdy SLC46A1 był obecny i mógł wprowadzić folian do wnętrza. W guzach mysich bezpośrednie wstrzyknięcia folianu do masy guza zmniejszały wzrost i oznaki podziału komórek, ponownie tylko gdy komórki nowotworowe nadal wytwarzały SLC46A1. Guzy pozbawione transportera reagowały w minimalnym stopniu. W próbkach od pacjentów badacze zaobserwowali wzorzec odwrotny: guzy z wysokim SLC46A1 miały niższy poziom folianu w płynie otaczającym, jakby efektywnie go wychwytywały, i wykazywały niższe poziomy FOS i PLAU. Guzy z niskim SLC46A1 pozostawiały więcej folianu niewykorzystanego i miały wyższe poziomy tych agresywnych markerów.
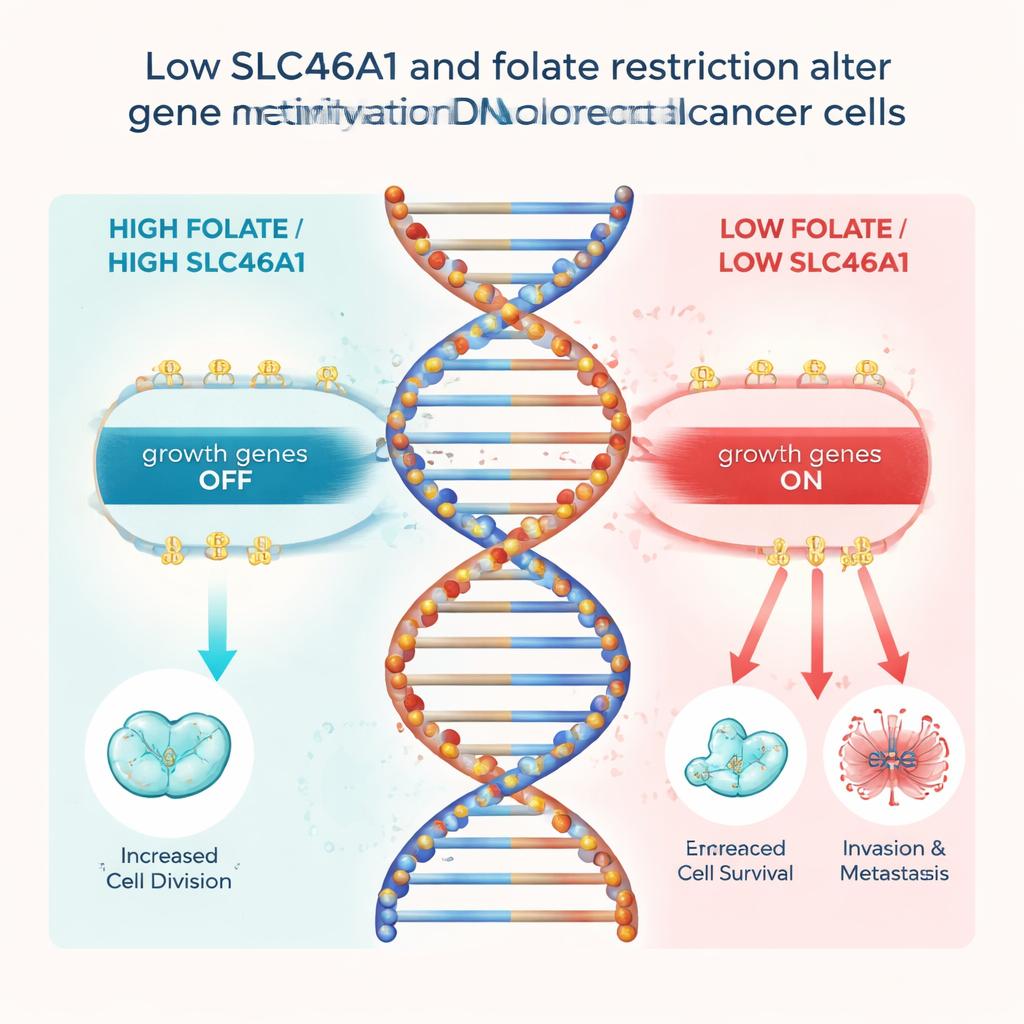
Co to oznacza dla pacjentów i profilaktyki
Dla laika główny przekaz jest taki, że wpływ folianu na raka jelita grubego zależy od tego, czy komórki guza nadal wyrażają „drzwi” SLC46A1, które wpuszczają folian do środka. Gdy drzwi są obecne, realistyczne ilości folianu mogą wspierać prawidłowe znakowanie DNA i pomagać utrzymać geny napędzające wzrost pod kontrolą. Gdy drzwi znikają, guz nie może wykorzystać folianu w ten ochronny sposób i zamiast tego przesuwa się ku bardziej agresywnemu stanowi napędzanemu przez uwolnione geny, takie jak FOS. Praca ta sugeruje, że w przyszłości badanie poziomów SLC46A1 w nowotworach jelita grubego mogłoby pomóc lekarzom przewidzieć rokowanie i zdecydować, czy diety lub terapie związane z folianem mogą być pomocne, stanowiąc krok w kierunku bardziej spersonalizowanej, świadomej pod względem składników odżywczych opieki onkologicznej.
Cytowanie: Zhou, Y., Liu, Y., Liu, Y. et al. SLC46A1 deficiency-mediated folate restriction suppresses colorectal cancer progression through epigenetic-transcriptional reprogramming. Cell Death Dis 17, 189 (2026). https://doi.org/10.1038/s41419-026-08423-8
Słowa kluczowe: kwas foliowy, rak jelita grubego, epigenetyka, SLC46A1, metylacja DNA