Clear Sky Science · pl
Laktylacja SLC26A3 w kwaśnym mikrośrodowisku guza sprzyja złośliwemu postępowi raka jelita grubego
Dlaczego kwaśność guza ma znaczenie
Rak jelita grubego pozostaje jednym z najgroźniejszych nowotworów na świecie, częściowo dlatego, że guzy często nawracają, dają przerzuty lub przestają reagować na leki. W tym badaniu zbadano mniej docenianego sprawcę takiego zachowania: kwaśne, bogate w kwas mlekowy środowisko wewnątrz guza. Odkrywając, jak to surowe otoczenie destabilizuje ochronny białkowy transporter błonowy SLC26A3, autorzy ukazują nowy łańcuch zdarzeń, który sprzyja przekształceniu komórek nowotworowych w bardziej przypominające komórki macierzyste, inwazyjne i oporne na leki — co daje nowe pomysły terapeutyczne.
Surowe sąsiedztwo wokół komórek nowotworowych
Szybko rosnące guzy zużywają duże ilości cukru i tlenu, uwalniając kwas mlekowy i jony wodorowe, które zakwaszają ich otoczenie. Wykorzystując obszerne zbiory danych pacjentów i próbki tkankowe, badacze pokazują, że ten kwaśny stan, śledzony przy pomocy markera CA9, idzie w parze z agresywnymi rakami jelita grubego. W bardziej zaawansowanych nowotworach poziomy CA9 są wysokie, podczas gdy poziomy SLC26A3 są konsekwentnie niskie. SLC26A3 zwykle znajduje się na powierzchni komórek jelita i pomaga wyrównywać jony soli oraz wodorowęglany, co z kolei pomaga kontrolować kwasowość. W próbkach guzów, liniach komórkowych i analizach pojedynczych komórek zespół stwierdza, że wzrost kwasowości prowadzi do spadku poziomów SLC26A3 — szczególnie w złośliwych, przypominających komórki macierzyste komórkach nowotworowych. 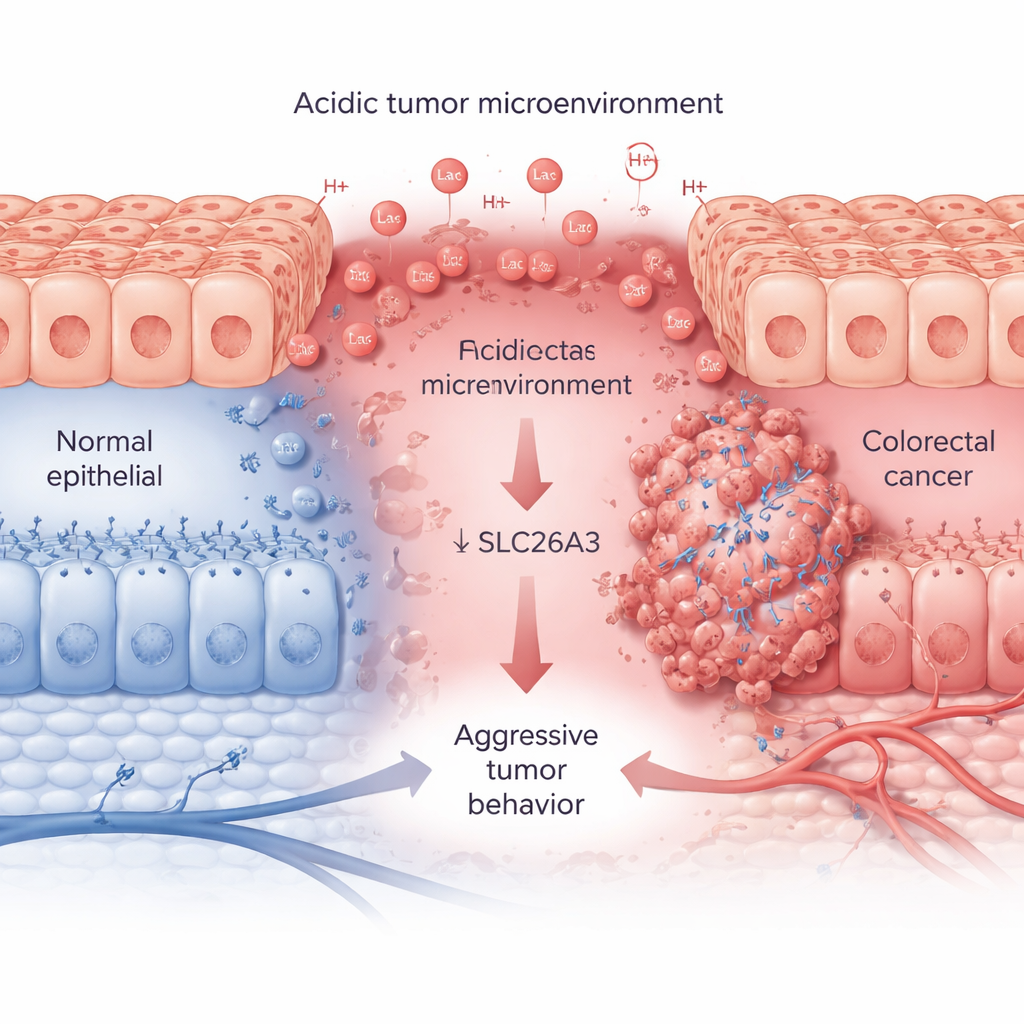
Jak kwas mlekowy oznacza cel do zniszczenia
Następnie autorzy zastanawiają się, dlaczego SLC26A3 spada w kwaśnych guzach. Koncentrują się na laktylacji, niedawno odkrytym chemicznym znaczniku powstającym z kwasu mlekowego, który może być dodawany do białek. Gdy komórki raka jelita grubego są wystawione na działanie kwasu mlekowego lub hodowane w kwaśnych warunkach, SLC26A3 ulega silnej laktylacji. Szczegółowa analiza białka wskazuje jedno kluczowe miejsce — resztę aminokwasową K536 — gdzie jest dodawany ten znacznik. Laktylacja w pozycji K536 czyni SLC26A3 mniej stabilnym: białko jest częściej znakowane ubikwityną, komórkowym sygnałem „usuń to”, i kierowane do mechanizmów recyklingu komórkowego. Blokowanie enzymu p300, który pomaga dodawać oznaczenia laktylacji, częściowo chroni SLC26A3 przed rozpadem. W efekcie kwasowość i laktoza tworzą szkodliwe sprzężenie zwrotne — więcej laktozy prowadzi do większej laktylacji, co zmniejsza SLC26A3, dalej zaburzając równowagę pH i sprzyjając jeszcze bardziej kwaśnemu mikrośrodowisku.
Wyłączenie hamulca na rzecz „stemness” i rozprzestrzeniania się
Przy wyczerpaniu SLC26A3 komórki nowotworowe zachowują się bardziej agresywnie. W hodowlach komórkowych komórki raka jelita grubego przypominające komórki macierzyste naturalnie wykazują mniej SLC26A3 niż ich nie‑stemowe odpowiedniki. Gdy badacze celowo obniżają poziomy SLC26A3, komórki guza tworzą więcej sfer (cecha stemness), efektywniej się odnawiają, inwazują przez sztuczne membrany i szybciej przemieszczają się w testach „scratch”. Stają się także mniej wrażliwe na powszechne leki chemioterapeutyczne, takie jak oksaliplatyna i 5‑fluorouracyl. Odwrotnie, zwiększenie ekspresji SLC26A3 zmniejsza markery stemness i spowalnia inwazję oraz migrację — ale korzyść ta jest osłabiona przy dodatku dodatkowej laktozy, co podkreśla, jak kwaśność może zniwelować efekt ochronny.
Ukryte powiązanie z kontrolą genów
Poza pomocą w regulacji kwasowości, SLC26A3 działa także jako rusztowanie wiążące dwa białka wiążące RNA, HuR i CUGBP1. Białka te kontrolują żywotność wielu mRNA kodujących białka istotne dla nowotworu. Gdy SLC26A3 jest obfity, sekwestruje część HuR i CUGBP1, ograniczając ich zdolność do stabilizowania lub destabilizowania określonych nowotworowych komunikatów. Gdy SLC26A3 zostaje utracony wskutek laktylacji i degradacji, HuR i CUGBP1 mają większą swobodę wiązania onkogennych mRNA, które promują stemness, przejście epiteliomięśniowe (EMT), inwazję i przeżycie. Eksperymenty pokazują, że HuR pomaga stabilizować mRNA markerów stemness i białek połączeń komórkowych, podczas gdy CUGBP1 może przeciwdziałać HuR dla niektórych celów, osłabiając integralność połączeń i sprzyjając EMT — oba zjawiska ułatwiają rozprzestrzenianie się guza.
Przywrócenie równowagi środowiska w walce z rakiem
Aby sprawdzić, czy te wnioski można przełożyć na strategię leczenia, badacze zastosowali modele mysie raka jelita grubego. Neutralizowanie kwaśności guza za pomocą wodorowęglanu sodu, blokowanie transportu laktatu inhibitorem MCT1 lub nadekspresja SLC26A3 wszystkie spowalniały wzrost guza. Połączenie przywrócenia SLC26A3 z chemioterapią dodatkowo zmniejszało guzy. W danych pacjentów wyższe poziomy SLC26A3 korelują z lepszym przeżyciem, mniejszą częstością nawrotów, mniejszą liczbą przerzutów i lepszą odpowiedzią na chemioterapię, co sugeruje, że to białko może służyć zarówno jako biomarker, jak i cel terapeutyczny. 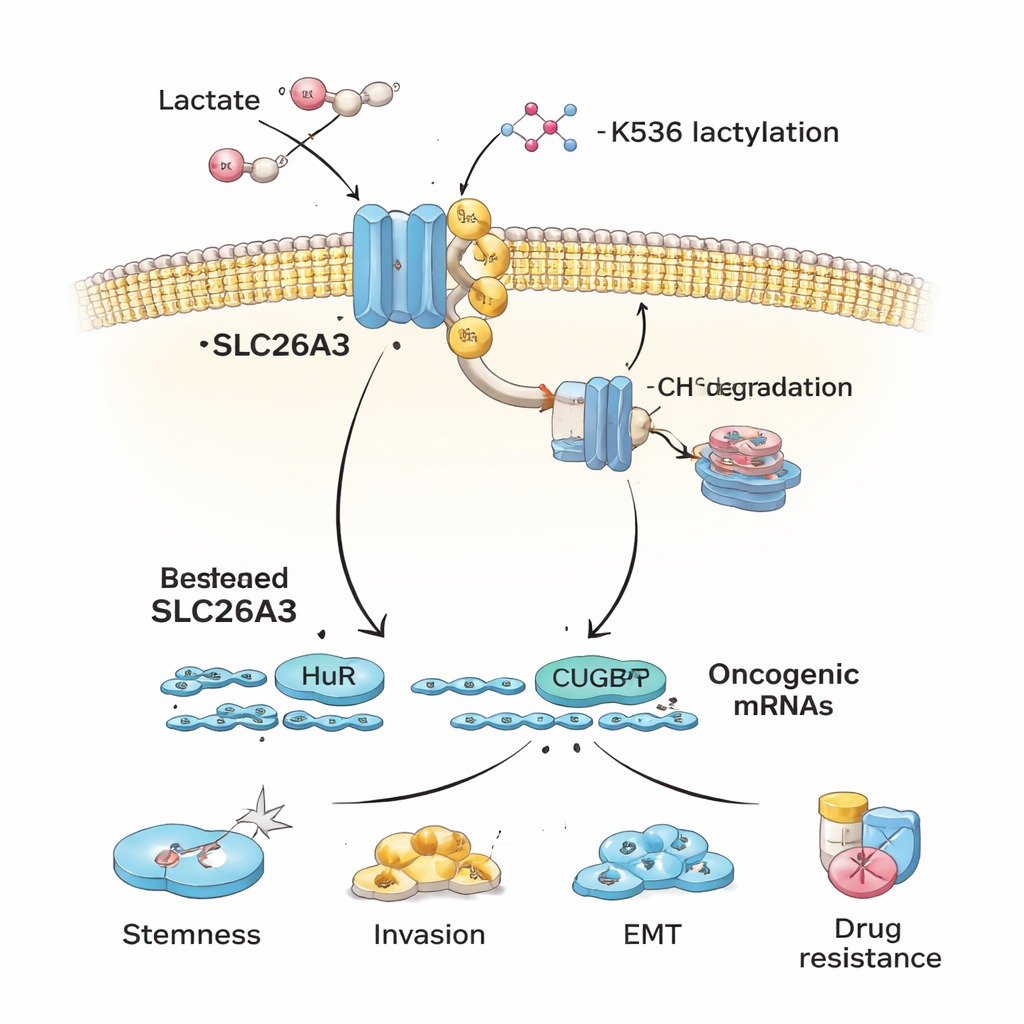
Co to oznacza dla pacjentów
Mówiąc prościej, to badanie pokazuje, że guzy jelita grubego rozwijają się w kwaśnej, bogatej w kwas mlekowy kąpieli, która chemicznie „oznacza” i niszczy ochronnego strażnika — SLC26A3. Gdy strażnik znika, komórki nowotworowe łatwiej przyjmują cechy podobne do komórek macierzystych, rozprzestrzeniają się i stają się oporne na leczenie, wspierane przez silne regulatory RNA wewnątrz komórki. Poprzez buforowanie kwaśności guza, blokowanie przetwarzania laktatu lub przywrócenie SLC26A3 możliwe jest osłabienie tego złośliwego sprzężenia zwrotnego i zwiększenie skuteczności standardowych terapii. Chociaż takie podejścia wymagają wciąż rygorystycznych badań klinicznych, otwierają obiecujący nowy kierunek pokazujący, jak zarządzanie chemicznym otoczeniem guza może pomóc w kontroli raka jelita grubego.
Cytowanie: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Słowa kluczowe: rak jelita grubego, mikrośrodowisko guza, laktylacja, komórki macierzyste nowotworu, oporność na chemioterapię