Clear Sky Science · pl
Celowanie w GNG4 hamuje progresję guza i przywraca wrażliwość na enzalutamid w raku prostaty przez tłumienie autofagii
Dlaczego to badanie ma znaczenie
Dla wielu mężczyzn z zaawansowanym rakiem prostaty silne leki blokujące hormony, takie jak enzalutamid, początkowo działają dobrze, ale z czasem tracą skuteczność. To badanie ujawnia ukryty mechanizm przetrwania wykorzystywany przez komórki nowotworowe i wskazuje konkretny białkowy przełącznik, GNG4, który pomaga nowotworom rosnąć i opierać się terapii. Zrozumienie tego mechanizmu może doprowadzić do terapii skojarzonych, które sprawią, że obecne leki będą działały lepiej i dłużej.
Przełącznik białkowy widoczny gołym okiem
Komórki raka prostaty są silnie napędzane przez hormony męskie, dlatego standardowe leczenie zaawansowanej choroby odcina te sygnały. Jednak większość guzów ostatecznie staje się „oporna na kastrację” i zaczyna znowu rosnąć. Autorzy poszukiwali genów znacznie bardziej aktywnych w tkance nowotworowej niż w sąsiedniej tkance gruczołu krokowego od tych samych pacjentów. Spośród kilku kandydatów wyróżnił się GNG4: gdy obniżono jego poziom w komórkach raka prostaty, wzrost komórek nowotworowych gwałtownie spadł. Analizy setek próbek od pacjentów potwierdziły, że GNG4 jest wyższy w pierwotnych rakach prostaty niż w tkance prawidłowej i jest szczególnie podwyższony w bardziej agresywnych, wysokogatunkowych nowotworach.
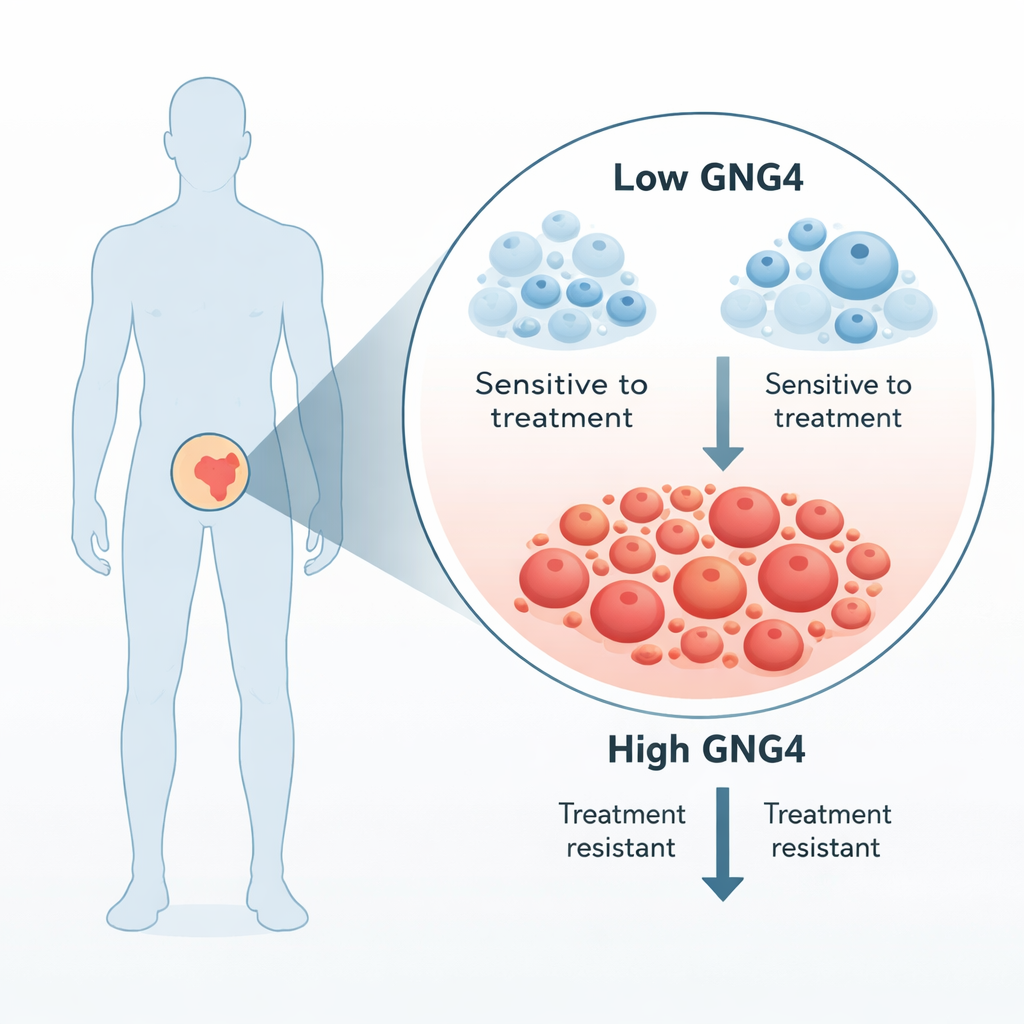
Jak GNG4 pomaga guzom przetrwać
GNG4 jest częścią większej rodziny białek sygnałowych znanych jako białka G, które znajdują się w błonie komórkowej i przekazują sygnały ze środowiska zewnętrznego do wnętrza komórki. Zespół pokazał, że zmniejszenie ekspresji GNG4 w liniach komórkowych raka prostaty spowalniało podziały komórkowe, powodowało zatrzymanie komórek w fazie kontrolnej cyklu komórkowego i zwiększało programowaną śmierć komórek. Zmiany te ograniczały również zdolność komórek nowotworowych do migracji i zamykania „ran” w testach laboratoryjnych, a guzy powstałe z komórek pozbawionych GNG4 rosły wolniej u myszy. Razem wyniki sugerują, że GNG4 działa jak pedał gazu napędzający wzrost i rozsiew raka prostaty.
Autofagia: awaryjna spiżarnia komórki nowotworowej
Następnie badacze skupili się na procesie zwanym autofagią, w którym komórki rozkładają i recyklingują własne składniki, by przetrwać stres, taki jak głodzenie czy leczenie lekami. W wielu zaawansowanych nowotworach autofagia służy jako awaryjna spiżarnia, która pomaga komórkom nowotworowym radzić sobie w trudnych warunkach. W tym badaniu komórki raka prostaty z wysoką aktywnością GNG4 wykazywały więcej oznak aktywnej autofagii, podczas gdy komórki z obniżonym GNG4 miały mniej struktur recyklingowych i niższe poziomy kluczowych markerów autofagii. Przy nadprodukcji GNG4 komórki lepiej tolerowały enzalutamid i przechodziły mniej śmierci komórkowej. Zablokowanie autofagii chemicznym inhibitorem zniwelowało dużą część tej ochrony, co wskazuje, że GNG4 pomaga nowotworom przetrwać leczenie głównie przez nasilanie tego systemu recyklingu.
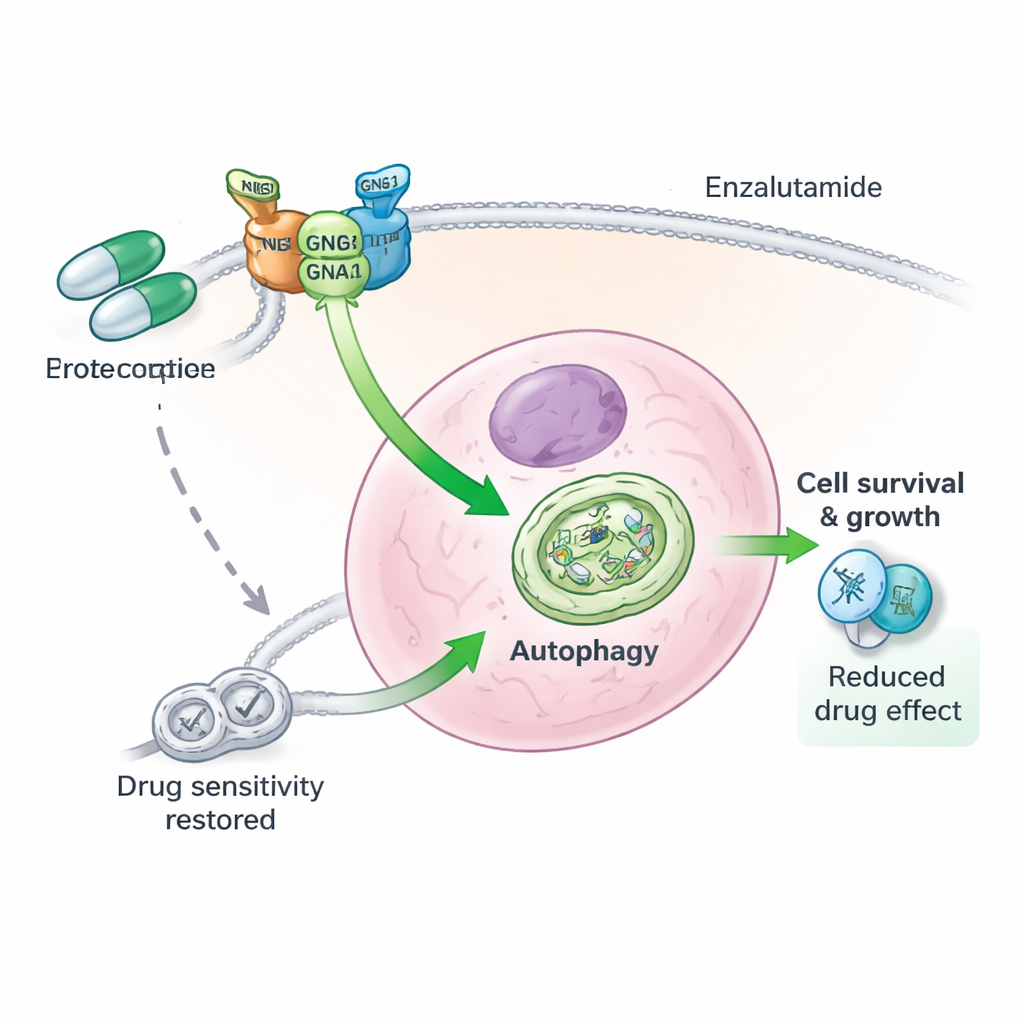
Trio białkowe stojące za opornością na leki
Głębiej poszukując, autorzy odkryli, że GNG4 nie działa samotnie. Fizycznie łączy się z innym podjednostkowym białkiem G, GNB1, aby stabilizować trzecie białko, GNAI3. Razem te trzy podjednostki tworzą funkcjonalny kompleks, który wzmacnia autofagię wewnątrz komórek raka prostaty. Gdy GNG4 było zmniejszone, białko GNAI3 było szybciej zaznaczane do zniszczenia i rozkładane przez mechanizmy komórkowego „utylizatora”, co wyłączało sygnał autofagii. Usunięcie samego GNAI3 niwelowało korzyści wzrostu i przetrwania nadane przez dodatkowe GNG4, zarówno w hodowlach komórkowych, jak i w guzach u myszy. Innymi słowy, GNG4 napędza złośliwość i odporność na stres w dużej mierze poprzez oś GNG4–GNB1–GNAI3.
Uczynienie obecnych leków bardziej skutecznymi
Na koniec zespół sprawdził, co się dzieje, gdy celowanie w GNG4 połączy się z enzalutamidem, wiodącym lekiem w zaawansowanym raku prostaty. W laboratorium redukcja GNG4 sprawiła, że komórki nowotworowe stały się znacząco bardziej wrażliwe na enzalutamid i zmniejszyła ich zdolność do tworzenia kolonii po leczeniu. U myszy guzy o obniżonym poziomie GNG4 bardziej się kurczyły po podaniu enzalutamidu niż guzy z normalnym poziomem GNG4, bez widocznego wzrostu toksyczności. Bezpośrednie blokowanie autofagii dało podobne ulepszenia. Wyniki te sugerują, że zakłócenie autofagii napędzanej przez GNG4 może pozbawić komórki nowotworowe istotnego mechanizmu radzenia sobie, pozwalając istniejącym terapiom blokującym hormony zadać silniejszy i trwalszy cios.
Co to oznacza dla pacjentów
Dla osoby niebędącej specjalistą kluczowe przesłanie brzmi: niektóre raki prostaty przetrwają leczenie, włączając wewnętrzny system recyklingu, który działa jak zapasowy generator. To badanie identyfikuje GNG4 jako główny przełącznik uruchamiający ten system, współdziałający z białkowymi partnerami, by chronić komórki nowotworowe przed enzalutamidem. Wyłączenie tego przełącznika — poprzez bezpośrednie celowanie w GNG4 lub bezpieczne stłumienie autofagii — może w przyszłości umożliwić spowolnienie wzrostu guza i przywrócenie wrażliwości na leki u mężczyzn, których nowotwory stały się trudne do leczenia.
Cytowanie: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Słowa kluczowe: rak prostaty, oporność na leki, autofagia, białka G, enzalutamid