Clear Sky Science · pl
DNA-PKcs orchestruje indukowaną przez deplecję CTLA-4 senescencję w komórkach nowotworowych
Przełączenie przełącznika wzrostu nowotworu na sygnał stop
Leki przeciwnowotworowe oparte na układzie odpornościowym często koncentrują się na cząsteczce zwanej CTLA-4, występującej na komórkach odpornościowych, aby pomóc organizmowi zwalczać guzy. W tym badaniu ujawniono zaskakujący zwrot akcji: CTLA-4 występuje także wewnątrz samych komórek nowotworowych i może działać jak ukryty pomocnik wzrostu. Gdy naukowcy celowo usunęli tę wewnętrzną CTLA-4 z komórek czerniaka, komórki nowotworowe przestały się rozmnażać i weszły w długotrwały stan „emerytury” zwany senescencją komórkową. Zrozumienie tej nieoczekiwanej roli otwiera nowe możliwości spowolnienia lub nawet zmniejszenia guzów przez celowanie w CTLA-4 wewnątrz komórek nowotworowych, a nie tylko na komórkach układu odpornościowego.
Gdy komórki wybierają emeryturę zamiast niekontrolowanego wzrostu
Komórki normalnie dzielą się, naprawiają i — gdy ulegną uszkodzeniu nie do naprawienia — albo obumierają, albo wchodzą w senescencję, trwałe zatrzymanie ich wzrostu. Komórki senescentne zwykle stają się większe, zmieniają kształt i produkują specyficzne markery, które naukowcy wykrywają w laboratorium. Badacze stwierdzili, że gdy obniżono poziom CTLA-4 wewnątrz mysich i ludzkich komórek czerniaka, komórki zwiększyły objętość, ich wzrost spadł gwałtownie, a klasyczne sygnały senescencji wzrosły, w tym enzymy wykrywalne specjalnymi barwieniami oraz białka takie jak p16 i p21, które blokują cykl komórkowy. Zmiany te obserwowano zarówno przy tymczasowym wyciszeniu CTLA-4, jak i przy trwałym jego usunięciu narzędziami edycji genów.
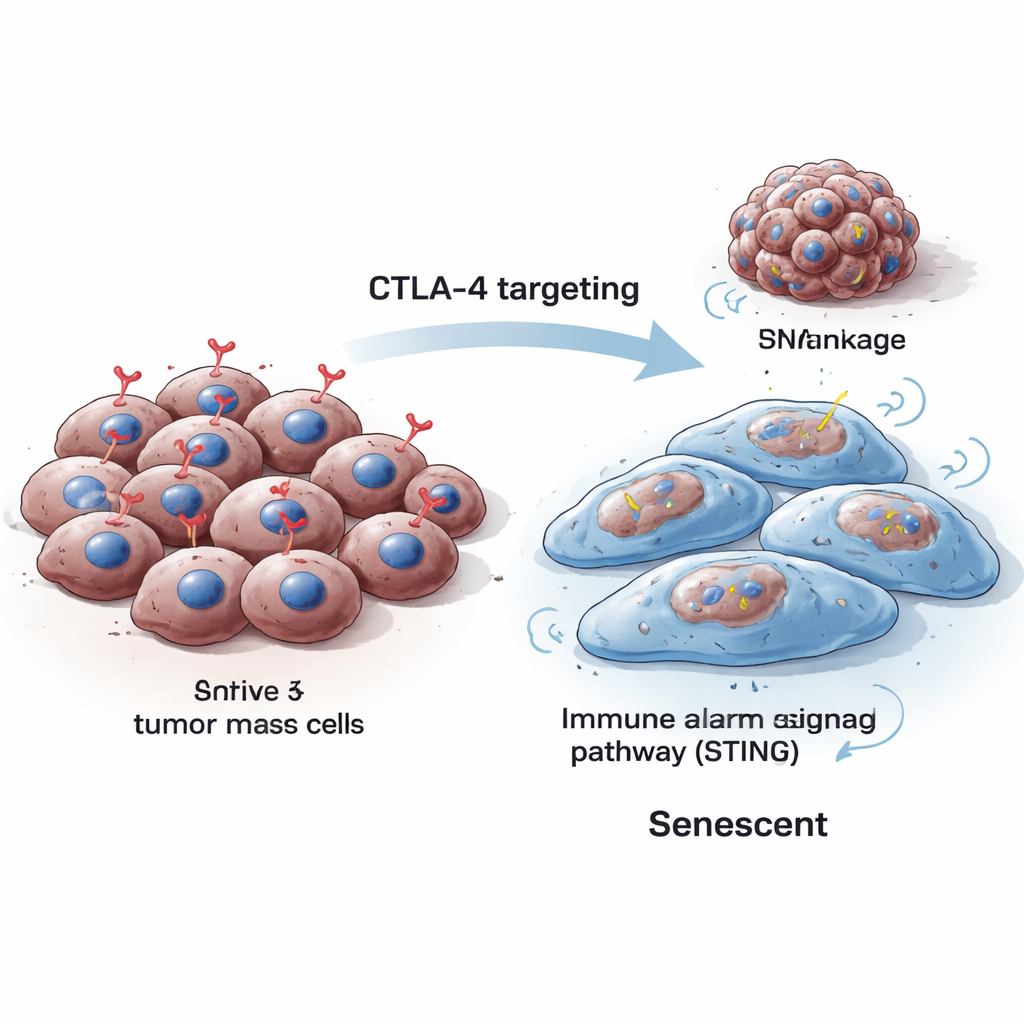
Pęknięcia w planie genetycznym prowadzą do zatrzymania
Aby zrozumieć, dlaczego utrata CTLA-4 popycha komórki nowotworowe w kierunku senescencji, zespół przyjrzał się, jak te komórki radzą sobie z DNA podczas podziału. Odkryto, że deplecja CTLA-4 obniża poziomy Aurory B, białka pomagającego w prawidłowym rozdziale chromosomów podczas podziału komórkowego. Gdy Aurora B spadła, komórki wykazywały niestabilność genomową: pojawiały się drobne dodatkowe ciała zawierające DNA zwane micronukleusami, a markery uszkodzeń DNA wzrosły. Taki stres genetyczny jest znanym czynnikiem kierującym komórki ku senescencji zamiast ku niekontrolowanemu wzrostowi. Co ważne, przywrócenie poziomów Aurory B pomogło zmniejszyć liczbę micronukleusów, łącząc bezpośrednio utratę CTLA-4 z nieprawidłowym rozdziałem chromosomów i uszkodzeniem DNA.
Uszkodzenia DNA uruchamiają wewnętrzną sieć alarmową
Złamane i nieprawidłowo umieszczone DNA w komórkach pozbawionych CTLA-4 nie pozostało niezauważone. Aktywowało DNA-PKcs, czujnik uszkodzeń DNA, który z kolei uruchomił ścieżkę STING — wbudowany system alarmowy reagujący na obce lub przemieszczone DNA w komórce. Gdy STING został włączony, sygnalizował dalej do cząsteczek takich jak TBK1 i IRF3, a także wzmacniał inną kluczową ścieżkę kontroli wzrostu — szlak AKT. Zamiast promować wzrost, to połączone sygnalizowanie ostatecznie zwiększało poziom p21, silnego hamulca cyklu komórkowego, wzmacniając stan senescencji. Gdy naukowcy zablokowali DNA-PKcs, aktywacja STING i cechy senescencji były znacznie zmniejszone, co pokazuje, że DNA-PKcs znajduje się w centrum tej sieci alarmowej.
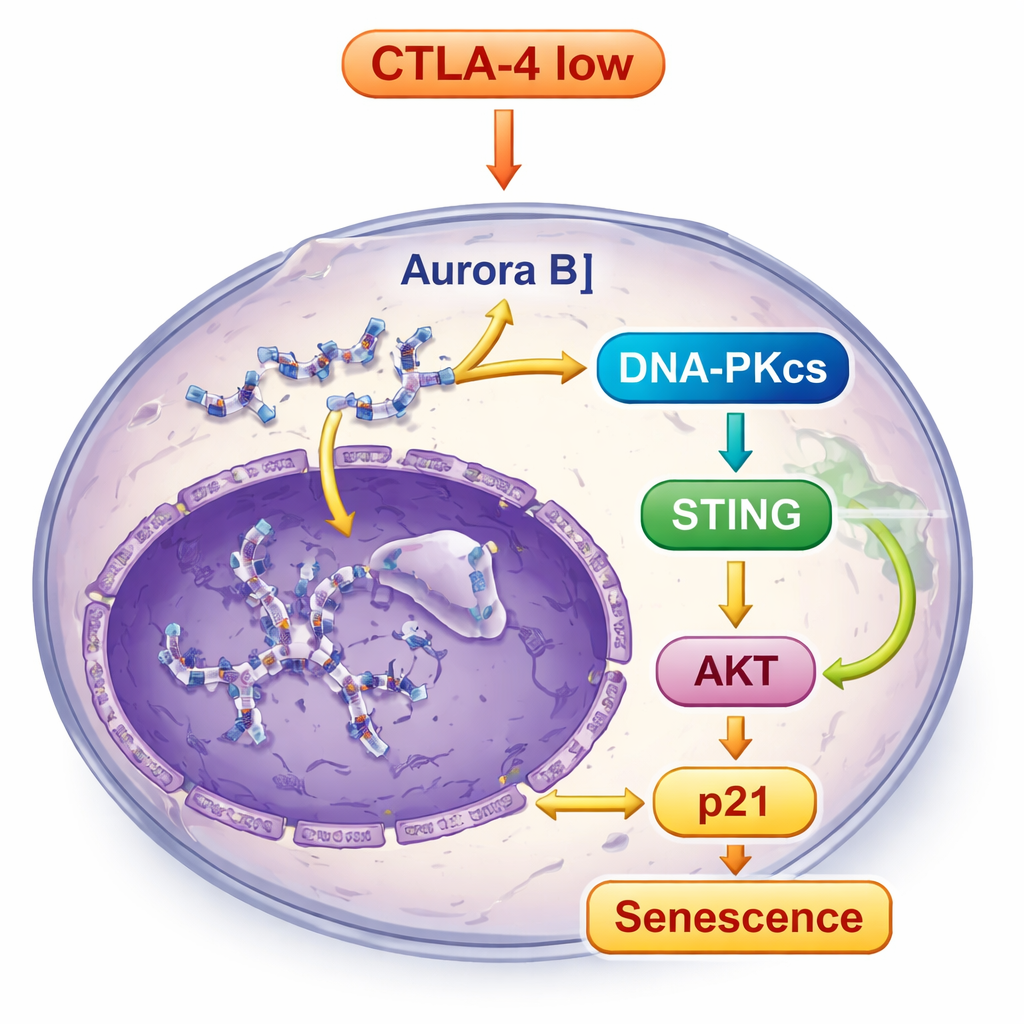
Z hodowli komórek do guzów u żywych zwierząt
Doświadczenia na szalkach laboratoryjnych dają tylko część obrazu, więc badacze sprawdzili, czy utrata CTLA-4 wpłynie na prawdziwe guzy u myszy. Wszczepili komórki czerniaka z CTLA-4 lub bez niego po przeciwnych stronach tych samych zwierząt. Guzy pozbawione CTLA-4 rosły wolniej, ważyły mniej i miały mniejszą objętość niż ich odpowiedniki zawierające CTLA-4. Te nowotwory z niedoborem CTLA-4 wykazywały również silniejsze barwienia wskazujące na senescencję oraz wyższe poziomy uszkodzeń DNA i aktywacji ścieżki STING. Analiza danych pacjentów z dużych publicznych baz potwierdziła związek: w różnych typach nowotworów ekspresja CTLA-4 wykazywała tendencję do bycia odwrotnie skorelowaną z DNA-PKcs i innymi składnikami naprawy DNA, odzwierciedlając wyniki laboratoryjne w chorobie ludzkiej.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Podsumowując, badanie pokazuje, że CTLA-4 wewnątrz komórek nowotworowych pomaga im utrzymać stabilność genetyczną i kontynuować podziały. Gdy CTLA-4 zostaje usunięta, chromosomy stają się niestabilne, kumulują się pęknięcia DNA, a wewnętrzna ścieżka alarmowa — skupiona wokół DNA-PKcs i STING — prowadzi komórki do trwałego zatrzymania wzrostu. Dla osoby niebędącej specjalistą oznacza to, że wyłączenie CTLA-4 w komórkach guza przesuwa nowotwory od niebezpiecznego, szybkiego wzrostu w kierunku bezpieczniejszego, „emerytalnego” stanu. Te spostrzeżenia sugerują, że przyszłe terapie przeciwnowotworowe mogą być projektowane nie tylko po to, by odblokować układ odpornościowy poprzez blokadę CTLA-4 na komórkach odpornościowych, ale także by bezpośrednio unieszkodliwiać guzy przez celowanie w CTLA-4 wewnątrz komórek nowotworowych i wykorzystanie senescencji jako wbudowanego hamulca wzrostu nowotworu.
Cytowanie: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Słowa kluczowe: senescencja komórkowa, czerniak, CTLA-4, uszkodzenie DNA, ścieżka STING