Clear Sky Science · pl
Cytoplazmatyczno‑jądrowy transport białka TET2: wewnętrzny hamulec w progresji raka jelita grubego
Jak komórki nowotworowe niosą własny hamulec
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie i staje się szczególnie niebezpieczny, gdy komórki guza uczą się naciekać okoliczne tkanki i rozprzestrzeniać się do innych narządów. Badanie to pokazuje, że wiele z tych komórek nosi wewnętrzny „system hamowania” — białko o nazwie TET2 — które może spowalniać ich postęp, gdy przemieści się do jądra komórkowego. Zrozumienie, jak ten wbudowany hamulec jest włączany i wyłączany, może otworzyć nowe drogi do powstrzymania wzrostu guza, nie tylko poprzez bezpośrednie niszczenie komórek nowotworowych.
Obserwowanie ruchu kluczowego białka w komórkach nowotworu
Naukowcy skupili się na TET2, białku, które pomaga kontrolować, które geny są aktywne, usuwając pewne chemiczne znaczniki z DNA. W próbkach tkanki od setek pacjentów z rakiem jelita grubego śledzili, gdzie TET2 lokalizuje się w komórkach guza. Wyróżnili cztery główne wzory: głównie w jądrze, głównie w cytoplazmie lub wyraźne przesunięcie w jedną ze stron. Pacjenci, których guzy miały więcej TET2 w jądrze, mieli zwykle dłuższe przeżycie, natomiast ci, których guzy utrzymywały TET2 w cytoplazmie, mieli gorsze rokowania. W miarę postępu choroby i przechodzenia do późniejszych stadiów klinicznych, jądrowe występowanie TET2 stawało się rzadsze, co sugeruje, że utrata tej jądrowej ochrony jest częścią procesu uczynienia guzów bardziej agresywnymi.
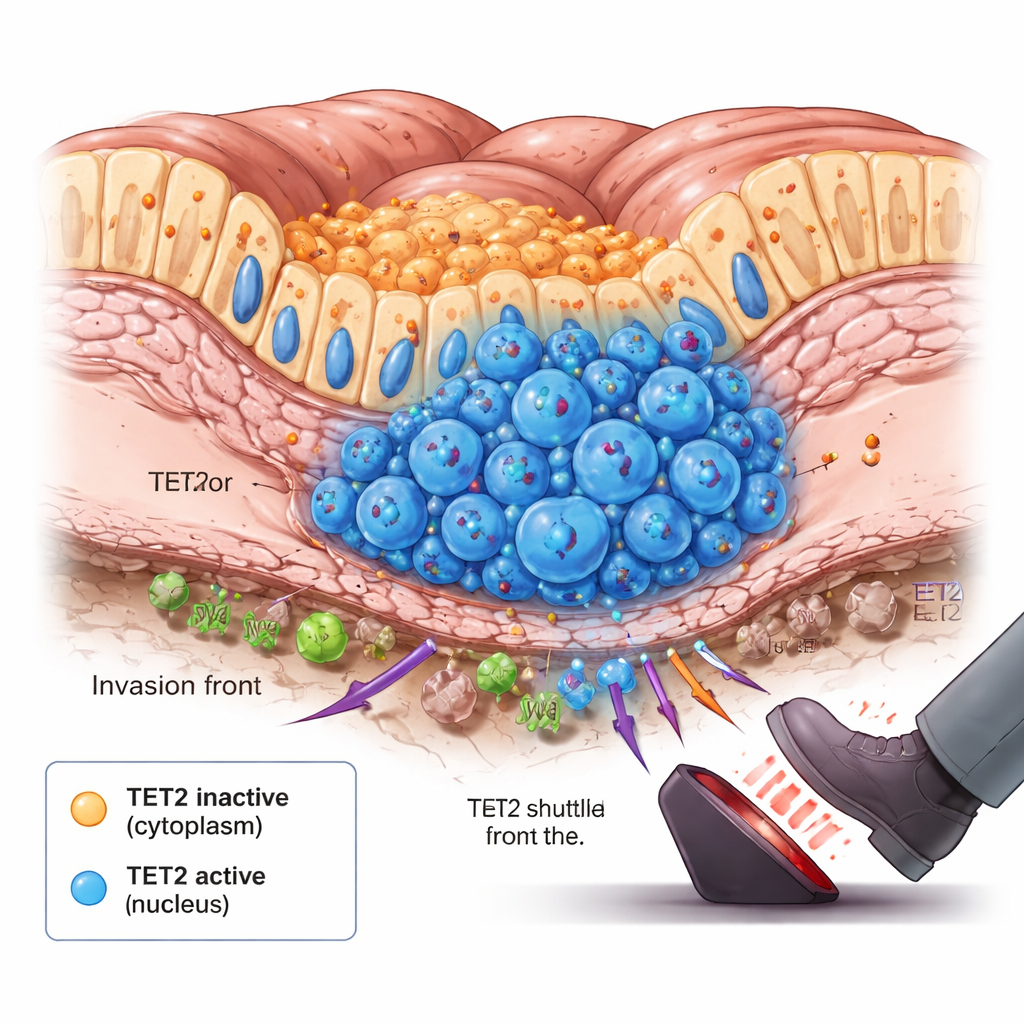
Pierwsza linia frontu guza i moment zmiany
Idąc dalej, zespół zauważył coś zaskakującego: w guzach, które dopiero zaczynały się rozprzestrzeniać, pojawiał się niewielki wzrost komórek, w których TET2 przeniósł się do jądra. Komórki te skupiały się u podstawy wyściółki jelita, na froncie inwazji, gdzie komórki nowotworowe po raz pierwszy wnikają w głębsze tkanki. Doświadczenia na zwierzętach i długoterminowe modele hodowli komórek, które odzwierciedlają wzrost guza, wykazały podobny wzorzec w czasie. Na początku TET2 pozostawało w cytoplazmie i było w dużej mierze nieaktywne. W miarę wzrostu guza i stopniowego niedoboru tlenu oraz składników odżywczych w jego wnętrzu, sygnały wewnątrzkomórkowe powodowały przemieszczenie TET2 do jądra w określonych subpopulacjach. Gdy znalazło się tam, TET2 zaczynało usuwać markery metylacji DNA i hamować wzrost guza, działając jak awaryjny hamulec, gdy nowotwór przekraczał niebezpieczny próg.
Gdy sygnały „naprzód” uruchamiają też hamulec
Guzy jelita grubego często polegają na dwóch silnych programach „naprzód”: procesie zmiany kształtu zwanego przejściem nabłonkowo‑mezenchymalnym (EMT), który ułatwia komórkom mobilność i inwazyjność, oraz ścieżce sygnalizacyjnej WNT, która wspiera wzrost i przetrwanie. Te szlaki zwykle uważa się za wyłącznie szkodliwe w kontekście nowotworu. Jednak badanie pokazuje, że gdy EMT i WNT są mocno aktywowane, jednocześnie sprzyjają przemieszczeniu TET2 do jądra. Przy użyciu leków i narzędzi genetycznych w hodowlach komórek naukowcy wykazali, że włączenie EMT lub WNT powodowało, iż więcej komórek przenosiło TET2 do jąder, podczas gdy blokowanie tych szlaków działało odwrotnie. Znajdując się w jądrze, aktywne TET2 wyciszało geny związane z EMT i WNT, zmniejszając migrację komórek i spowalniając proliferację. Innymi słowy, te same sygnały, które pomagają guzom rosnąć, uruchamiają jednocześnie wewnętrzną siłę przeciwstawną.
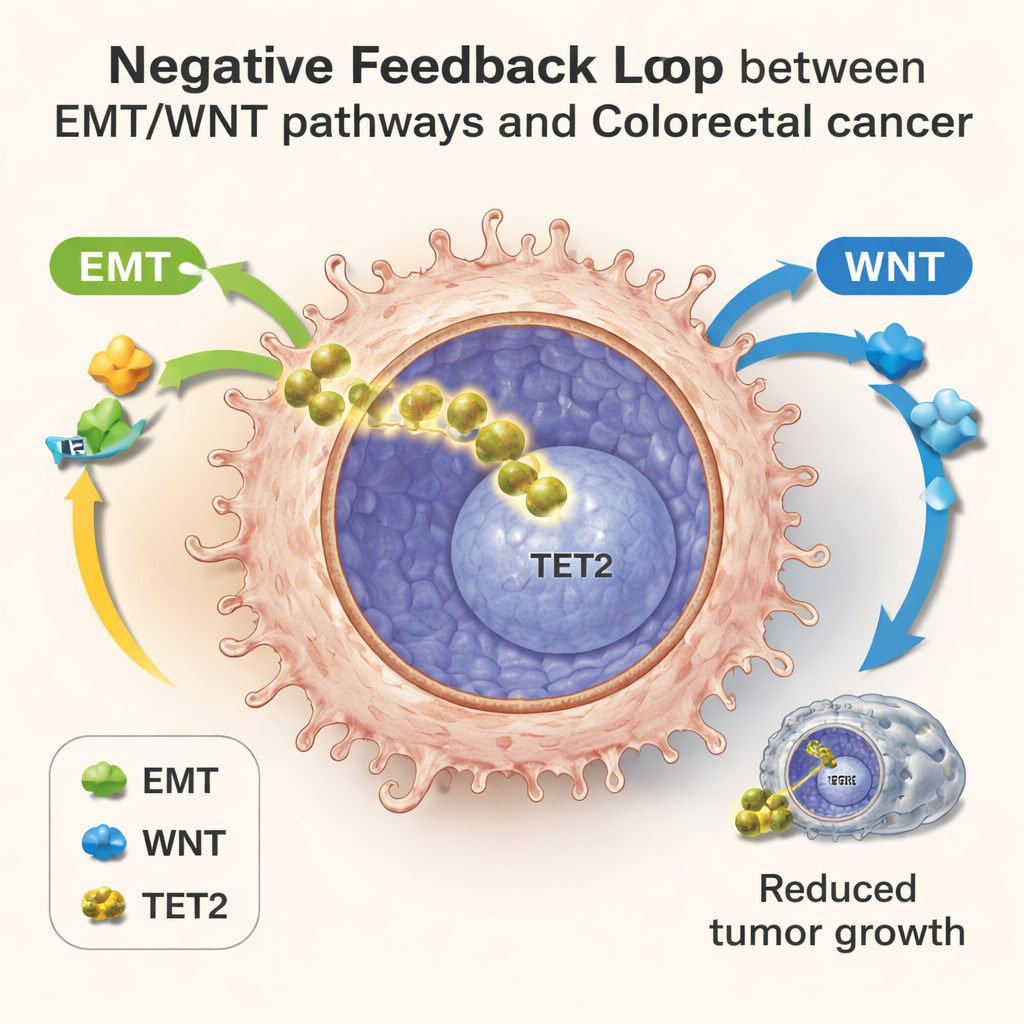
Pojedyncze komórki ujawniają ukrytą pętlę zwrotną
Aby odwzorować tę walkę o wpływy w detalach, zespół zastosował sekwencjonowanie RNA pojedynczych komórek, które odczytuje, które geny są aktywne w tysiącach pojedynczych komórek jednocześnie. W koloniach hodowanych w laboratorium, w guzach mysich i w próbkach od pacjentów z rakiem jelita grubego zaobserwowano komórki rozłożone wzdłuż osi postępu. Komórki we wczesnym stadium wykazywały normalne wykorzystanie energii i słabą aktywność EMT/WNT; komórki późniejsze wykazywały metaboliczne przeprogramowanie, silne sygnały EMT/WNT, a następnie wzrost ekspresji genów docelowych TET2. Na tych późniejszych etapach komórki z wyższą aktywnością TET2 miały niższe poziomy genów związanych z inwazją i wiązały się z lepszymi wynikami u pacjentów, nawet wśród guzów, które już zaczęły się rozprzestrzeniać. Ten wzorzec wspiera model ujemnej pętli zwrotnej: stres metaboliczny i aktywacja EMT/WNT popychają TET2 do jądra, a jądrowe TET2 z kolei hamuje te same agresywne programy.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że progresja raka jelita grubego nie jest prostym przełącznikiem „włącz/wyłącz” między zachowaniem dobrym a złym. Istnieje wbudowany, opóźniony mechanizm bezpieczeństwa: w miarę jak komórki guza stają się bardziej inwazyjne, aktywują one także TET2 w jądrach, co częściowo je powściąga. Z czasem wiele guzów unika tego mechanizmu, tracąc jądrowe TET2 lub przewyższając jego działanie. Znalezienie sposobów na utrzymanie TET2 w jądrze lub zwiększenie jego aktywności — być może w połączeniu z lekami modulującymi EMT lub WNT — mogłoby wzmocnić ten naturalny hamulec i spowolnić rozprzestrzenianie się raka. Zamiast jedynie atakować komórki nowotworowe z zewnątrz, przyszłe terapie mogłyby działać poprzez przywracanie i wzmacnianie tego wewnętrznego systemu kontroli.
Cytowanie: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Słowa kluczowe: rak jelita grubego, TET2, epigenetyka, EMT WNT sygnalizacja, progresja nowotworu