Clear Sky Science · pl
Nieprawidłowe utrzymanie czynnika transkrypcyjnego rozwoju PAX6 sprzyja śmierci komórek nerwowych przez sygnalizację JNK3
Dlaczego to badanie ma znaczenie dla widzenia
Jaskra jest jedną z głównych przyczyn trwałej ślepoty, przede wszystkim dlatego, że komórki nerwowe przenoszące informacje wzrokowe z oka do mózgu stopniowo obumierają. Wiele terapii obniża ciśnienie wewnątrzgałkowe, ale pacjenci mogą tracić wzrok mimo dobrego jego kontroli. To badanie stawia głębsze pytanie: co powoduje, że komórki zwojowe siatkówki decydują się na śmierć pod wpływem stresu i czy tę decyzję można wyłączyć na poziomie regulacji genów w jądrze komórkowym?
Siatkówka pod atakiem stresu
U podstaw jaskry i powiązanych chorób oczu leży powolna utrata komórek zwojowych siatkówki (RGC), będących neuronami wyjściowymi oka. Komórki te są podatne na wiele rodzajów stresu, w tym toksyczne poziomy przekaźnika glutaminianu, który nadmiernie aktywuje receptory NMDA i wywołuje szkodliwe przeciążenie wapniowe. Badacze zastosowali dobrze znany model myszy, w którym niewielką ilość NMDA wstrzykuje się do oka, selektywnie uszkadzając RGC przy zachowaniu większości pozostałych warstw siatkówki. Potwierdzili, że to leczenie nie zmienia ciśnienia oka, lecz wywołuje typowe oznaki programowanej śmierci komórek w RGC, takie jak uwalnianie cytochromu c z mitochondriów i pojawienie się jąder pozytywnych w teście TUNEL.
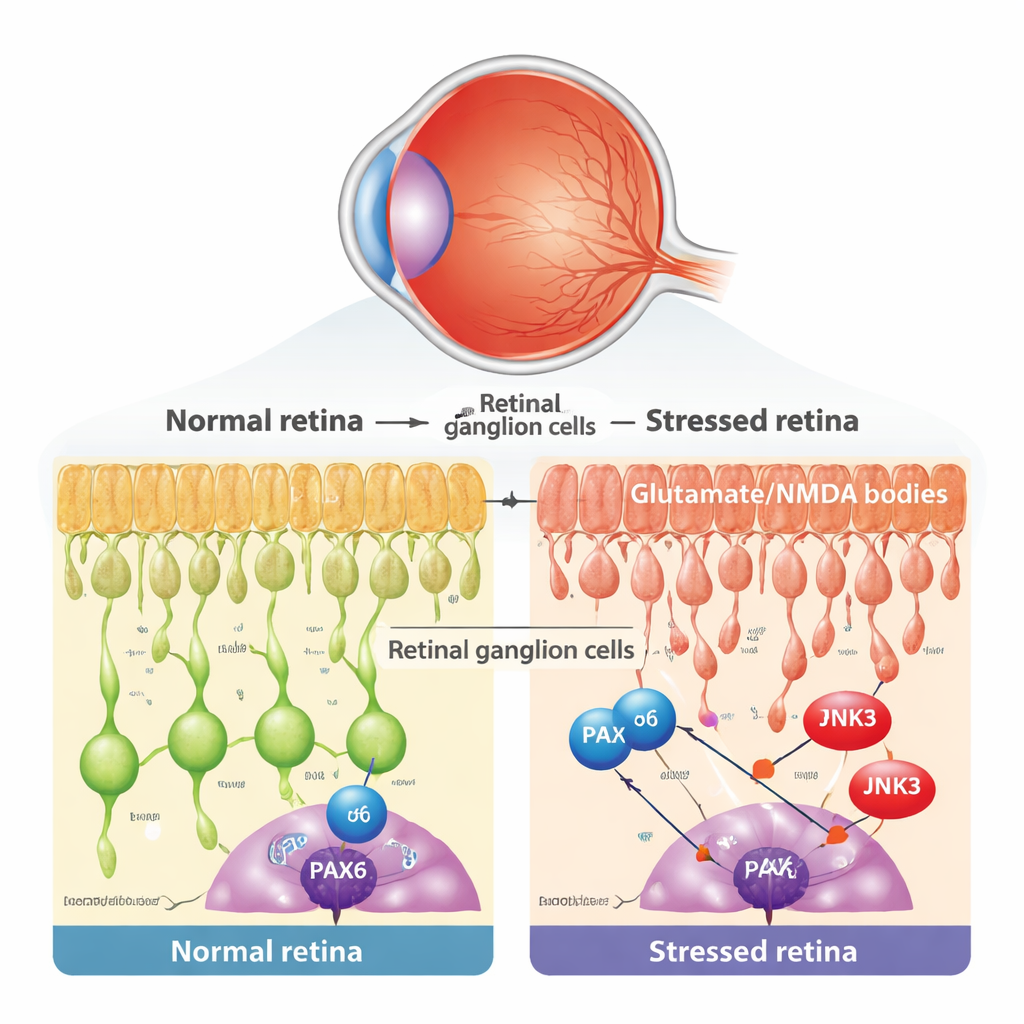
Gen rozwojowy, który odmawia emerytury
W czasie wczesnego rozwoju regulator genowy PAX6 działa jako główny architekt oka, kierując powstawaniem i okablowaniem różnych komórek siatkówki. Powszechne przekonanie głosi, że takie programy rozwojowe w dorosłości są w dużej mierze wyciszane. Ponowna analiza danych z pojedynczych komórek RNA-seq z mysich i ludzkich siatkówek wykazała jednak, że PAX6 jest silnie i selektywnie utrzymywany w dojrzałych RGC i w pewnych interneuronach. Badania mikroskopowe z barwieniem pokazały, że w warstwie, gdzie znajdują się RGC, PAX6 występuje głównie w komórkach zwojowych, a nie w sąsiednich komórkach amakrynowych. To zasugerowało intrygującą możliwość: w chorobie dorosłych dawny program rozwojowy może zostać przejęty i przerodzony w czynnik napędzający degenerację.
Z opiekuna w kata: PAX6 zmienia role
Aby sprawdzić, czy PAX6 pomaga RGC przetrwać, czy też ginąć pod wpływem stresu, naukowcy zastosowali podejście przypominające terapię genową. Dostarczyli wektor wirusowy niosący małe RNA specyficznie obniżające poziom PAX6 w siatkówce, a następnie poddali oczy działaniu NMDA. W porównaniu z oczami kontrolnymi siatkówki pozbawione PAX6 wykazywały znacznie mniej apoptycznych RGC i znacznie mniejsze uszkodzenia mitochondriów, co wskazuje, że PAX6 jest wymagany do pełnego przebiegu śmierci komórki w tym modelu. Sekwencjonowanie RNA całego genomu ujawniło, że wiele genów pro-śmierci, szczególnie zaangażowanych w uszkodzenie mitochondriów i aktywację kaspaz, było silnie indukowanych przez NMDA u normalnych myszy, lecz ich indukcja była osłabiona po wyciszeniu PAX6. Innymi słowy, PAX6 pomaga włączać sieć genów, które doprowadzają RGC do granicy przeżycia.
Kinaza stresu, która przełącza PAX6
Jak stres aktywuje PAX6 bez zwiększania jego ilości? Zespół skupił się na JNK3, enzymie reagującym na stres, występującym głównie w neuronach. W czasie urazu NMDA JNK3 przemieścił się do jądra RGC i fizycznie związał z PAX6. Doświadczenia biochemiczne „próbówkowe” z oczyszczonymi białkami pokazały, że JNK3 może bezpośrednio dodać grupy fosforanowe do PAX6, a reakcję tę blokował inhibitor JNK. U myszy pozbawionych genu Jnk3 NMDA nie wywoływało już tego samego wzoru fosforylacji PAX6. Mapowanie chromatyny (ChIP-seq) i ukierunkowane testy wiązania DNA ujawniły, że pod wpływem stresu ufosforylowany PAX6 wraz z JNK3 zaczyna silniej wiązać się w rejonach kontrolnych kluczowych genów pro-apoptotycznych, takich jak Bax i Gadd45a, zwiększając ich aktywność. Gdy PAX6 był wyciszony lub JNK3 genetycznie usunięty, to wiązanie i odpowiadająca mu aktywacja genów pro-śmierci były wyraźnie osłabione.
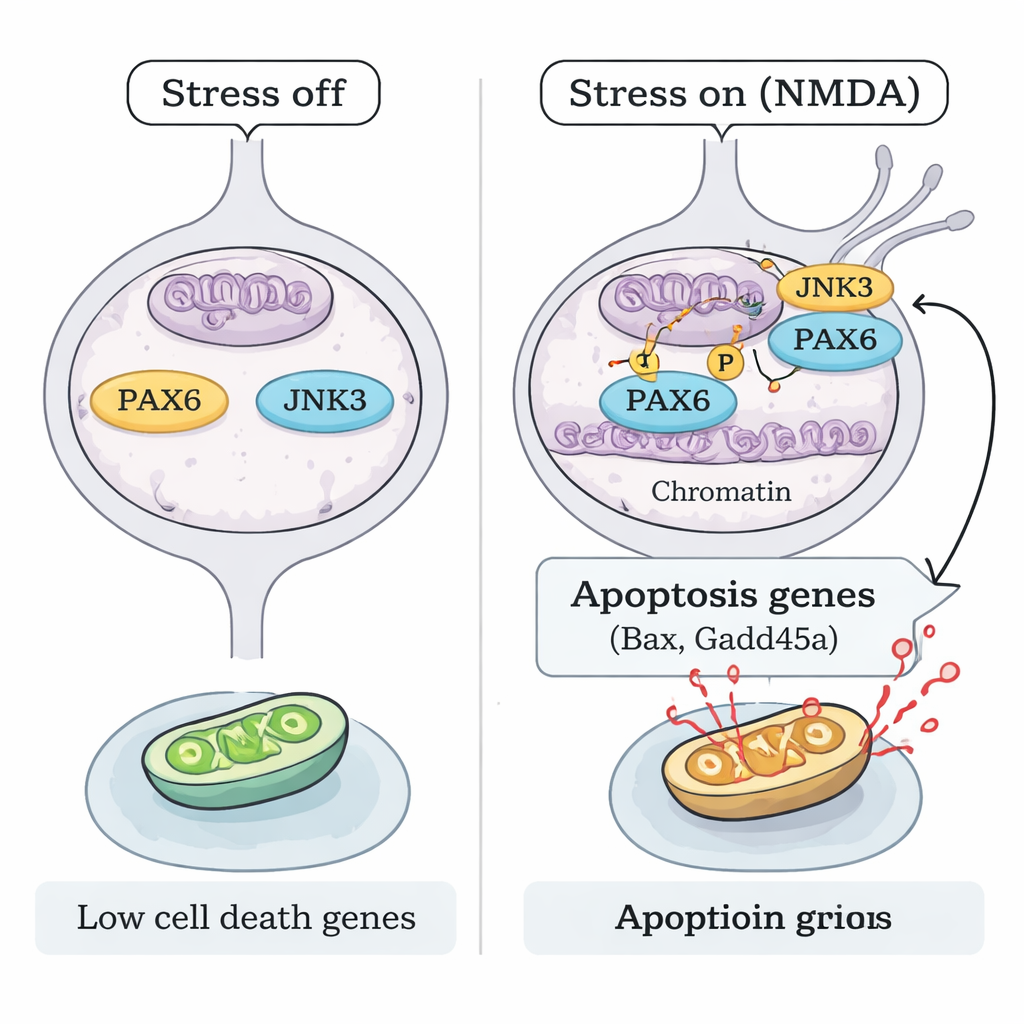
Wyłączanie programu śmierci dla ochrony wzroku
Na koniec badacze sprawdzili, czy zablokowanie osi JNK3–PAX6 wystarczy, by chronić komórki krytyczne dla widzenia. Zarówno w myszach z wyciszonym PAX6, jak i w myszach pozbawionych JNK3, RGC były istotnie zachowane po ekspozycji na NMDA, z mniejszą liczbą umierających komórek i lepszą strukturą siatkówki. To wskazuje jasny model mechanistyczny: pod wpływem pobudzenia toksycznego JNK3 fosforyluje trwale obecny PAX6, przekształcając go z budowniczego rozwojowego w silny aktywator programu genów prowadzących do śmierci komórki w dojrzałych RGC. Przerwanie tego połączenia — przez wyciszenie PAX6 lub wyłączenie JNK3 — utrzymuje wiele z tych neuronów przy życiu. Dla pacjentów wynika z tego, że przyszłe terapie jaskry mogą wykraczać poza obniżanie ciśnienia oka i bezpośrednio celować w genetyczne przełączniki decydujące o losie neuronów siatkówki.
Cytowanie: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
Słowa kluczowe: jaskra, komórki zwojowe siatkówki, PAX6, JNK3, neurodegeneracja