Clear Sky Science · pl
Ukierunkowanie ENO1 przeprogramowuje polaryzację makrofagów, aby wywołać odporność przeciwnowotworową i poprawia efekt terapeutyczny radioterapii
Przekształcanie tarcz nowotworu w cele
Nowotwory często przetrwają nie tylko dzięki szybkiemu wzrostowi, lecz także przez ciche unieszkodliwianie obrony organizmu. W tym badaniu analizuje się ukryty czynnik na komórkach nowotworowych, nazwany ENO1, który pomaga guzom unikać układu odpornościowego i opierać się radioterapii. Opracowując nowe przeciwciało celowane przeciw ENO1, badacze pokazują, że można usunąć ochronne związki z guza, obudzić komórki odpornościowe i zwiększyć skuteczność promieniowania w modelach raka jelita grubego i potrójnie ujemnego raka piersi. 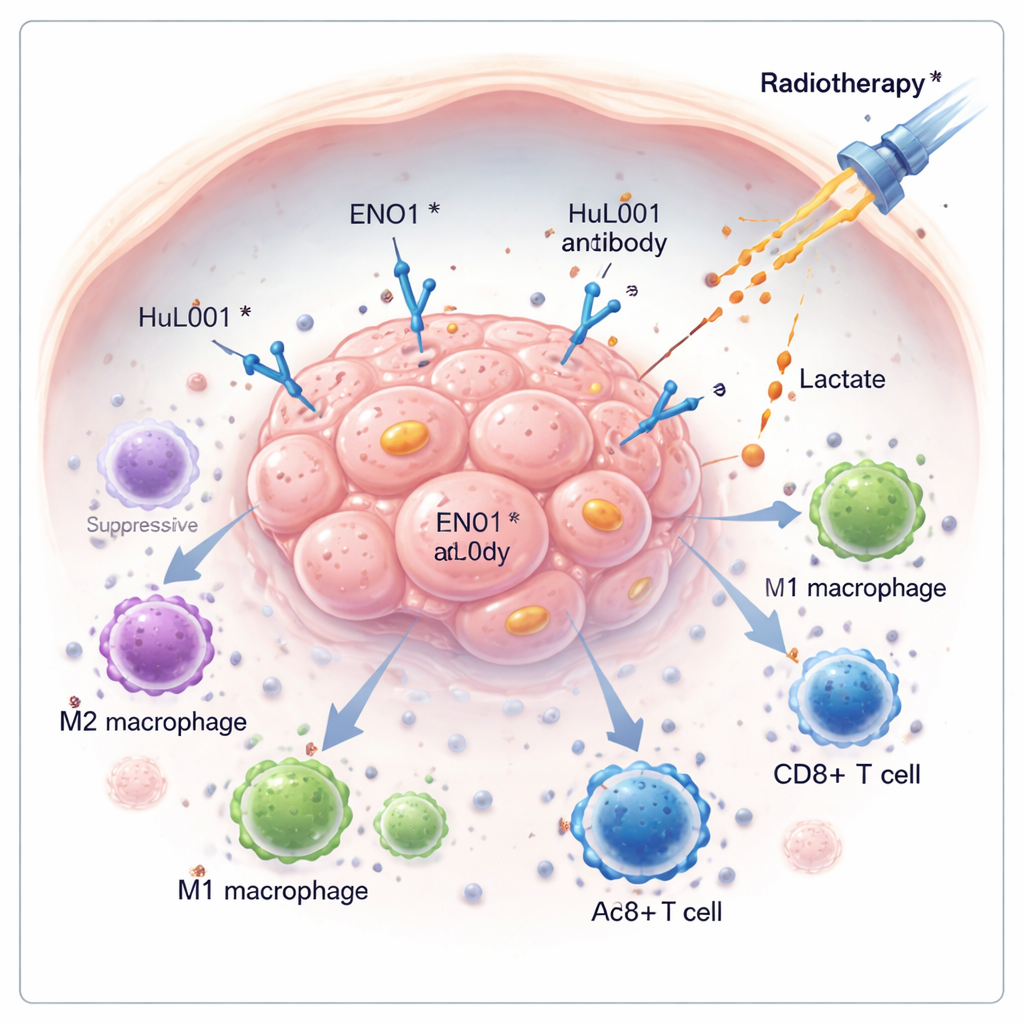
Metaboliczny trik, który ucisza odporność
Wiele guzów przebudowuje sposób wykorzystania energii, rozkładając cukier w sposób generujący duże ilości kwasu mlekowego nawet przy dostępnie tlenu. Ten kwas mlekowy jest wypompowywany z komórek nowotworowych i gromadzi się wokół guza, przekształcając otoczenie w agresywną, kwaśną niszę osłabiającą atak immunologiczny. W niniejszej pracy autorzy skupiają się na ENO1, enzymie uczestniczącym w rozkładzie cukrów, który może także pojawiać się na powierzchni komórek nowotworowych. Gdy znajduje się na powłoce komórkowej, ENO1 współpracuje z innym białkiem — transporterem MCT4 — aby pomagać w eksporcie mleczanu, podtrzymując środowisko sprzyjające wzrostowi guza i tłumiące komórki odpornościowe.
Jak radioterapia może się zemścić
Radioterapia ma na celu uszkodzenie DNA guza i wywołanie odpowiedzi immunologicznych, ale ma też skutki uboczne w mikrośrodowisku guza. Zespół odkrył, że sygnały wywoływane przez cząsteczkę TGFβ1, które są nasilane przez promieniowanie, aktywują enzym (PRMT5), który chemicznie modyfikuje ENO1 i przemieszcza je na powierzchnię komórek nowotworowych. Gdy tam się znajdzie, ENO1 fizycznie interaguje z MCT4, stabilizując go i promując eksport mleczanu. Wyższe poziomy ENO1 na powierzchni wykryto u pacjentów z zaawansowanym rakiem jelita grubego i potrójnie ujemnym rakiem piersi — powiązano je z większą przerzutowością i gorszym przeżyciem, co sugeruje, że radioterapia może mimowolnie wzmocnić tarczę tłumiącą odporność opartą na mleczanie wokół guzów.
Przeprogramowywanie „przyjaznych” i wrogich komórek odpornościowych
W kwaśnej otoczce wokół guzów komórki odpornościowe zwane makrofagami zostają wypchnięte w stan „leczący” (często nazywany M2), który w istocie pomaga guzzom, tłumiąc zapalenie i wspierając naprawę zamiast zabijania komórek nowotworowych. Naukowcy stworzyli zhumanizowane przeciwciało, HuL001, które rozpoznaje ENO1 zarówno na komórkach mysich, jak i ludzkich. W hodowlach komórkowych i modelach mysich HuL001 zakłócał wsparcie ENO1 dla MCT4, zmniejszał uwalnianie mleczanu i przesuwał makrofagi z promotorowego dla guza stanu M2 w stronę stanu M1, który jest bardziej agresywny wobec nowotworu i lepiej pochłania komórki nowotworowe. Co ważne, HuL001 nie zabijał po prostu makrofagów; zamiast tego przeedukowywał je, jednocześnie bezpośrednio zwiększając śmierć komórek nowotworowych.
Sprawienie, by radioterapia działała mocniej
Gdy HuL001 połączono z radioterapią w modelach mysich raka jelita grubego i potrójnie ujemnego raka piersi, guzy kurczyły się bardziej, odrastały wolniej, a u wielu zwierząt całkowicie zanikały. 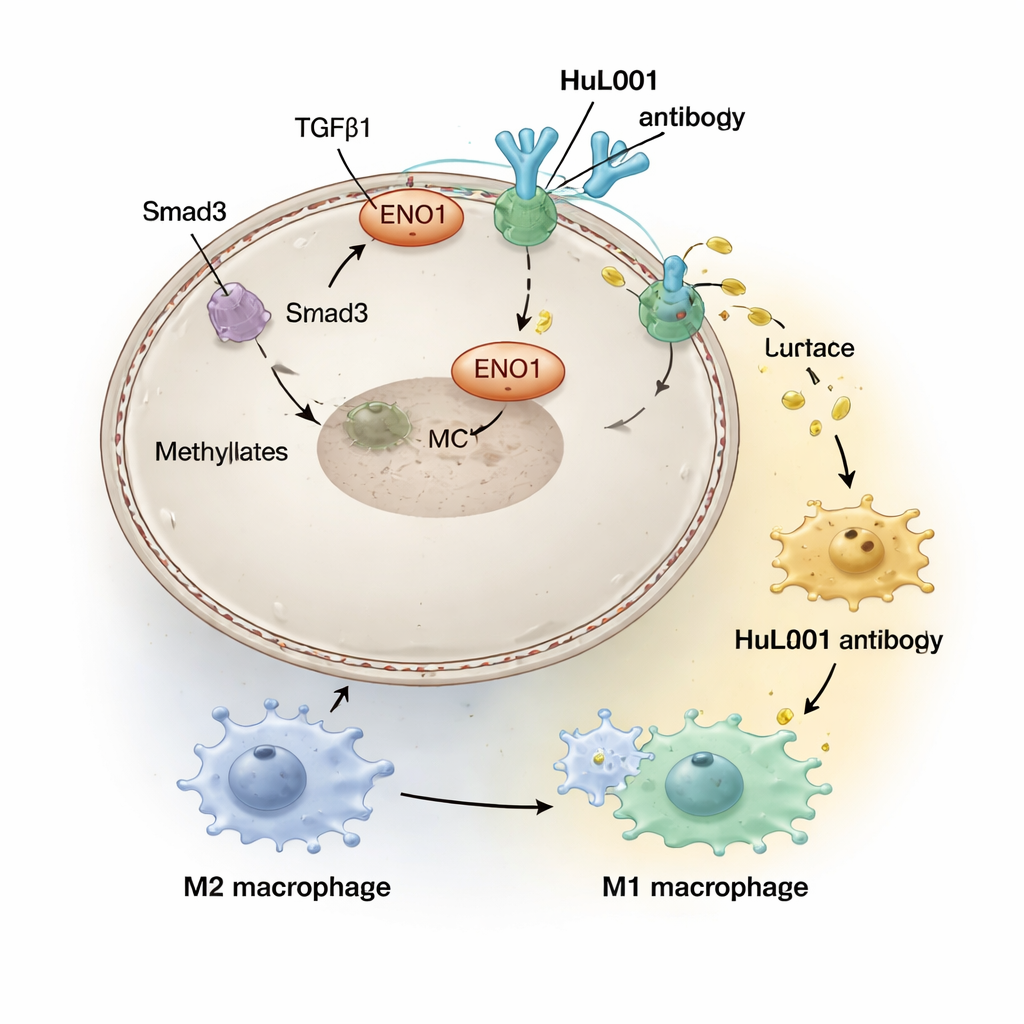
Od złożonych szlaków do praktycznych obietnic
Dla czytelników niebędących specjalistami przesłanie tego badania jest takie, że chemia guza i jego sąsiedztwo komórek odpornościowych są głęboko powiązane. ENO1 znajduje się na skrzyżowaniu: pomaga guzom spalać cukier, eksportować kwas mlekowy i rekrutować niewłaściwy rodzaj pomocy immunologicznej. Blokując powierzchniowe ENO1 za pomocą celowanego przeciwciała, badacze byli w stanie zmniejszyć szkodliwe gromadzenie mleczanu, przestawić makrofagi z pomocników guza na jego przeciwników i zwiększyć skuteczność radioterapii w trudno leczonych modelach raka. Choć HuL001 nie jest jeszcze lekiem klinicznym, praca ta sugeruje, że celowanie w metabolicznych strażników, takich jak ENO1, może stać się skutecznym sposobem, by obrócić obronę guza przeciwko niemu samemu i wzmocnić istniejące terapie, takie jak radioterapia.
Cytowanie: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
Słowa kluczowe: metabolizm guza, polaryzacja makrofagów, radioterapia, immunoterapia, mleczan