Clear Sky Science · pl
Sec8: nowy pozytywny regulator RIG-I w obronie przed wirusami RNA
Jak nasze komórki wykrywają podstępne wirusy
Wiele groźnych wirusów, w tym wirus grypy i wyłaniające się wirusy zwierzęce, przechowuje materiał genetyczny w postaci RNA. Nasze komórki polegają na wewnętrznych systemach alarmowych, które szybko dostrzegają tych najeźdźców i uruchamiają odpowiedź przeciwwirusową. W tej pracy zbadano mało znane białko komórkowe o nazwie Sec8 i pokazano, że odgrywa istotną rolę w utrzymywaniu jednego z kluczowych czujników wirusowych, RIG‑I, przy życiu i aktywnym wystarczająco długo, by nas chronić.
Komórkowy alarm włamywacza zagrożony
RIG‑I to molekularny „alarm antywłamaniowy”, który patroluje wnętrze komórek w poszukiwaniu fragmentów wirusowego RNA. Gdy wykryje podejrzane RNA, zmienia konformację, aktywuje się i wysyła sygnały, które ostatecznie wywołują produkcję interferonów typu I — silnych cząsteczek ostrzegawczych, które pomagają pobliskim komórkom stawić opór zakażeniu i uruchamiać mechanizmy odpornościowe. Ponieważ nadmiernie aktywny alarm może powodować szkodliwe stany zapalne lub choroby autoimmunologiczne, komórki ściśle regulują poziomy RIG‑I. Kilka innych białek może oznaczać RIG‑I do zniszczenia przez przyłączenie małych łańcuchów ubikwityny, kierując je do komórkowego „niszczyciela” — proteasomu. Dotąd nie było jasne, które dodatkowe czynniki komórkowe chronią RIG‑I przed przedwczesnym zniszczeniem, zwłaszcza podczas aktywnej infekcji wirusami RNA.
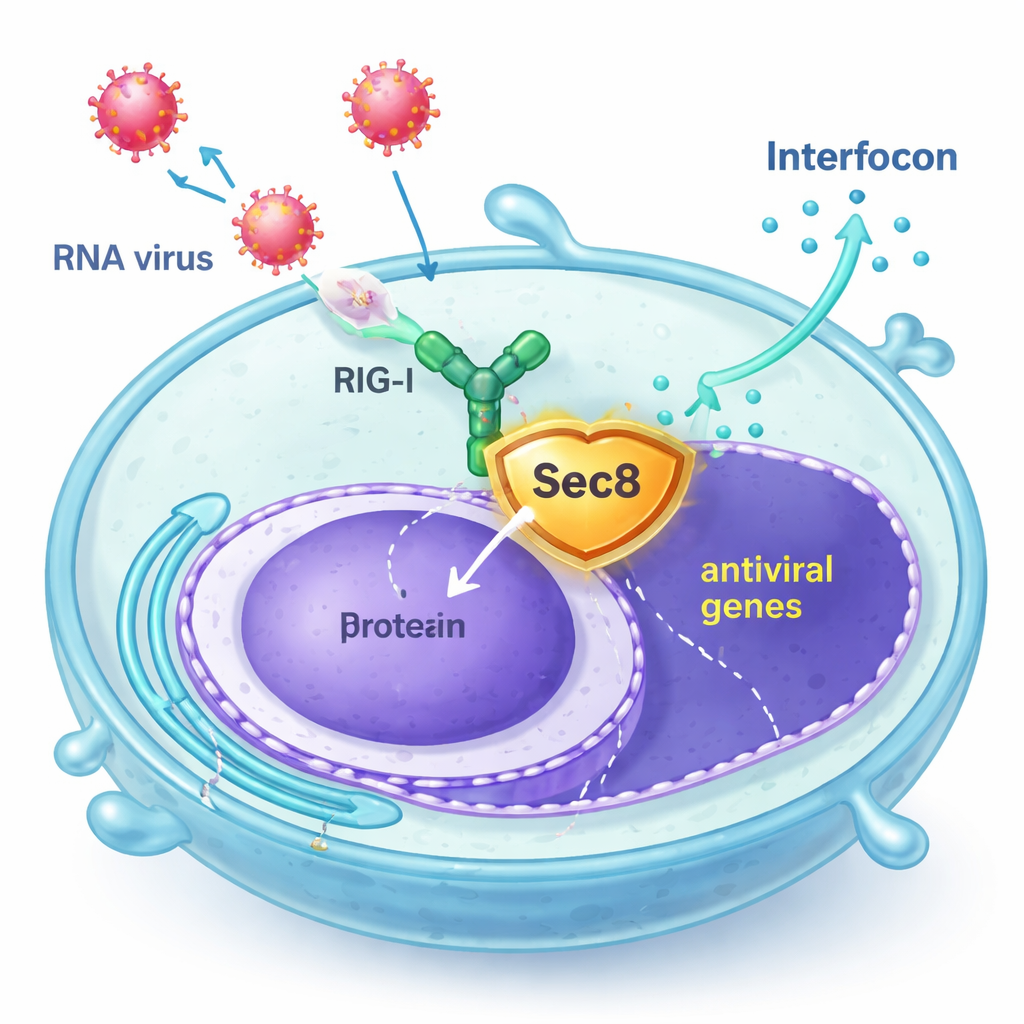
Sec8 wchodzi do gry jako ochroniarz
Autorzy odkryli, że Sec8, znany przede wszystkim jako członek ośmiobiałkowego kompleksu wspomagającego fuzję pęcherzyków wydzielniczych z powierzchnią komórki, w rzeczywistości wzmacnia sygnalizację przeciwwirusową. W ludzkich liniach komórkowych i w pierwotnych komórkach odpornościowych myszy zwiększenie poziomów Sec8 prowadziło do silniejszej aktywacji genów związanych z interferonem po zakażeniu wirusami RNA, takimi jak wirus pęcherzykowego zapalenia jamy ustnej (VSV) i wirus Sendai, albo po ekspozycji na syntetyczne RNA wirusowe. Odwrotnie, zmniejszenie ilości Sec8 obniżało produkcję interferonu i genów stymulowanych przez interferon, pozostawiając komórki mniej zdolne do hamowania replikacji wirusa. Wyniki te sugerują, że Sec8 działa nie tylko w wydzielaniu, lecz także jako pozytywny regulator w ścieżce alarmu przeciwwirusowego.
Blokowanie komórkowego niszczyciela
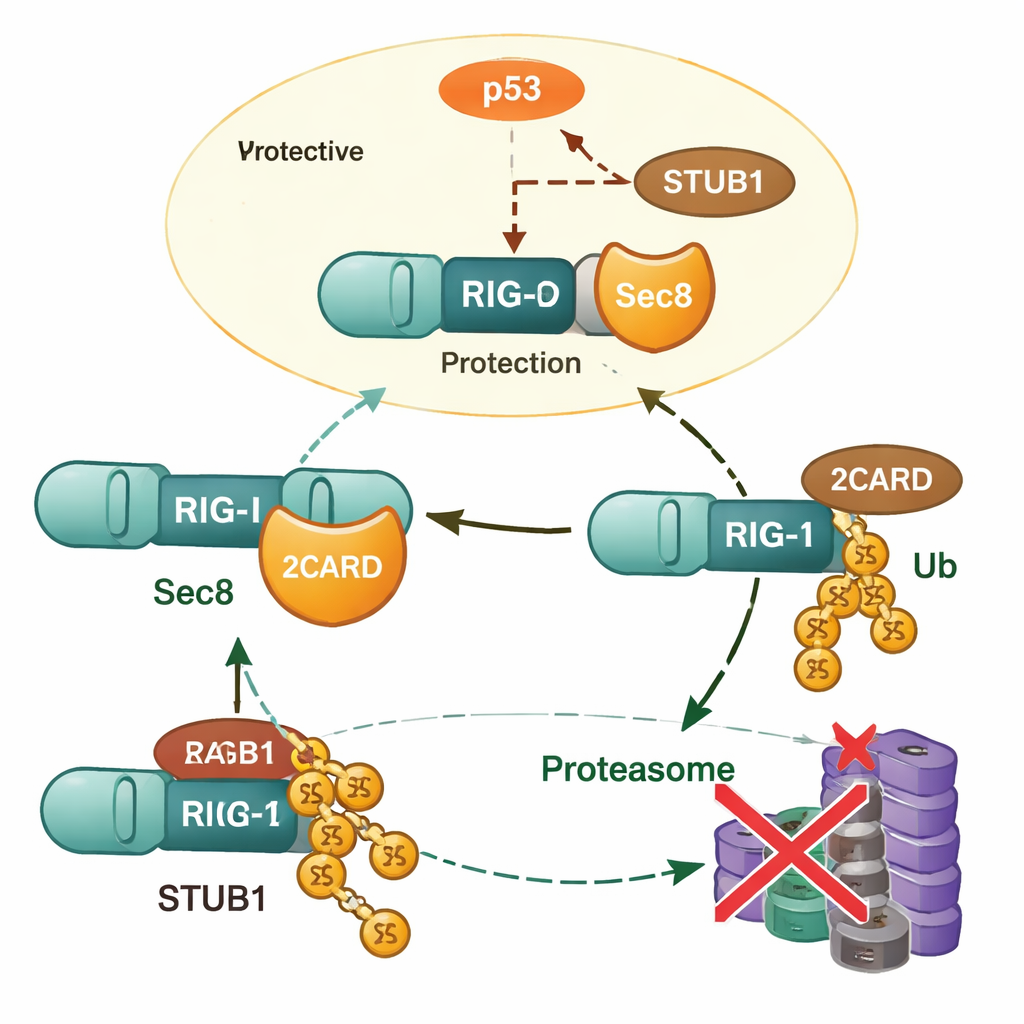
Wnikliwsze badania wykazały, że Sec8 nie zwiększa ekspresji genu RIG‑I; zamiast tego chroni białko RIG‑I przed degradacją. Gdy Sec8 usunięto, poziomy RIG‑I spadały szybciej, a tej utraty można było zapobiec za pomocą leków blokujących proteasom, co wskazuje na zaangażowanie komórkowego systemu recyklingu białek. Zespół zidentyfikował inne białko, STUB1, jako kluczowego „oznaczającego”, które przyłącza specyficzny typ łańcucha ubikwityny (powiązany przez K48) do RIG‑I w reszcie aminokwasowej lizyny 190. Ten znacznik kieruje RIG‑I do zniszczenia. Sec8 zakłóca ten proces na dwa sposoby: fizycznie konkuruje ze STUB1 o wiązanie się z tym samym regionem aktywacyjnym RIG‑I oraz obniża ilość STUB1 produkowaną przez komórkę.
Sec8, p53 i kontrola „znacznika”
Aby wyjaśnić, jak Sec8 redukuje produkcję STUB1, autorzy zwrócili się do regulacji genów. Wskaźnikowo zidentyfikowali krótki odcinek DNA, który działa jako kluczowy włącznik (promotor) genu STUB1 i wykazali, że słynne białko supresorowe nowotworów p53 wiąże się z tym regionem i podnosi poziomy STUB1. Sec8 osłabia zarówno ilość p53, jak i jego aktywującą fosforylację, więc p53 nie może już tak skutecznie pobudzać produkcji STUB1. Gdy p53 było zablokowane lub STUB1 wyciszone, szkodliwe efekty utraty Sec8 na produkcję interferonu i wzrost wirusa zostały w dużej mierze odwrócone. Umieszcza to Sec8 na szczycie łańcucha regulacyjnego biegnącego od p53 do STUB1 i ostatecznie do stabilności RIG‑I.
Z płytki Petriego do organizmów żywych
Zespół następnie przetestował znaczenie Sec8 u myszy zaprojektowanych tak, by brakowało genu Sec8 specyficznie w niektórych komórkach odpornościowych. Po zakażeniu VSV te zwierzęta produkowały mniej interferonu, miały większe ilości wirusa w narządach takich jak śledziona, wątroba i płuca oraz wykazywały poważniejsze uszkodzenia płuc, większą utratę masy ciała i niższą przeżywalność niż myszy kontrolne. Wyniki in vivo potwierdziły, że Sec8 nie jest drobnym graczem, lecz istotnym opiekunem przeciwko zakażeniom wirusami RNA w całym organizmie.
Dlaczego to ma znaczenie dla przyszłych terapii
Mówiąc wprost, to badanie pokazuje, że Sec8 działa jak ochroniarz czujnika przeciwwirusowego RIG‑I. Utrzymując „oznaczające” białko STUB1 w ryzach i bezpośrednio osłaniając RIG‑I przed skierowaniem do komórkowego niszczyciela, Sec8 pozwala komórkom szybko wygenerować odpowiedź interferonową i lepiej kontrolować wirusy RNA. Zrozumienie nowo opisanego osi p53–STUB1–RIG‑I otwiera drzwi do przyszłych strategii przeciwwirusowych, które stabilizowałyby RIG‑I lub naśladowałyby ochronne działania Sec8, potencjalnie wzmacniając nasze mechanizmy obronne przeciw szerokiemu spektrum wirusów opartych na RNA.
Cytowanie: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Słowa kluczowe: odporność wrodzona, wirusy RNA, RIG-I, ubikwitynacja, sygnalizacja interferonowa