Clear Sky Science · pl
Fibroblasty związane z rakiem (CAF) pochodzące od MFAP2 wspierają proliferację i przerzuty CRC, jednocześnie tłumiąc przeciwnowotworową odporność komórek CD8+ T
Dlaczego sąsiedztwo guza ma znaczenie
Rak jelita grubego należy do najczęstszych i najbardziej śmiertelnych nowotworów na świecie, a lekarze wciąż mają trudności z powstrzymaniem jego rozsiewu i z przewidywaniem, u których pacjentów przebieg będzie niekorzystny. To badanie analizuje nie tylko komórki nowotworowe, lecz także ich „sąsiadów” — komórki wspierające i komórki odpornościowe współdzielące to samo środowisko. Badacze ujawniają, jak określony typ komórek wspomagających, zwany fibroblastami związanymi z nowotworem, może dyskretnie napędzać wzrost guza i uciszać własne komórki T organizmu zdolne do zabijania raka. Zrozumienie tej ukrytej komunikacji może otworzyć drogę do nowych terapii, które zwiększą skuteczność obecnych metod leczenia.
Ukryci pomocnicy wewnątrz guzów jelita
Guz jelita to nie tylko skupisko zbuntowanych komórek, lecz miniaturowy ekosystem. Jednymi z najważniejszych jego mieszkańców są fibroblasty związane z nowotworem, czyli CAF. Komórki te tworzą tkankę łączną, przebudowują otoczenie guza i wydzielają czynniki sygnalizacyjne. Analizując próbki od pacjentów i duże bazy danych genowych, autorzy stwierdzili, że białko o nazwie MFAP2 występuje na znacznie wyższym poziomie w nowotworach jelita cienkiego i grubego niż w prawidłowej tkance okrężnicy, a pacjenci z wyższym poziomem MFAP2 mają tendencję do gorszego przeżycia. Wykazali, że to właśnie CAF, a nie same komórki nowotworowe, są głównymi producentami MFAP2 w tych guzach. W komórkach hodowanych w laboratorium i w modelach mysi obecność CAF bogatych w MFAP2 ściśle korelowała z szybszym wzrostem guza i bardziej agresywnym przebiegiem choroby.
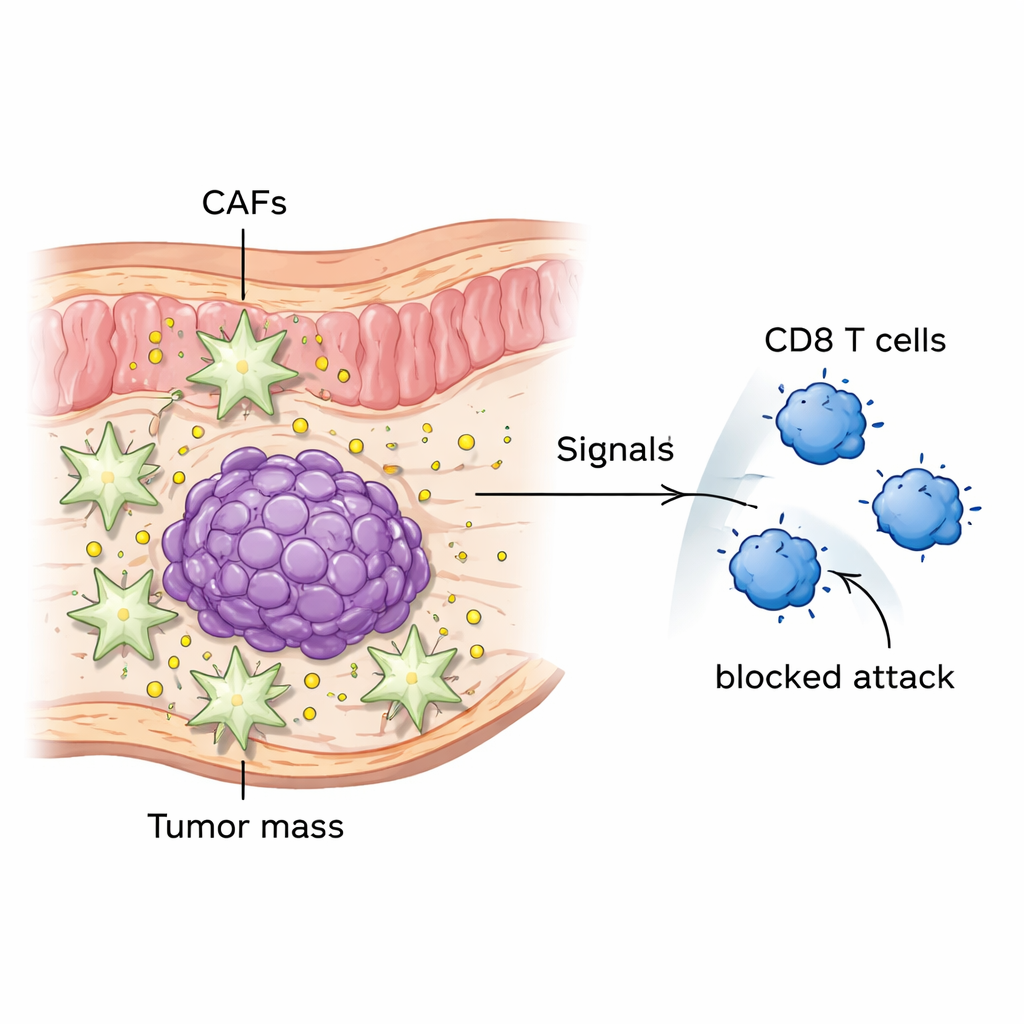
Przełącznik wzrostu w komórkach nowotworowych
Zespół następnie zbadał, w jaki sposób MFAP2 faktycznie pobudza komórki rakowe do wzrostu i rozsiewu. Odkryli, że MFAP2 uwalniane przez CAF wiąże się z receptorem o nazwie integryna β8 (ITGB8) na powierzchni komórek raka jelita grubego. To połączenie uruchamia wewnętrzny szlak sygnałowy znany jako FAK–ERK1/2, dobrze znany z roli w stymulacji podziałów i migracji komórek. Jednym z kluczowych regulatorów włączanych przez ten szlak jest czynnik transkrypcyjny ETS2. Wzrost poziomów ETS2 sprawia, że komórki nowotworowe jelita stają się bardziej inwazyjne i lepiej znoszą atak komórek odpornościowych. Gdy badacze zablokowali MFAP2 lub ITGB8 albo obniżyli poziom ETS2, guzy u myszy zmniejszały się, a przerzuty do wątroby występowały rzadziej.
Jak guzy pozbawiają się ataku ze strony odporności
Guzy jelita często są nacieczone komórkami T CD8 — komórkami odpornościowymi wyspecjalizowanymi w rozpoznawaniu i zabijaniu komórek nowotworowych. Pacjenci, których guzy zawierają więcej tych komórek, zwykle żyją dłużej. Tymczasem w guzach o wysokim poziomie MFAP2 badacze stwierdzili mniej komórek CD8 oraz cechy ich wyczerpania i mniejszej efektywności. Efekt ten powiązano ze zmianą w sposobie gospodarowania cholesterolem przez komórki guza. ETS2 zwiększa ekspresję enzymu CYP27A1, który przekształca cholesterol w cząsteczkę 27‑hydroksycholesterolu (27‑HC). Ta lipofilna cząsteczka działa następnie na sensor w komórkach T zwany LXRβ, co osłabia ich aktywność. Zarówno w hodowlach komórkowych, jak i u myszy, więcej MFAP2 wiązało się z wyższym poziomem 27‑HC w mikrośrodowisku guza, większą śmiercią i dysfunkcją komórek T oraz nasilonym wzrostem guza.
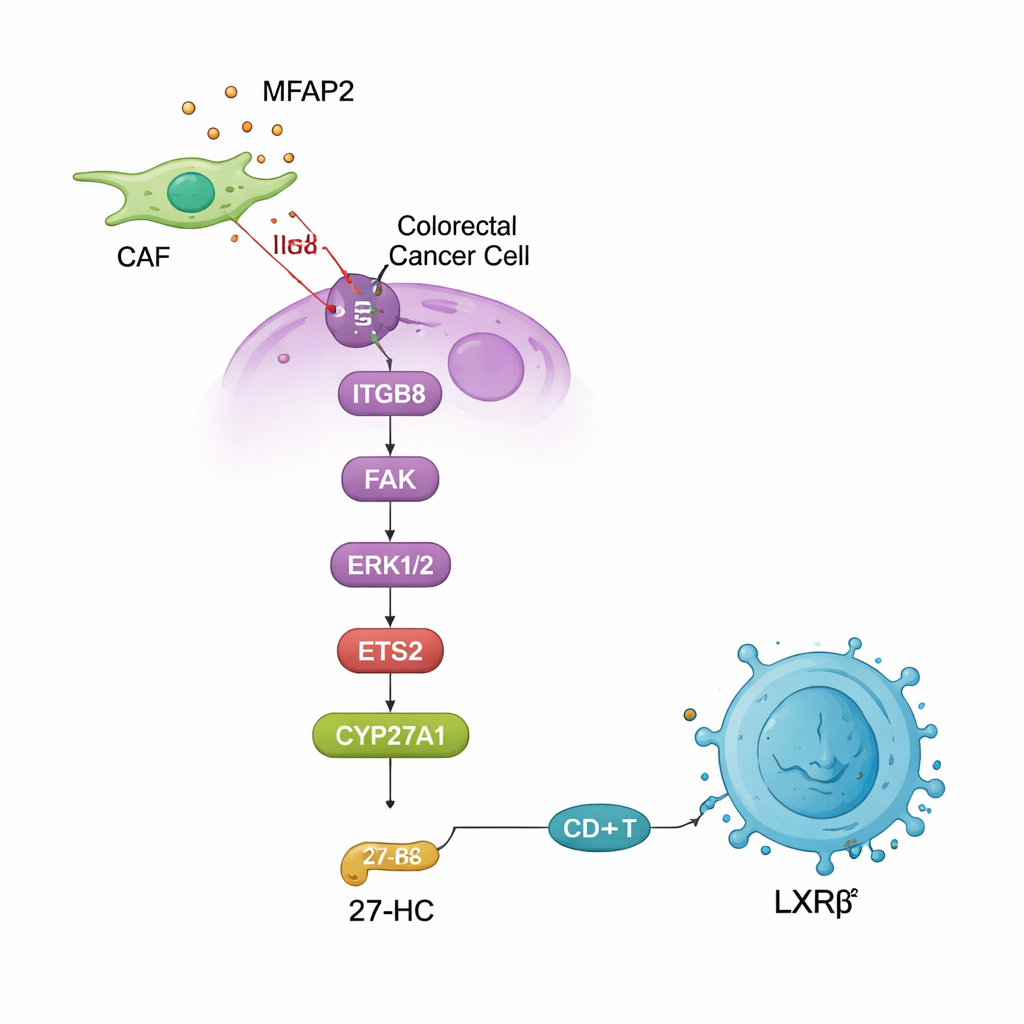
Łączenie metabolizmu, fibroblastów i ucieczki przed odpornością
Praca ta spina ze sobą kilka pozornie odrębnych aspektów biologii nowotworu: komórki wspierające otaczające guz, wewnętrzne sygnalizowanie w komórkach rakowych oraz sposób, w jaki guz przeprogramowuje metabolizm lipidów, aby unieszkodliwić obronę immunologiczną. Umieszczając MFAP2 na początku łańcucha biegnącego przez ITGB8, FAK, ERK1/2, ETS2 i CYP27A1, a kończącego się na 27‑HC wyłączającym komórki CD8 za pośrednictwem LXRβ, autorzy opisują kompletną trasę od sygnału fibroblastów do ucieczki przed odpornością. Co ważne, blokada MFAP2 lub ETS2 nie tylko spowalniała wzrost guza, lecz także przywracała naciekanie i funkcję komórek T u myszy, sugerując, że ten szlak może być celem terapeutycznym zwiększającym skuteczność immunoterapii i standardowych terapii.
Co to oznacza dla przyszłych terapii
Dla osób niebędących specjalistami główny wniosek jest taki, że jednymi z najbardziej szkodliwych uczestników procesu w raku jelita nie są wyłącznie komórki nowotworowe, lecz ich wspólnicy i chemiczne sygnały, które wysyłają. MFAP2 produkowane przez fibroblasty w guzie pomaga komórkom rakowym rosnąć i chroni je przed atakiem, osłabiając działanie własnych „zabójczych” komórek T organizmu poprzez sygnał oparty na cholesterolu. Ponieważ łańcuch napędzany przez MFAP2 ma wiele ogniw — na poziomie fibroblasta, powierzchni komórki nowotworowej, sygnalizacji wewnątrzkomórkowej i komórki T — oferuje kilka potencjalnych punktów docelowych dla nowych leków. Terapie przerywające ten szlak mogłyby zarówno spowolnić rozsiew nowotworu, jak i „obudzić” wyczerpane komórki T, poprawiając rokowanie pacjentów z rakiem jelita grubego.
Cytowanie: Zhang, X., Fei, Y., Xie, C. et al. Cancer-associated fibroblasts (CAFs) derived from MFAP2 promote CRC proliferation and metastasis while suppressing CD8+ T cell-mediated antitumor immunity. Cell Death Dis 17, 159 (2026). https://doi.org/10.1038/s41419-026-08413-w
Słowa kluczowe: rak jelita grubego, mikrośrodowisko guza, fibroblasty związane z nowotworem, uchylanie się przed układem odpornościowym, metabolizm cholesterolu