Clear Sky Science · pl
Przenoszenie mleczanu z niedotlenionych komórek nowotworowych promuje starzenie makrofagów i polaryzację M2 za pośrednictwem osi DNMT1‑NHE7, przyspieszając progresję raka endometrium
Dlaczego odcinanie nowotworu od tlenu ma znaczenie
Rak endometrium, który rozwija się z błony śluzowej macicy, staje się coraz częstszy na całym świecie. Wiele zaawansowanych guzów jest trudnych do leczenia, ponieważ nawracają, dają przerzuty lub opierają się standardowym terapiom. W tym badaniu przyjrzano się temu, co dzieje się w takich guzach, gdy cierpią na niedobór tlenu — powszechny objaw szybko rosnących nowotworów — i pokazano, jak prosty produkt uboczny, mleczan, może przeprogramować pobliskie komórki odpornościowe, aby wspierały rozwój raka zamiast go zwalczać.
Niski poziom tlenu zamienia guzy w fabryki mleczanu
W miarę mnożenia się komórek raka endometrium ich unaczynienie nie nadąża, tworząc obszary o niskim natlenieniu, czyli hipoksję. Komórki reagują, uruchamiając główny regulator HIF1A, który przestawia sposób pozyskiwania przez nie energii. Zamiast polegać głównie na wydajnych procesach energetycznych, komórki zwiększają glikolizę — szybką, lecz mało efektywną drogę, produkującą duże ilości mleczanu. Naukowcy przeanalizowali dane z setek pacjentów i stwierdzili, że wyższy poziom HIF1A szedł w parze ze zwiększoną aktywnością wielu genów związanych z glikolizą oraz transporterów wypompowujących mleczan z komórek nowotworowych. Pacjenci, których guzy miały więcej HIF1A, zwykle mieli gorsze rokowanie, co sugeruje, że ta zmiana metaboliczna łączy się z agresywnym przebiegiem choroby.
Jak odpady nowotworu przekształcają pomocne komórki odpornościowe
Makrofagi to komórki odpornościowe, które mogą albo atakować guzy, albo je wspierać, w zależności od swojego stanu. W pracy tej zespół wykazał, że pod wpływem hipoksji komórki raka endometrium wydzielają znacznie więcej mleczanu do otoczenia. Mleczan jest eksportowany przez transporter MCT3 na komórkach nowotworowych, a następnie importowany do makrofagów za pośrednictwem innego transportera, MCT1. Po wejściu do środka mleczan skłania makrofagi do odejścia od trybu obronnego w kierunku tzw. stanu M2, związanego z naprawą tkanek, tłumieniem zapalenia i, niestety, wspieraniem wzrostu guza. W eksperymentach laboratoryjnych makrofagi wystawione na płyn bogaty w mleczan wykazywały więcej markerów typu M2, a wydzielane przez nie czynniki z kolei zwiększały wzrost, migrację i inwazyjność komórek nowotworowych. 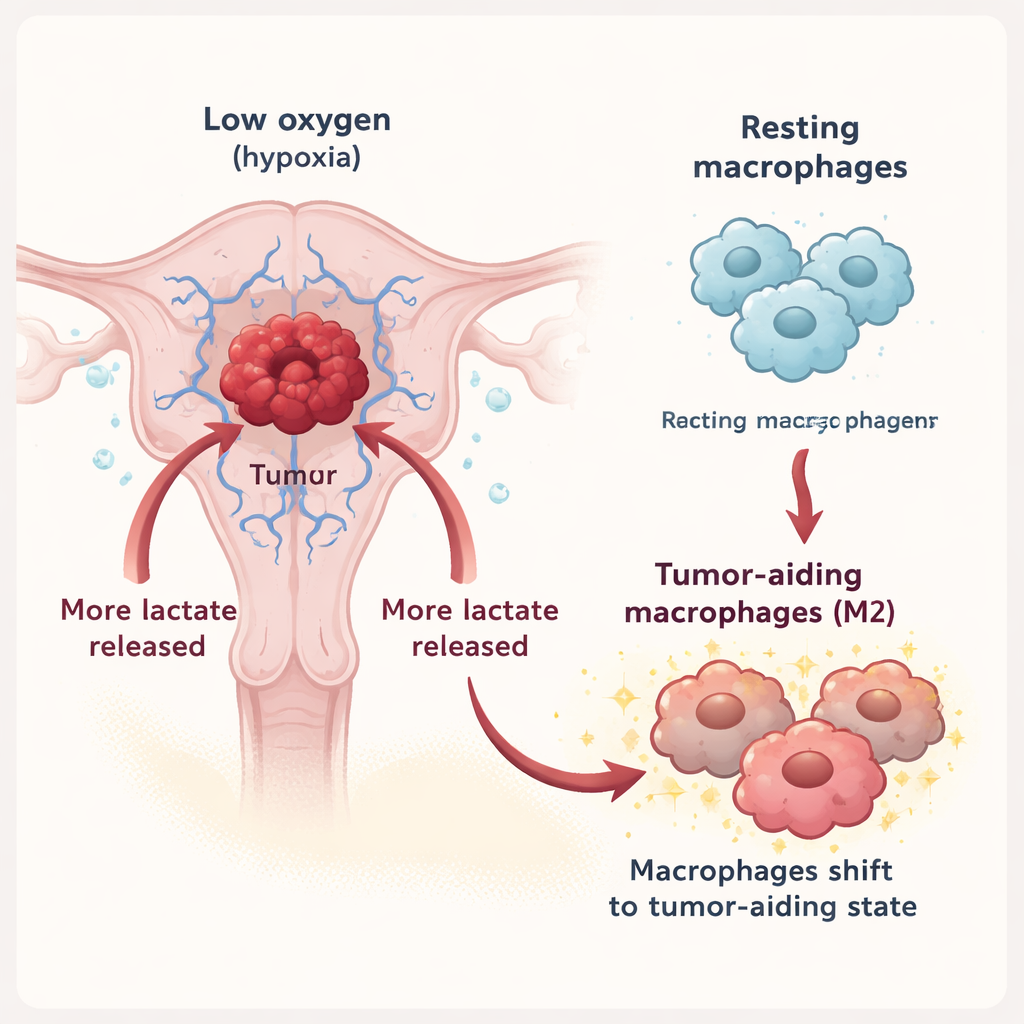
Przełącznik epigenetyczny wyciszający komórkowy „zawór pH”
Badanie posuwa się dalej, odkrywając molekularny przełącznik w makrofagach, który łączy mleczan pochodzący z guza z tym szkodliwym zachowaniem. Mleczan nie krąży bez działania — może modifikować białka histonowe w jądrze poprzez dodanie grupy zwanej lactylacją, co wpływa na to, które geny są włączane lub wyłączane. Naukowcy odkryli, że mleczan zwiększa konkretną modyfikację histonów w regionie kontrolnym genu DNMT1, podnosząc jego aktywność. DNMT1 to enzym dodający grupy metylowe do DNA, co może prowadzić do wyciszenia genów. Jednym z jego celów tu jest gen NHE7, kodujący białko pomagające kontrolować kwasowość w określonych przedziałach komórkowych. Gdy DNMT1 jest pobudzony, zwiększa metylację genu NHE7, obniżając jego ekspresję. Zredukowane NHE7 zaburza wewnętrzną równowagę pH i aktywuje szlak sygnałowy MAPK. Ten szlak z kolei popycha makrofagi w kierunku wspierającego guz stanu M2 oraz formy starzenia komórkowego zwanej senescencją, która utrwala je w przewlekle pro‑nowotworowym stanie.
Od molekularnej kaskady do szybciej rosnących guzów
Aby sprawdzić, czy ten łańcuch zdarzeń ma znaczenie in vivo, naukowcy stworzyli modele myszy, w których komórki ludzkiego raka endometrium były hodowane razem z makrofagami o cechach ludzkich. Gdy dostarczono dodatkowy mleczan, guzy były większe, zawierały więcej dzielących się komórek i miały więcej makrofagów typu M2 oraz senescentnych z wysokim DNMT1 i niskim NHE7. Co istotne, gdy makrofagi zostały zaprojektowane do nadprodukcji NHE7, osłabiło to efekt pobudzający guza przez mleczan: guzy były mniejsze, miały więcej komórek obumierających i zawierały mniej makrofagów typu M2 oraz mniej makrofagów senescentnych. Blokowanie enzymu DNMT1 lub szlaku MAPK również osłabiało zdolność mleczanu do przeprogramowywania makrofagów, wzmacniając koncepcję, że te cząsteczki tworzą powiązaną oś.
Przekształcanie sztuczek guza w cele terapeutyczne
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że guzy endometrium mogą wykorzystywać niski poziom tlenu i mleczan — kiedyś uważany za zwykły odpad komórkowy — do „prania mózgu” pobliskich komórek odpornościowych, aby pomagały one rakowi. Dzieje się to poprzez epigenetyczne przekaźnictwo: mleczan zwiększa DNMT1, który wycisza NHE7, a to aktywuje sygnalizację utrwalającą makrofagi w przyjaznym dla guza, postarzałym stanie. Zakłócenie dowolnego kroku w tym łańcuchu mleczan–DNMT1–NHE7–MAPK może przywrócić bardziej przeciw‑nowotworową aktywność układu odpornościowego i spowolnić wzrost raka. Praca ta wskazuje kierunki przyszłych terapii, które nie tylko bezpośrednio atakują komórki nowotworowe, ale też re‑edukują otaczające je komórki odpornościowe przejęte przez guz.
Cytowanie: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Słowa kluczowe: rak endometrium, mikrośrodowisko nowotworu, metabolizm mleczanu, polaryzacja makrofagów, regulacja epigenetyczna