Clear Sky Science · pl
Ponad metabolizmem: badanie regulacyjnych i terapeutycznych implikacji mleczanu i laktylacji w komórkowej śmierci regulowanej w nowotworach
Dlaczego „produkt odpadowy” ze spalania cukru ma znaczenie dla raka
Przez dekady mleczan — substancja powodująca pieczenie przemęczonych mięśni — był traktowany jako komórkowe śmieci. Niniejszy przegląd pokazuje, że w nowotworach mleczan wcale nie jest odpadem. Działa jako paliwo, sygnał chemiczny, a nawet przełącznik decydujący o życiu lub śmierci komórek nowotworowych. Zrozumienie tej ukrytej roli może otworzyć nowe sposoby skłonienia komórek nowotworowych do samobójczej autodestrukcji przy jednoczesnym oszczędzeniu tkanek zdrowych.
Skrót cukrowy, który przestawia komórki nowotworowe
Komórki nowotworowe są znane z „słodkiego zęba”. Nawet przy obfitości tlenu wolą szybko rozkładać glukozę do mleczanu zamiast całkowicie jej utleniać w mitochondriach — przesunięcie znane jako efekt Warburga. Strategia ta pozwala guzom szybko generować energię i składniki budulcowe. Powstający napływ mleczanu jest wypompowywany przez specjalne transportery, kształtując kwaśne, bogate w składniki odżywcze mikrośrodowisko guza, które wspiera wzrost i pomaga nowotworom przystosować się do stresu, takiego jak niedobór tlenu czy chemioterapia.
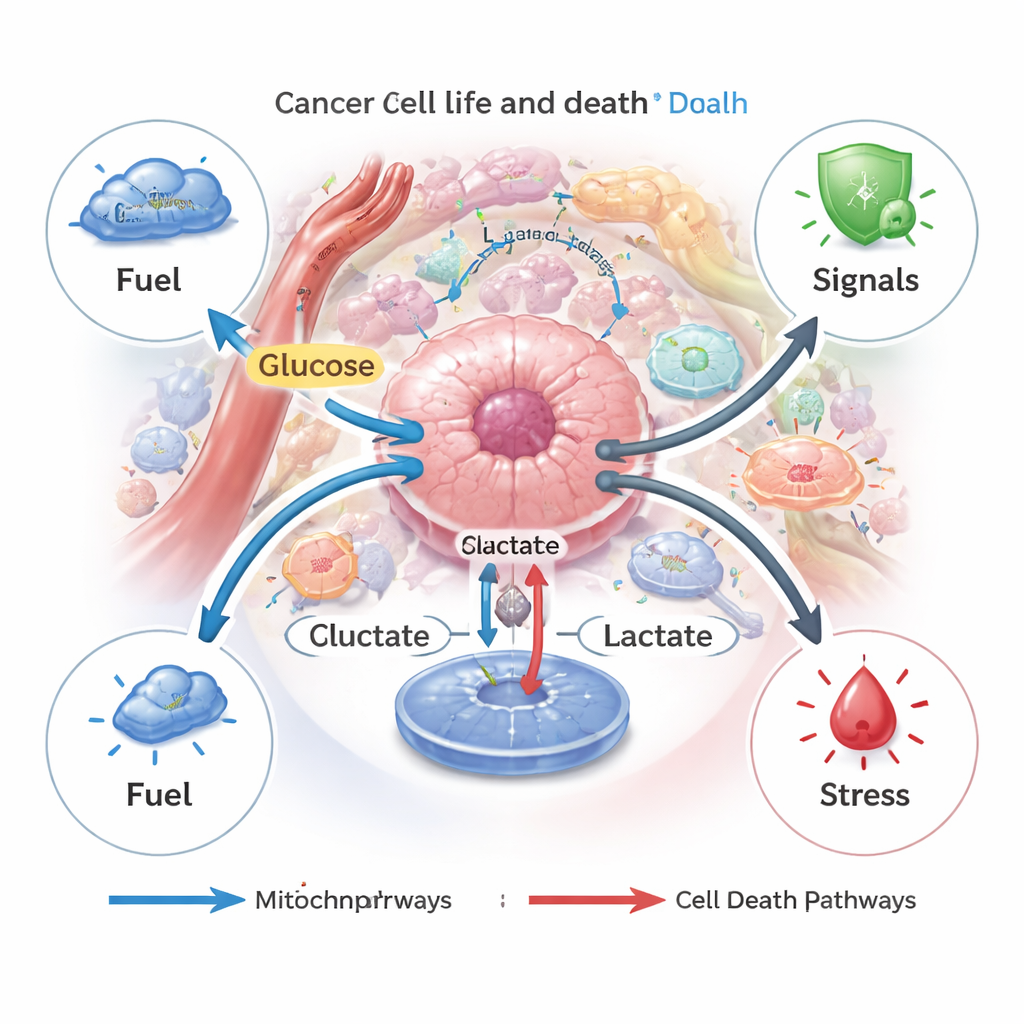
Mleczan jako regulator różnych rodzajów śmierci komórkowej
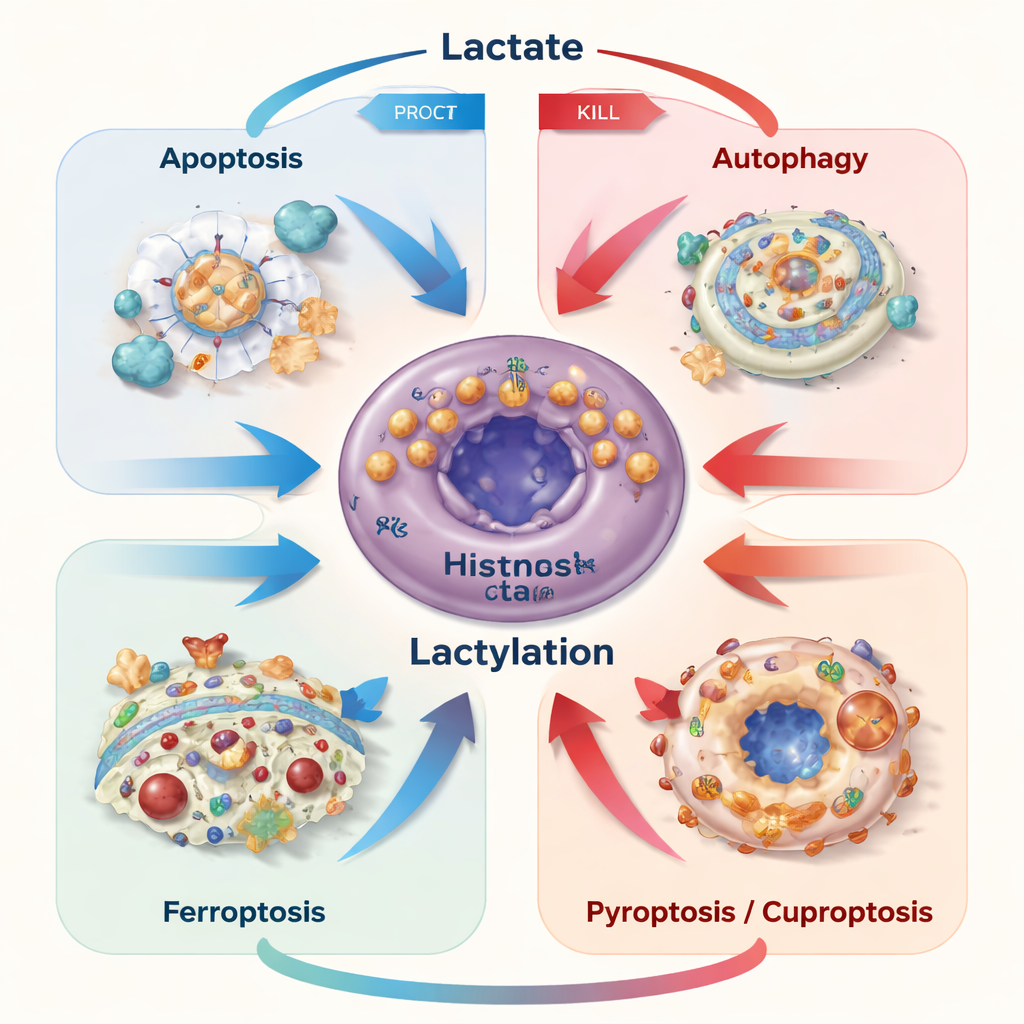
Śmierć komórek w organizmie zwykle jest ściśle kontrolowana, co pomaga usuwać uszkodzone lub niebezpieczne komórki. Komórki nowotworowe często unikają tych programów. Autorzy opisują, jak mleczan może zarówno blokować, jak i wywoływać kilka regulowanych szlaków śmierci — apoptozę (komórkowe „samobójstwo”), autofagię (samostrawienie), ferroptozę (uszkodzenie błony zależne od żelaza), pyroptoza (zapalenne pęknięcie) oraz cuproptozę (zapaść zależna od miedzi). Gdy komórki nowotworowe wytwarzają lub importują umiarkowane ilości mleczanu, używają go jako paliwa i sygnału przeżyciowego, włączając ścieżki chroniące przed chemioterapią, niedoborem składników odżywczych czy lekami celowanymi. Jednak gdy mleczan gromadzi się wewnątrz komórek, np. gdy jego eksport jest zablokowany, powstający stres kwasowy i uszkodzenie mitochondriów mogą przełączyć program i pchnąć komórki w kierunku apoptozy lub ferroptozy.
Laktylacja: gdy mleczan zapisuje się na białkach
Wyróżniające się ostatnie odkrycie pokazuje, że mleczan może zostać przekształcony w małą grupę chemiczną i przyłączony do reszt lizyn na białkach — modyfikację znaną jako laktylacja. Enzymy działają jako „pisarze” i „wymazywacze” tych znaczników, dekorując zarówno histony związane z DNA, jak i wiele innych białek. Te znaczniki zmieniają, które geny są włączane, jak zachowują się enzymy i jak stabilne są kluczowe regulatory. W nowotworach laktylacja precyzyjnie dostraja równowagę między przeżyciem a autodestrukcją. Może na przykład zwiększać poziom białek blokujących apoptozę, wzmacniać recykling przez autofagię, chronić komórki przed ferroptozą poprzez zacieśnienie kontroli żelaza i wzmocnienie przeciwutleniaczy, albo modyfikować nowe formy śmierci jak cuproptoza przez zmianę sposobu radzenia sobie z białkami wrażliwymi na miedź.
Dwukierunkowa rozmowa między metabolizmem a programami śmierci
Relacja nie jest jednostronna: szlaki śmierci komórkowej także przekształcają sposób, w jaki guzy wykorzystują cukry i produkują mleczan. Gdy mitochondria są uszkadzane podczas wczesnej apoptozy lub mitofagii (selektywnego usuwania mitochondriów), komórki często cofają się do szybkiej glikolizy, zwiększając wydzielanie mleczanu. Otaczające komórki wspierające, takie jak fibroblasty związane z nowotworem, mogą przechodzić podobne przemiany i stać się fabrykami mleczanu, które karmią pobliskie komórki guzowe. Inne typy śmierci, jak ferroptoza, mają tendencję do tłumienia glikolizy, a tym samym obniżania poziomu mleczanu. W efekcie powstaje dynamiczna pętla sprzężenia zwrotnego, w której metabolizm i mechanizmy śmierci nieustannie się dostosowują w miarę rozwoju guza i reakcji na leczenie.
Przekształcanie słabości w strategię terapeutyczną
Ponieważ mleczan i laktylacja mogą w zależności od kontekstu chronić lub zabijać komórki nowotworowe, autorzy twierdzą, że terapie muszą robić więcej niż tylko blokować produkcję mleczanu. Zamiast tego przyszłe leczenia mogą selektywnie przekierowywać przepływy mleczanu, modulować jego transportery lub celować w określone markery laktylacji, aby przechylić komórki nowotworowe na krawędź śmierci, jednocześnie przywracając energię komórkom odpornościowym przeciwnowotworowym, które są obecnie sparaliżowane przez kwaśne środowisko. Inteligentne systemy dostarczania leków i nanomedycyny reagujące na lokalne poziomy mleczanu lub pH pojawiają się jako sposoby zastosowania tej precyzji. Mówiąc prościej, przesłanie artykułu jest takie, że to, co kiedyś wyglądało jak metaboliczne odpady, jest w rzeczywistości potężnym pokrętłem kontrolującym los komórek nowotworowych — a nauka, jak nim właściwie pokręcić, może znacznie zwiększyć skuteczność istniejących terapii.
Cytowanie: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Słowa kluczowe: mleczan, laktylacja, śmierć komórek nowotworowych, metabolizm guza, ferroptoza