Clear Sky Science · pl
Skuteczność i bezpieczeństwo niskointensywnego i wysokointensywnego ultradźwięku ogniskowego w glejaku wielopostaciowym: przegląd systematyczny badań przedklinicznych i klinicznych
Przełamywanie obrony mózgu
Glejaki wielopostaciowe należą do najbardziej śmiertelnych nowotworów mózgu, częściowo dlatego, że ukrywają się za naturalną tarczą mózgu — barierą krew–mózg — która uniemożliwia dotarcie wielu leków. Ten artykuł przeglądowy bada nowy sposób docierania do tych guzów i ich zwalczania bez otwierania czaszki: precyzyjnie skupione fale dźwiękowe. Porównując dziesiątki eksperymentów na zwierzętach i wczesnych prób u ludzi, autorzy analizują, jak dwa rodzaje ultradźwięku ogniskowego mogą współdziałać, by skuteczniej dostarczać leki, a nawet wypalać fragmenty guza.
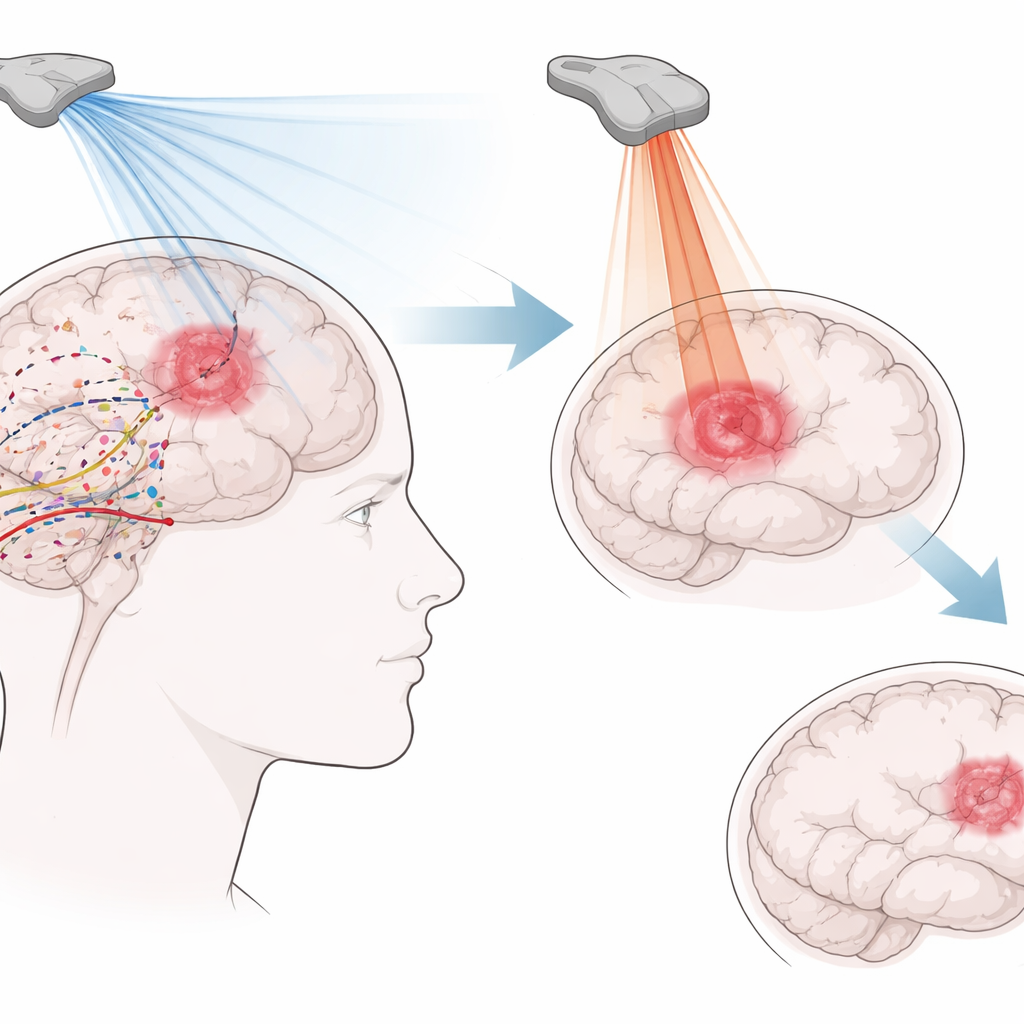
Dlaczego ten nowotwór mózgu jest tak trudny do leczenia
Standardowe leczenie glejaka łączy chirurgię, napromienianie i chemioterapię, jednak większość chorych przeżywa nieco ponad rok. Guz rozrasta się jak korzenie w obrębie mózgu, co sprawia, że całkowite usunięcie jest niemal niemożliwe. Jednocześnie bariera krew–mózg, która normalnie chroni mózg, blokuje dotarcie wielu leków przeciwnowotworowych do pojedynczych komórek pozostających po operacji. Otoczenie guza jest też nieprzyjazne dla układu odpornościowego — jest tam mało limfocytów T zdolnych zwalczać nowotwór, a wiele komórek układu odpornościowego wręcz sprzyja jego wzrostowi. Te nakładające się przeszkody tłumaczą, dlaczego nawet silne nowe leki często zawodzą, gdy mają dotrzeć do mózgu.
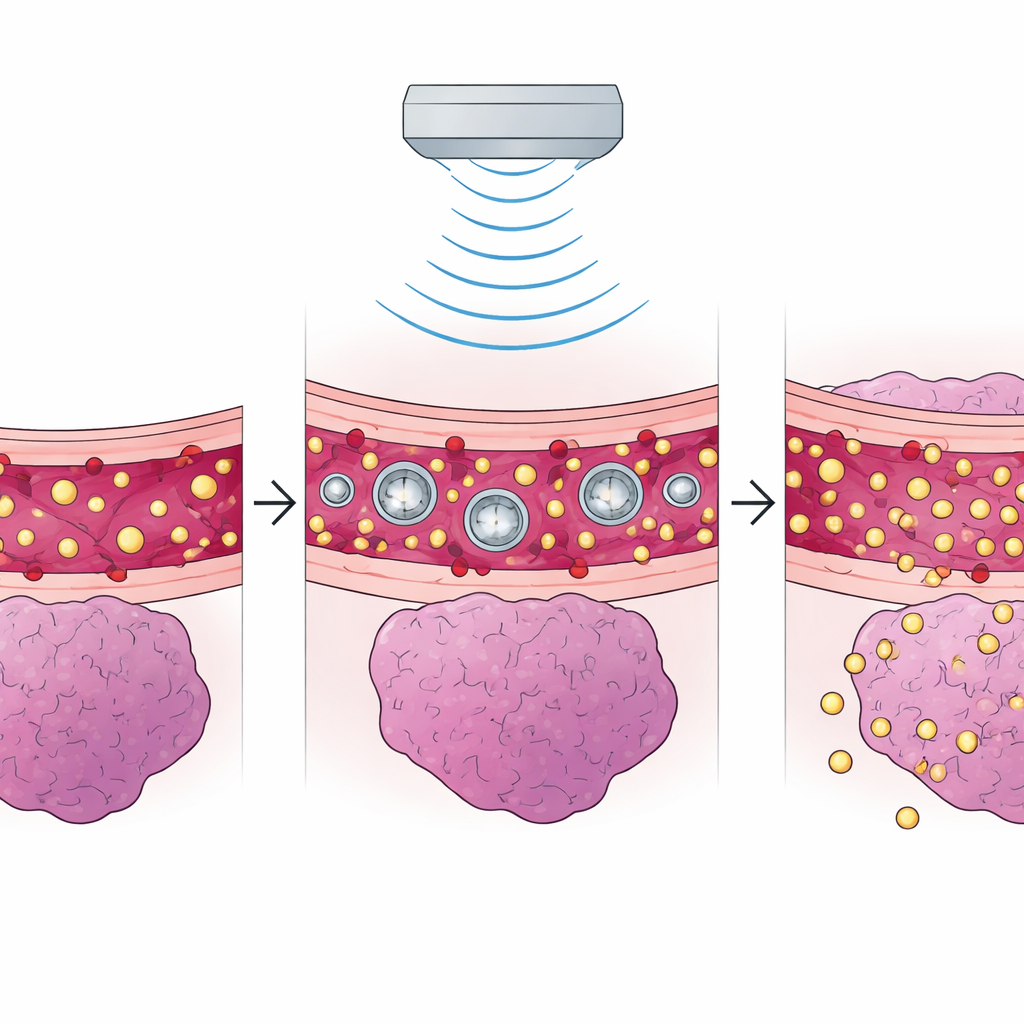
Delikatny dźwięk, który otwiera bramę mózgu
Niskointensywny ultradźwięk ogniskowy wykorzystuje drobne pęcherzyki gazu wstrzyknięte do krwiobiegu. Gdy przechodzą przez nie fale dźwiękowe, pęcherzyki delikatnie wibrują i rozchylają ściśle zamknięte komórki wyściełające naczynia mózgowe. W badaniach na zwierzętach takie tymczasowe „poluzowanie” pozwalało na znacznie większe przenikanie chemioterapeutyków, terapii immunologicznych, a nawet cząstek niosących geny do guzów. W wielu eksperymentach obserwowano zmniejszenie guzów i wydłużenie przeżycia z około trzech–czterech tygodni do sześciu–jednastu tygodni. Wczesne próby kliniczne potwierdzają te wzorce: stosowanie tej metody razem ze standardowymi lekami, takimi jak temozolomid czy karboplatyna, niezawodnie otwierało barierę, zwiększało stężenia leków w leczonych obszarach mózgu i dawało okresy wolne od progresji trwające kilka miesięcy — w jednej małej grupie wszyscy pacjenci byli żywi po roku.
Zmiana dźwięku w precyzyjne gorące ostrze
Wysokointensywny ultradźwięk ogniskowy działa inaczej. Tutaj silniejsze fale dźwiękowe są skupione na małym celu, ogrzewając tkankę na tyle, by bezpośrednio zniszczyć komórki nowotworowe. W modelach zwierzęcych łączenie tego silniejszego ultradźwięku z cząstkami niosącymi leki lub środkami kontrastowymi często hamowało wzrost guza o około 70% i poprawiało przeżycie, bez uszkodzeń pobliskich narządów. U ludzi wyniki jak dotąd były bardziej umiarkowane. Jeden starannie monitorowany przypadek zniszczył jedynie około jednej dziesiątej objętości guza, a inna wczesna próba osiągnęła terapeutyczne temperatury bez widocznego zmniejszenia guza. Tendencja czaszki do załamywania i absorbowania energii ultradźwiękowej oraz dyfuzyjne rozprzestrzenianie się komórek glejaka poza wyraźnie odgraniczony guz sprawiają, że metoda oparta na cieple jest technicznie wymagająca.
Bezpieczeństwo, ograniczenia i dalsze kroki
W przeglądzie 40 badań oba podejścia wydawały się wyjątkowo bezpieczne przy ostrożnym stosowaniu. Leczenia niskointensywne powodowały głównie łagodne, krótkotrwałe efekty, takie jak bóle głowy, drobne punkcikowe krwawienia widoczne jedynie w badaniach obrazowych czy przejściowe odczucia mrowienia lub ciepła. Bariera krew–mózg zazwyczaj zamykała się ponownie w ciągu doby i nie zgłaszano trwałych uszkodzeń mózgu. Leczenia wysokointensywne powodowały krótkotrwałe uczucie ciepła lub dyskomfort, ale jak dotąd nie odnotowano poważnych krwawień ani trwałych deficytów u niewielkiej liczby leczonych pacjentów. Mimo to baza dowodowa jest nierówna: większość badań na zwierzętach nie spełniała pełnych standardów zaślepienia czy randomizacji, a większość danych klinicznych pochodzi z małych, nierandomizowanych prób prowadzonych w zamożnych krajach, co utrudnia wyciąganie pewnych wniosków.
Co to oznacza dla pacjentów i rodzin
Autorzy wnioskują, że niskointensywny i wysokointensywny ultradźwięk ogniskowy to obiecujące, uzupełniające się narzędzia, a nie samodzielne terapie. Niskointensywny ultradźwięk jest najbliżej zastosowań klinicznych: może wielokrotnie i odwracalnie otwierać „bramę” mózgu, dzięki czemu więcej leków i komórek odpornościowych dociera do ukrytych ognisk guza. Wysokointensywny ultradźwięk może pewnego dnia pomóc wypalić wyraźnie ograniczone rdzenie guza, zwłaszcza w połączeniu z lepszymi metodami dostarczania leków. Jednak żadna z metod nie jest jeszcze gotowa do zastąpienia chirurgii, radioterapii czy chemioterapii. Wciąż potrzebne są duże, starannie zaprojektowane badania — najlepiej wieloośrodkowe i z ustandaryzowanymi ustawieniami leczenia — aby udowodnić, czy te strategie oparte na dźwięku mogą istotnie wydłużyć życie i zachować jego jakość u osób zmagających się z glejakiem wielopostaciowym.
Cytowanie: Alrashidi, M., Ferro, F., Almohammadi, A. et al. Efficacy and safety of low- and high-intensity focused ultrasound in glioblastoma: a systematic review of preclinical and clinical studies. Br J Cancer 134, 977–995 (2026). https://doi.org/10.1038/s41416-025-03325-6
Słowa kluczowe: glejak wielopostaciowy, ultradźwięk ogniskowy, bariera krew–mózg</keyword-barrier> <keyword>terapia guzów mózgu, onkologia nieinwazyjna