Clear Sky Science · pl
Kontext immunologiczny guza i ucieczka przed układem odpornościowym w sporadycznych i związanych z zespołem Lyncha rakach jelita grubego z niestabilnością mikrosatelitową
Dlaczego to ma znaczenie dla pacjentów onkologicznych
Immunoterapia zmieniła perspektywy dla wielu osób z rakiem jelita grubego, ale nie wszyscy odnoszą korzyść. W tym badaniu postawiono kluczowe pytanie: dlaczego niektóre guzy, które teoretycznie powinny być dobrze widoczne dla układu odpornościowego, nadal potrafią umknąć jego kontroli? Porównując dwa typy genetycznie niestabilnych nowotworów jelita — związane z dziedzicznym zespołem Lyncha oraz powstające sporadycznie — badacze uwidocznili ważne różnice w tym, jak komórki odpornościowe otaczają, atakują, a czasem chronią te guzy.
Dwie drogi do tego samego rodzaju guza
Raki jelita grubego z niestabilnością mikrosatelitową (MSI) zawierają dużą liczbę błędów DNA, które prowadzą do powstawania nieprawidłowych białek mogących działać jak „flagii” dla układu odpornościowego. Guzy te mogą powstawać wskutek dziedzicznych defektów naprawy DNA (zespół Lyncha) albo w wyniku zmian występujących tylko w samym guzie (sporadyczne nowotwory MSI). Choć oba typy podobnie wyglądają pod mikroskopem, ich immunologiczne otoczenie — a być może także reakcje na leczenie — nie są identyczne. Zespół zebrał 43 raki jelita grubego MSI pochodzące od fińskich pacjentów, obejmujące przypadki związane z zespołem Lyncha i przypadki sporadyczne, i przeanalizował je za pomocą barwień tkanek, sekwencjonowania całego genomu oraz sekwencjonowania RNA, by szczegółowo zmapować, które komórki odpornościowe były obecne i jak guzy unikały zniszczenia.
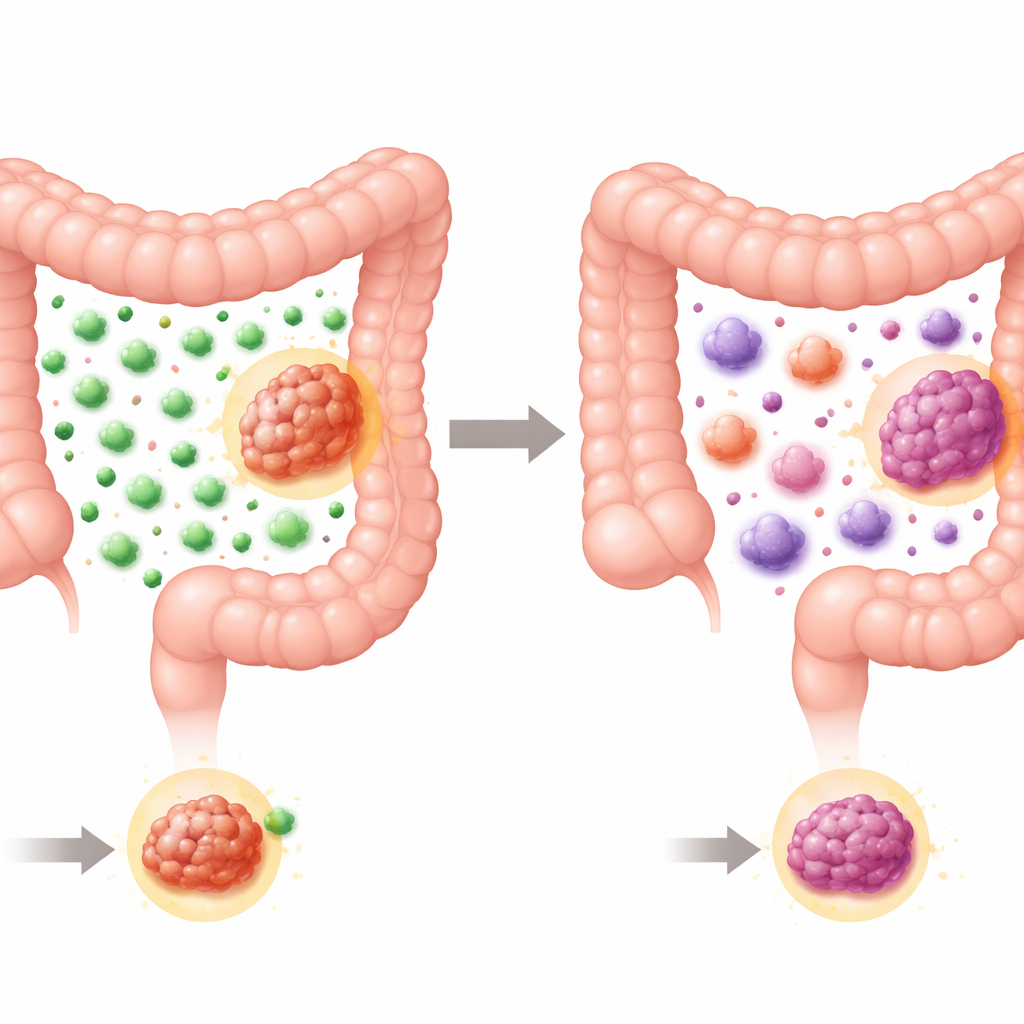
Ile komórek odpornościowych się pojawia
Badacze najpierw skupili się na komórkach T, wyspecjalizowanych „egzekutorach” układu odpornościowego. Mierzyli ustalony wskaźnik komórek odpornościowych, który łączy gęstość ogólnej populacji i komórek T cytotoksycznych w centrum guza i na jego granicy inwazyjnej. Jak można było oczekiwać, guzy MSI ogólnie miały wyższe wyniki niż typowe raki jelita grubego, co odzwierciedla ich większą zdolność do przyciągania limfocytów T. Jednak w obrębie grupy MSI wyłonił się wyraźny wzorzec: każdy guz związany z zespołem Lyncha miał wysoki wynik immunologiczny, podczas gdy guzy sporadyczne rozdzieliły się mniej więcej po połowie między wysokie a niskie wyniki. Innymi słowy, nowotwory dziedziczne MSI niemal zawsze przyciągały silne „armie” limfocytów T, podczas gdy nowotwory sporadyczne były bardziej zróżnicowane, niektóre wyglądając względnie „zimno” dla układu odpornościowego.
„Przyjazne” i „nieprzyjazne” komórki wspomagające
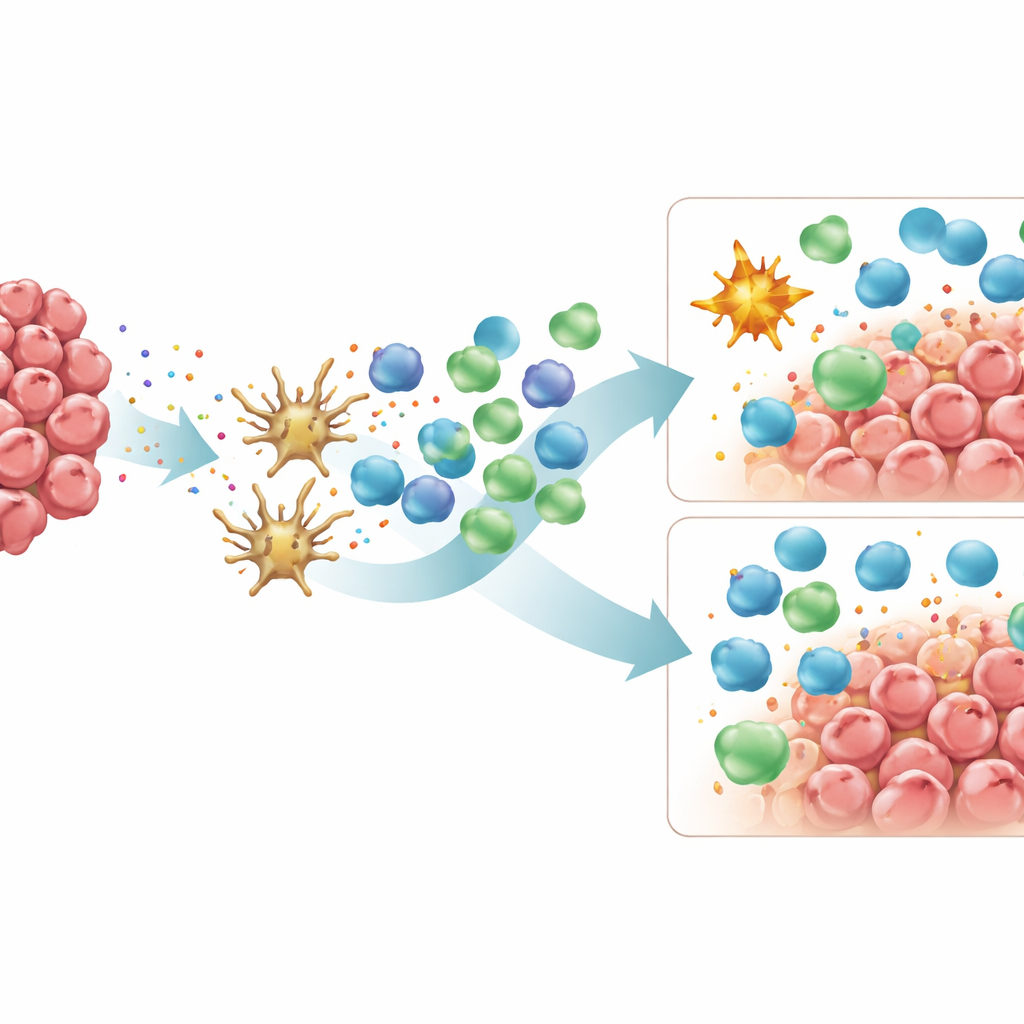
Następnie badanie skupiło się na komórkach mieloidalnych — wrodzonych komórkach odpornościowych, takich jak makrofagi i neutrofile, które mogą albo pomagać limfocytom T w walce z nowotworem, albo paradoksalnie go chronić. Przy użyciu multiplexowego barwienia oznaczającego kilka białek jednocześnie, autorzy sklasyfikowali makrofagi na dwa szerokie typy: komórki typu M1, które wspierają stan zapalny i zabijanie komórek nowotworowych, oraz komórki typu M2, które mają raczej działanie przeciwzapalne, wspomagające gojenie i często sprzyjające rozwojowi guza. Zarówno guzy MSI związane z Lynchem, jak i sporadyczne zawierały wiele komórek mieloidalnych, ale to guzy sporadyczne wyróżniały się większą liczbą makrofagów typu M2, szczególnie w tkance podtrzymującej na granicy inwazyjnej guza. W tym obszarze komórki typu M2 nawet przewyższały liczebnie M1 w guzach sporadycznych. Wśród grupy sporadycznej te guzy, które miały wysoki wynik limfocytów T, także wykazywały więcej makrofagów typu M1, podczas gdy poziomy M2 pozostawały wysokie niezależnie — co sugeruje, że równowaga między tymi dwoma rodzajami makrofagów może decydować o tym, czy limfocyty T zdołają przeprowadzić skuteczny atak.
Genetyczne sztuczki i różnorodność guza
Aby zrozumieć, dlaczego niektóre guzy MSI unikają układu odpornościowego, badacze przeanalizowali zmiany genetyczne wpływające na prezentację antygenów oraz na mechanizmy „hamujące” odpowiedź immunologiczną. Zarówno guzy MSI związane z Lynchem, jak i sporadyczne często miały mutacje w kluczowych elementach aparatu prezentacji antygenów, lecz różnice między grupami były jedynie subtelne. Bardziej wyraźne były różnice w sygnałach „checkpoint” immunologicznych. Guzy sporadyczne wykazywały wyższe poziomy PD-L2 i CD40L — cząsteczek, które mogą kształtować zachowanie komórek odpornościowych i które coraz częściej są badane jako cele terapeutyczne w połączeniu z istniejącymi inhibitorami punktów kontrolnych. Zespół zmierzył także, ile potencjalnych neoantygenów nosił każdy guz oraz jak genetycznie jednorodne lub zróżnicowane (klonalne kontra heterogenne) były guzy. Co zaskakujące, wyższe przewidywane obciążenie neoantygenami nie przekładało się na większą liczbę limfocytów T. Zamiast tego guzy bardziej genetycznie zróżnicowane — zwłaszcza sporadyczne MSI — miały tendencję do noszenia więcej neoantygenów, ale jednocześnie wykazywały wzorce, takie jak zmniejszona obecność neutrofili, co sugerowało, że układ odpornościowy nie w pełni wykorzystuje te cele.
Co to znaczy dla przyszłych terapii
Podsumowując, badanie przedstawia raki jelita grubego MSI związane z zespołem Lyncha jako konsekwentnie „gorące” guzy bogate w limfocyty T, podczas gdy guzy sporadyczne MSI tworzą bardziej mieszaną grupę — niektóre są silnie nacieczone, inne zaś osłaniane przez immunosupresyjne makrofagi i wyższe ekspresje niektórych cząsteczek punktów kontrolnych. Równocześnie guzy sporadyczne częściej wykazują wysoką różnorodność genetyczną i duże obciążenie neoantygenami rozproszonymi w różnych subklonach komórek nowotworowych — wzorzec, który wcześniejsze badania sugerują, może osłabiać skuteczność odpowiedzi limfocytów T. Dla pacjentów wnioski te pomagają wyjaśnić, dlaczego nie wszystkie raki MSI reagują jednakowo na immunoterapię, mimo wspólnej wysokiej częstości mutacji. Wskazują także na nowe strategie, takie jak leki reprogramujące lub depletujące makrofagi typu M2 albo terapie ukierunkowane na dodatkowe punkty kontrolne, jak PD-L2 i CD40L, które mogą być szczególnie istotne w guzach sporadycznych MSI. Lepsze dopasowanie podejścia terapeutycznego do unikalnego immunologicznego krajobrazu każdego guza może pozwolić klinicystom poprawić i spersonalizować efekty immunoterapii w raku jelita grubego.
Cytowanie: Martin, S., Elomaa, H., Väyrynen, J.P. et al. Tumour immune contexture and immune evasion in sporadic and Lynch syndrome-associated microsatellite unstable colorectal cancers. Br J Cancer 134, 1019–1030 (2026). https://doi.org/10.1038/s41416-025-03302-z
Słowa kluczowe: rak jelita grubego z niestabilnością mikrosatelitową, zespół Lyncha, mikrośrodowisko immunologiczne guza, makrofagi związane z guzem, immunoterapia nowotworów