Clear Sky Science · pl
Immunosupresyjne pejzaże mikrośrodowiska immunologicznego w raku żołądka z wysoką ekspresją VISTA
Dlaczego obrona organizmu czasem zawodzi wobec raka żołądka
Współczesne terapie przeciwnowotworowe coraz częściej polegają na pobudzeniu układu odpornościowego, aby mógł zaatakować guzy. Mimo to u wielu chorych z zaawansowanym rakiem żołądka te silne leki słabo działają lub przestają działać. W badaniu tym przyjrzano się jednej ważnej przyczynie: cząsteczce hamującej o nazwie VISTA, która przebudowuje lokalne otoczenie guza, zamieniając komórki odpornościowe z bojowników w obserwatorów, a czasem nawet sojuszników nowotworu. Zrozumienie tego ukrytego przełącznika kontroli może otworzyć drogę do bardziej precyzyjnej i skutecznej immunoterapii.
Ukryty hamulec w sąsiedztwie guza
Autorzy skoncentrowali się na VISTA, białku występującym głównie na niektórych komórkach białokrwinkowych zlokalizowanych w obrębie i wokół guzów. VISTA działa jak sygnał stop dla reakcji immunologicznych. Podczas gdy inne hamulce, takie jak PD-1 i PD-L1, są już celem zatwierdzonych leków, rola VISTY w raku żołądka była niejasna. Aby to zbadać, zespół przeanalizował tkanki od 172 pacjentów, wykorzystując zaawansowane wielobarwne barwienia do jednoczesnego mapowania wielu typów komórek. W mniejszych zestawach próbek zastosowano także sekwencjonowanie RNA pojedynczych komórek i transkryptomikę przestrzenną, aby sprawdzić, które komórki niosą VISTĘ, co te komórki robią i gdzie dokładnie się znajdują w krajobrazie guza. 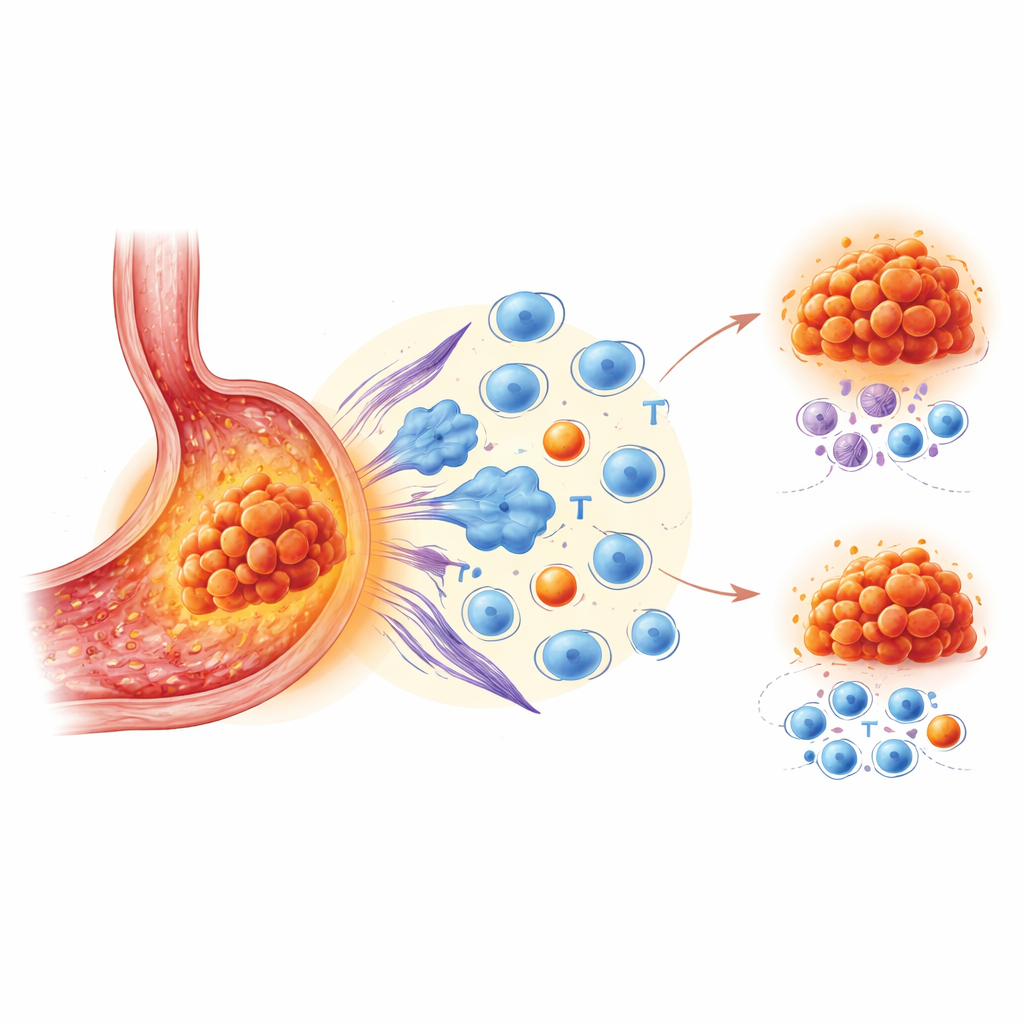
Gdy VISTA jest wysoka, układ odpornościowy jest stłumiony
Porównując guzy o wysokim i niskim poziomie VISTY, badacze zaobserwowali spójny wzorzec. Nowotwory bogate w VISTĘ były otoczone komórkami odpornościowymi, ale nie takimi, które prowadzą silny atak. Zamiast tego występowało nagromadzenie wyczerpanych cytotoksycznych limfocytów T, które utraciły swoją skuteczność, komórek T regulatorowych tłumiących odpowiedzi immunologiczne, tworzących blizny komórek podporowych zwanych fibroblastami oraz makrofagów przesuniętych w stronę stanu sprzyjającego nowotworowi. Pacjenci, których obszary guza zawierały więcej VISTY, mieli krótszy czas do progresji choroby po immunoterapii, nawet po uwzględnieniu innych czynników klinicznych. Innymi słowy, sąsiedztwo o dużej zawartości VISTY wyglądało mikroskopowo na aktywne, lecz funkcjonowało jako „strefa immunologicznie cicha” lub supresyjna.
Makrofagi jako kluczowi pośrednicy
Wnikliwsze analizy skupiły się na monocytach i makrofagach — komórkach odpornościowych, które mogą albo pożerać komórki nowotworowe, albo je chronić. Na poziomie pojedynczych komórek gen kodujący VISTĘ (oznaczany jako VSIR) był szczególnie aktywny w kilku podgrupach makrofagów, zwłaszcza tych, które efektywnie prezentują fragmenty białek nowotworowych na swojej powierzchni, oraz tych o cechach tzw. makrofagów M2, związanych z gojeniem ran. Przy użyciu obliczeniowej osi czasu rozwoju komórek zespół zaobserwował włączenie VISTY w miarę przechodzenia komórek od wczesnych monocytów do bardziej dojrzałych makrofagów gromadzących się wokół komórek nowotworowych. Mapowanie przestrzenne potwierdziło, że makrofagi pozytywne na VISTĘ zazwyczaj lokalizowały się blisko komórek nowotworowych, a pacjenci, których guzy miały więcej takich komórek właśnie w tych miejscach, mieli gorsze wyniki po terapii inhibitorami punktów kontrolnych. 
Jak komórki z VISTĄ osłabiają limfocyty T
Badanie zbadało także, jak makrofagi niosące VISTĘ komunikują się z limfocytami T. Mapy komunikacji zbudowane na danych o ekspresji genów sugerowały, że te makrofagi często kontaktują się z limfocytami T poprzez pary molekularne, takie jak LGALS9 i PTPRC, oraz poprzez cząsteczki zaangażowane w prezentowanie fragmentów guza limfocytom T. Stała prezentacja może z biegiem czasu przesunąć limfocyty T ze stanu wczesnej aktywacji w stan przewlekłego pobudzenia i wyczerpania, charakteryzujący się wieloma sygnałami hamującymi na ich powierzchni. W próbkach, w których makrofagi wykazywały wyższą ekspresję VSIR, obserwowano więcej komórek T regulatorowych i więcej wyczerpanych cytotoksycznych limfocytów T, co wzmacnia hipotezę, że makrofagi z VISTĄ przyczyniają się do „wypalenia” odporności, zamiast do ostrych, efektywnych ataków.
Co to może oznaczać dla przyszłych terapii
Całościowo praca przedstawia VISTĘ jako centralny przełącznik, który pomaga guzom żołądka zbudować immunosupresyjną niszę, zwłaszcza poprzez wyspecjalizowane makrofagi, które jednocześnie prezentują materiał nowotworowy i wysyłają hamujące sygnały do limfocytów T. Dla pacjentów sugeruje to, że wysoka ekspresja VISTY oznacza formę oporności na obecne leki ukierunkowane jedynie na PD‑1 lub PD‑L1. Blokowanie VISTY — być może w połączeniu z istniejącymi inhibitorami punktów kontrolnych — mogłoby ożywić limfocyty T i przechylić równowagę z powrotem na kontrolę guza. Choć potrzebne są dalsze badania laboratoryjne i kliniczne, to badanie daje mapę drogową do projektowania nowych kombinacji terapeutycznych oraz do identyfikowania pacjentów, którzy najprawdopodobniej skorzystają z takich podejść.
Cytowanie: Luo, Y., Peng, H., Yao, Q. et al. Immunosuppressive immune microenvironment landscapes in VISTA-high gastric cancer. Br J Cancer 134, 1066–1079 (2026). https://doi.org/10.1038/s41416-025-03290-0
Słowa kluczowe: rak żołądka, mikrośrodowisko guza, punkt kontrolny układu odpornościowego, makrofagi, wyczerpanie limfocytów T