Clear Sky Science · pl
Spektrum i funkcje kanałów jonowych oraz transporterów w osteoklastach
Dlaczego nasze kości potrzebują maleńkich strażników
Nasze kości wydają się solidne i niezmienne, ale są nieustannie niszczone i odbudowywane. Specjalne komórki zwane osteoklastami pełnią rolę ekipy rozbiórkowej, rozpuszczając starą tkankę kostną, by mogła powstać nowa. Ten artykuł przeglądowy bada ukrytą obsadę mikroskopijnych „strażników” — białek kanałowych i transporterów — które umożliwiają przemieszczenie naładowanych atomów i substancji odżywczych do wnętrza i na zewnątrz osteoklastów. Zrozumienie, jak te maleńkie bramki kontrolują rozkład kości, ma pomóc naukowcom w projektowaniu lepszych terapii przeciw osteoporozie i innym chorobom kości.
Jak komórki „jedzące kość” wykonują swoją pracę
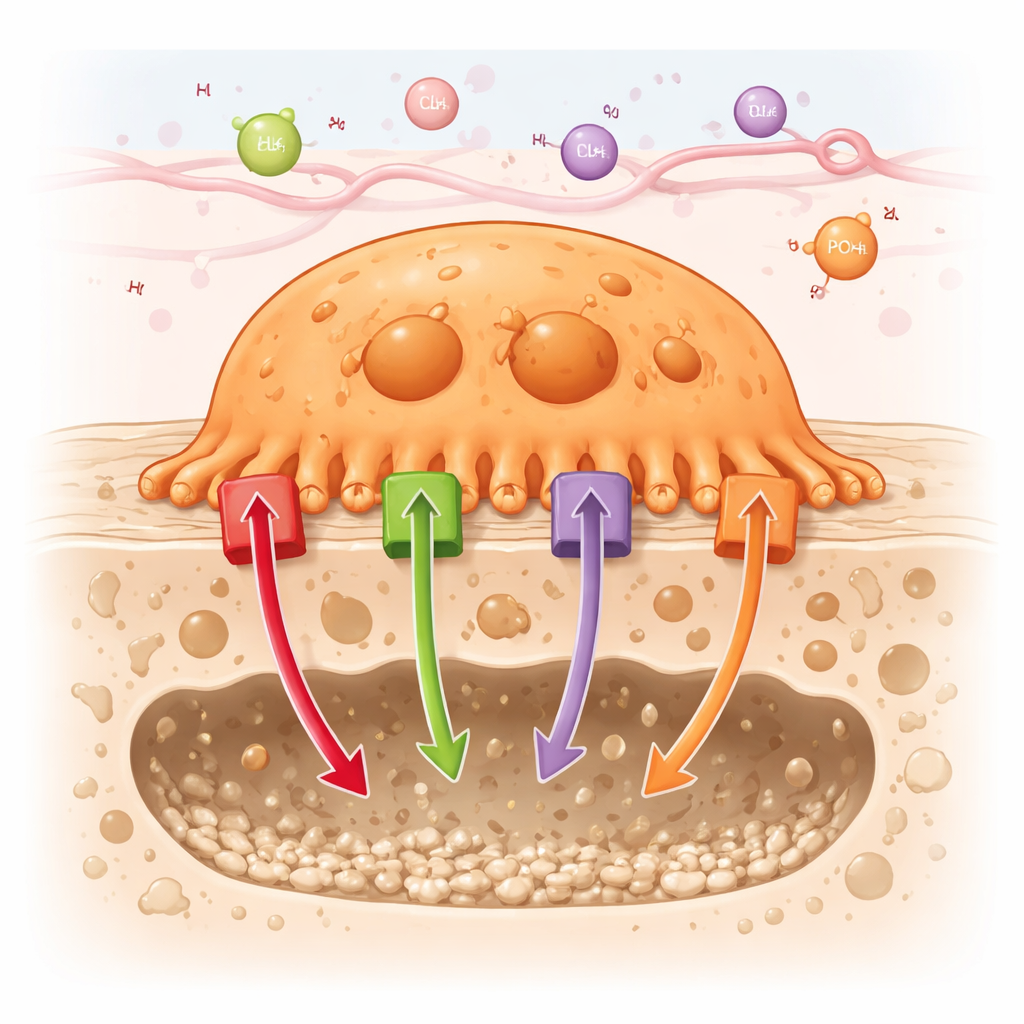
Osteoklasty działają, przyczepiając się ciasno do powierzchni kości i tworząc odizolowaną przestrzeń, w której bezpiecznie rozpuszczają minerały i trawią białka. Aby ta miniaturowa „komora trawienia” stała się bardzo kwaśna, osteoklasty pompują dużą liczbę protonów (jonów wodorowych) do tej przestrzeni. Równocześnie transportują inne jony — takie jak chlorki, wapń i fosforany — przez błony komórkowe i do wnętrza organelli. Artykuł omawia około 90 różnych kanałów i transporterów występujących w osteoklastach i grupuje je w sześć rodzin, w tym pompy napędzane energią (ATPazy), kanały kationowe i anionowe, transportery sprzężone, nośniki składników odżywczych oraz transportery ABC (wiązanie ATP).
Kwas, sól i energia: podstawowy mechanizm
Dwa systemy białkowe wyróżniają się jako kluczowe dla resorpcji kości. Po pierwsze, wakuolowe pompy protonowe znane jako V-ATPazy aktywnie wtłaczają protony do kieszonki resorpcyjnej, powodując zakwaszenie wystarczające do rozpuszczenia minerału kostnego i aktywacji enzymów trawiących białka. Konkretne podjednostki V-ATPazy, takie jak a3, d2 oraz kilka składników V1, są skoncentrowane przy pofalowanej granicy osteoklastu i w lizosomach; wady genetyczne tych podjednostek mogą osłabiać kość albo powodować nieprawidłowe jej zgrubienie. Po drugie, wymieniacz chlor‑proton o nazwie ClC-7, współdziałający z białkiem OSTM1, dostarcza jony chlorkowe do tej samej przestrzeni. To wyrównuje ładunek elektryczny i pozwala na ciągłe pompowanie protonów. Mutacje w ClC-7 u ludzi i myszy powodują osteopetrozę — stan charakteryzujący się nadmiernie gęstymi, lecz kruchymi kośćmi — co ilustruje, jak istotny jest prawidłowy przepływ jonów dla zdrowia szkieletu.
Wapń, fosfor i inni gracze wspierający
Ponad produkcją kwasu, osteoklasty polegają na precyzyjnej kontroli wapnia i fosforu. Sieć kanałów i pomp wapniowych w błonie komórkowej, retikulum endoplazmatycznym, lizosomach i mitochondriach generuje rytmiczne „oscylacje” wapniowe, które uruchamiają kluczowe geny zaangażowane w formowanie i fuzję osteoklastów. Transportery przy pofalowanej granicy i po przeciwnej stronie komórki przemieszczają wapń i fosfor z rozpuszczonej kości, albo recyklingując je wewnątrz komórki, albo przekazując z powrotem do krwiobiegu. Inne metale i minerały — takie jak mangan, magnez, cynk, miedź i żelazo — również są kontrolowane przez wyspecjalizowane transportery i wpływają na intensywność resorpcji kości. Na przykład żelazo i pewne formy śmierci komórkowej związane z żelazem mogą zwiększać lub zmniejszać aktywność osteoklastów, podczas gdy transportery cynku mają tendencję do hamowania nadmiernej utraty kości.
Ruch drogowy wewnątrz komórki
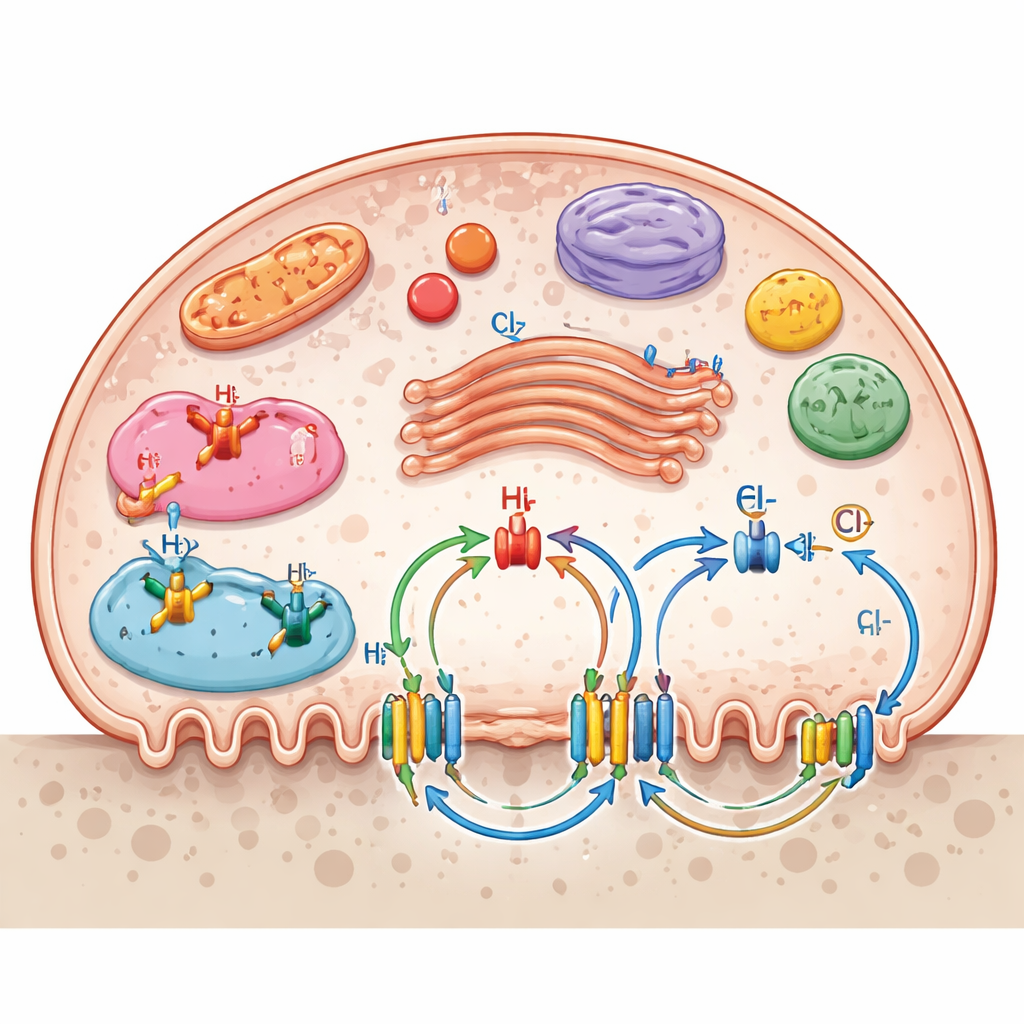
Kanały jonowe nie ograniczają się do błony zewnętrznej. Wiele z nich znajduje się na wewnętrznych przegrodkach, takich jak lizosomy, endosomy, aparat Golgiego i mitochondria, tworząc wielowarstwową sieć transportową. Te wewnętrzne bramki pomagają ustawić pH w pęcherzykach trawiących, wspierają produkcję paliwa w mitochondriach oraz przemieszczanie enzymów i odpadów. Przegląd podkreśla, jak wiele systemów kanałowych współpracuje: wymienniki sodowo‑wodorowe regulują wewnętrzną kwasowość, kotransportery potasowo‑chlorkowe pomagają utrzymać napięcie błonowe i równowagę chlorkową, a kanały purynergiczne i mechanosensoryczne tłumaczą sygnały chemiczne lub mechaniczne na zmiany w resorpcji kości. Transportery składników odżywczych dla glukozy, aminokwasów, nukleozydów i witaminy C dodatkowo wspierają wysokie zapotrzebowanie energetyczne i biosyntetyczne aktywnie resorbujących osteoklastów.
Od biologii podstawowej do nowych terapii
Ponieważ wiele zaburzeń kostnych wynika z nadmiernej lub niewystarczającej aktywności osteoklastów, kanały i transportery kierujące ich zachowaniem są atrakcyjnymi celami lekowymi. Autorzy przeglądu omawiają istniejące i eksperymentalne związki blokujące V-ATPazy, kanały wapniowe TRP, wymieniacze chlorkowe, receptory purynergiczne i inne transportery, a także nowe koncepcje, takie jak zakłócanie konkretnych interakcji podjednostek czy wykorzystanie ukierunkowanych nanocząstek do dostarczania leków bezpośrednio do kości. Zwracają uwagę, że wiele z tych białek występuje również w innych tkankach, więc osiągnięcie prawdziwej specyficzności wobec osteoklastów pozostaje wyzwaniem. Mimo to, w miarę jak narzędzia genomiki i obrazowania ujawniają więcej o lokalizacji tych kanałów i ich wzajemnych interakcjach, rozszerzająca się „mapa jonowa” osteoklastów prawdopodobnie przyniesie bardziej precyzyjne terapie dla osteoporozy, zapalnej utraty kości i rzadkich genetycznych chorób kości.
Cytowanie: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Słowa kluczowe: osteoklasty, kanały jonowe, resorpcja kości, V-ATPaza, osteoporoza