Clear Sky Science · pl
PRMT6 jest niezbędny do zapoczątkowania i wzmocnienia makrofagowo-indukowanego zapalenia w heterotopowej kostnieniu przez zwiększenie ekspresji CCL2
Kiedy gojenie idzie za daleko
Czasami po poważnym urazie lub zabiegu ciało tak bardzo stara się naprawić uszkodzenie, że tworzy nową tkankę kostną tam, gdzie nie powinna się pojawić. Ten bolesny stan, zwany niechcianym wzrostem kości w tkankach miękkich, może unieruchomić stawy, utrudnić amputacje i utrudniać codzienne poruszanie się. Dostępne terapie są ograniczone i często nie zapobiegają nawrotom. W tym badaniu odkryto kluczowy wczesny przełącznik w układzie odpornościowym, łączący uraz z tym nieprawidłowym tworzeniem kości — i wskazano krótki, krytyczny okres, w którym ukierunkowane leczenie mogłoby zatrzymać proces zanim się rozwinie. 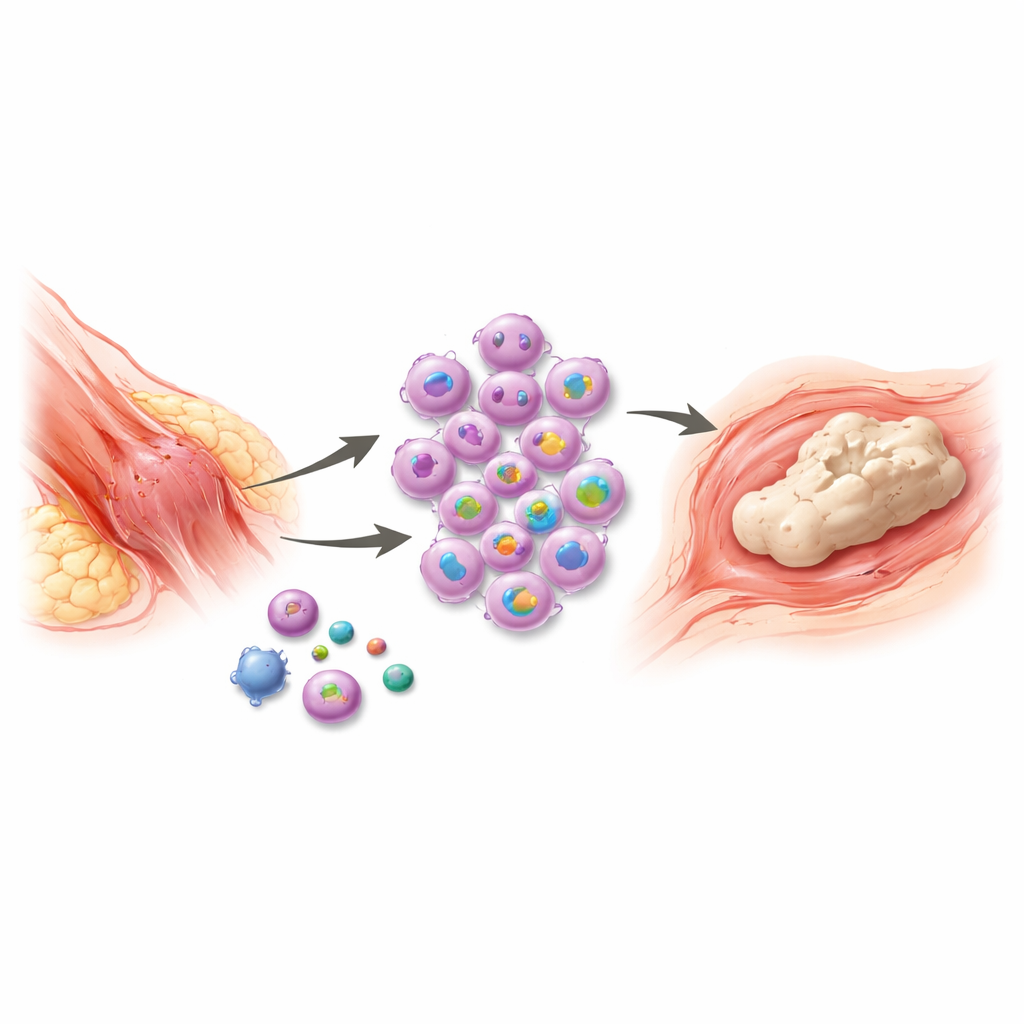
Problem kości w niewłaściwym miejscu
Po poważnym urazie, takim jak oparzenia, złamania czy zabiegi ortopedyczne, u niektórych pacjentów mogą powstawać wyspy kości wewnątrz mięśni, ścięgien i innych tkanek miękkich. Nowa tkanka kostna tworzy się w procesie podobnym do normalnego rozwoju kości, zaczynając od stanu zapalnego, a kończąc na dojrzałej, zmineralizowanej tkance. Chociaż wiadomo, że komórki odpornościowe zwane makrofagami odgrywają centralną rolę w tej reakcji, szczegółowy mechanizm kontrolujący, jak one inicjują i podtrzymują zapalenie, pozostawał niejasny. Bez tej wiedzy terapie takie jak leki przeciwzapalne, napromienianie czy późniejsze chirurgiczne usuwanie głównie leczą skutki, a nie przyczynę, co sprzyja nawrotom.
Kluczowy pośrednik zapalenia
Wykorzystując model myszy łączący uszkodzenie ścięgna z oparzeniem — wiernie odwzorowujący ciężkie urazy u ludzi — badacze śledzili zmiany w miejscu urazu w czasie. Zaobserwowali szybkie gromadzenie się makrofagów w ciągu pierwszych dni po urazie, które następnie utrzymywało się podczas formowania nieprawidłowej kości. Gdy pozbawiono tych komórek, dodatkowa kość niemal zanikła, a otaczająca tkanka wykazywała znacznie mniejsze zaburzenia naczyń krwionośnych i komórek podtrzymujących. Dogłębna analiza ekspresji genów w uszkodzonej tkance wyróżniła jeden molekuł w tych makrofagach: PRMT6, enzym modyfikujący białka i pomagający kontrolować, które geny są aktywowane.
Molekularny przycisk głośności zapalenia
Zespół odkrył, że poziomy PRMT6 w makrofagach szybko wzrastały po urazie i w odpowiedzi na sygnały zagrożenia oraz składniki bakteryjne w warunkach laboratoryjnych. Myszy pozbawione PRMT6, lub u których PRMT6 był selektywnie zredukowany tylko w makrofagach, miały znacznie mniej makrofagów w miejscu urazu i rozwijały się u nich dramatycznie mniejsze ilości nieprawidłowej kości. Co istotne, uszkodzone ścięgna u tych zwierząt goiły się lepiej, z bardziej uporządkowaną tkanką i mniejszym bliznowaceniem. Wskazuje to, że PRMT6 nie jest niezbędny do zdrowej naprawy, lecz działa jak pokrętło głośności, które wzmacnia szkodliwe zapalenie. Gdy badacze zablokowali PRMT6 za pomocą leku, efekt wystąpił tylko przy podaniu wczesnym — w ciągu pierwszych tygodni po urazie. Rozpoczęcie leczenia później miało niewielki wpływ, ujawniając wąskie, lecz silne okno terapeutyczne. 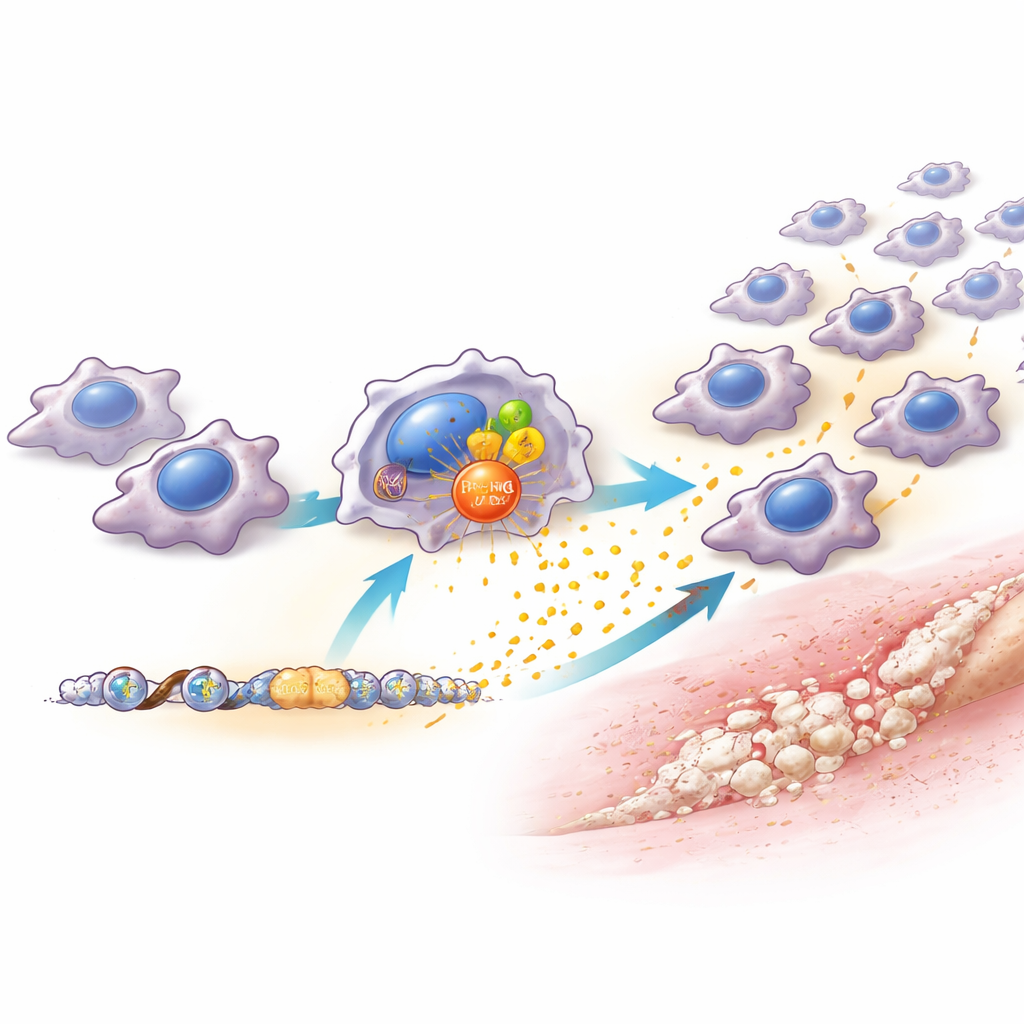
Jak jeden sygnał przyciąga wiele komórek odpornościowych
Aby zrozumieć, jak PRMT6 wywołuje ten efekt, naukowcy szczegółowo przebadali makrofagi. Bez PRMT6 te komórki wytwarzały znacznie mniejsze ilości kilku chemicznych atrakcyjnych czynników, zwłaszcza jednego zwanego CCL2, który zazwyczaj przyciąga więcej monocytów i makrofagów z krwi do uszkodzonej tkanki. PRMT6 pomaga włącząć gen CCL2 na dwa sposoby: współdziała ze znanym regulatorem zapalenia NF-κB oraz chemicznie oznacza pobliskie białka opakowujące DNA, ułatwiając odczyt tego genu. W efekcie makrofagi z wysokim poziomem PRMT6 wydzielają więcej CCL2, przyciągając dodatkowe makrofagi i budując "ognisko zapalne", które wspiera naczynia krwionośne i komórki macierzyste tworzące kość. Gdy CCL2 zostało specyficznie ograniczone tylko w makrofagach, wynik przypominał utratę PRMT6 — mniej makrofagów, słabsze nisze zapalne i mniejsza ilość dodatkowej kości. Przywrócenie CCL2 częściowo odtworzyło zarówno napływ makrofagów, jak i powstawanie nieprawidłowej kości.
Skierowana szansa zapobiegania niechcianej kości
Podsumowując, badanie pokazuje, że PRMT6 w makrofagach działa jako wczesny wzmacniacz epigenetyczny: zwiększa kluczowy sygnał chemiczny rekrutujący więcej komórek odpornościowych, co z kolei napędza tworzenie kości tam, gdzie nie powinno być. Ponieważ blokowanie PRMT6 tylko w wczesnej fazie zapalnej znacząco zmniejszało niechcianą kostninę, przy jednoczesnym zachowaniu prawidłowego gojenia ścięgien — a nawet poprawie organizacji tkanki — ta ścieżka oferuje obiecującą nową strategię. W praktyce krótki, dobrze wyważony kurs terapii ukierunkowanej na PRMT6 po poważnym urazie lub zabiegu mógłby zapobiec długotrwałej niepełnosprawności spowodowanej ektopową kością, nie osłabiając zdolności organizmu do samodzielnej naprawy.
Cytowanie: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Słowa kluczowe: heterotopowa kostnina, makrofagi, zapalenie, regulacja epigenetyczna, sygnalizacja CCL2