Clear Sky Science · pl
C/EBPβ dyktuje transkrypcję podjednostki β FSH po menopauzie, a blokada szlaku AEP/C/EBPβ łagodzi osteoporozę
Dlaczego to badanie ma znaczenie dla życia po menopauzie
Wiele kobiet słyszy, że spadek estrogenu jest główną przyczyną łamliwości kości po menopauzie. To badanie wnosi nowy element do układanki: inny hormon, hormon folikulotropowy (FSH), oraz para białek w mózgu i kościach — C/EBPβ i AEP — współdziałają, przyspieszając ubytek masy kostnej. Co jeszcze ciekawsze, naukowcy pokazują na myszach, że zablokowanie tego szlaku eksperymentalną pigułką może chronić kości równie skutecznie jak zatwierdzony lek na osteoporozę.
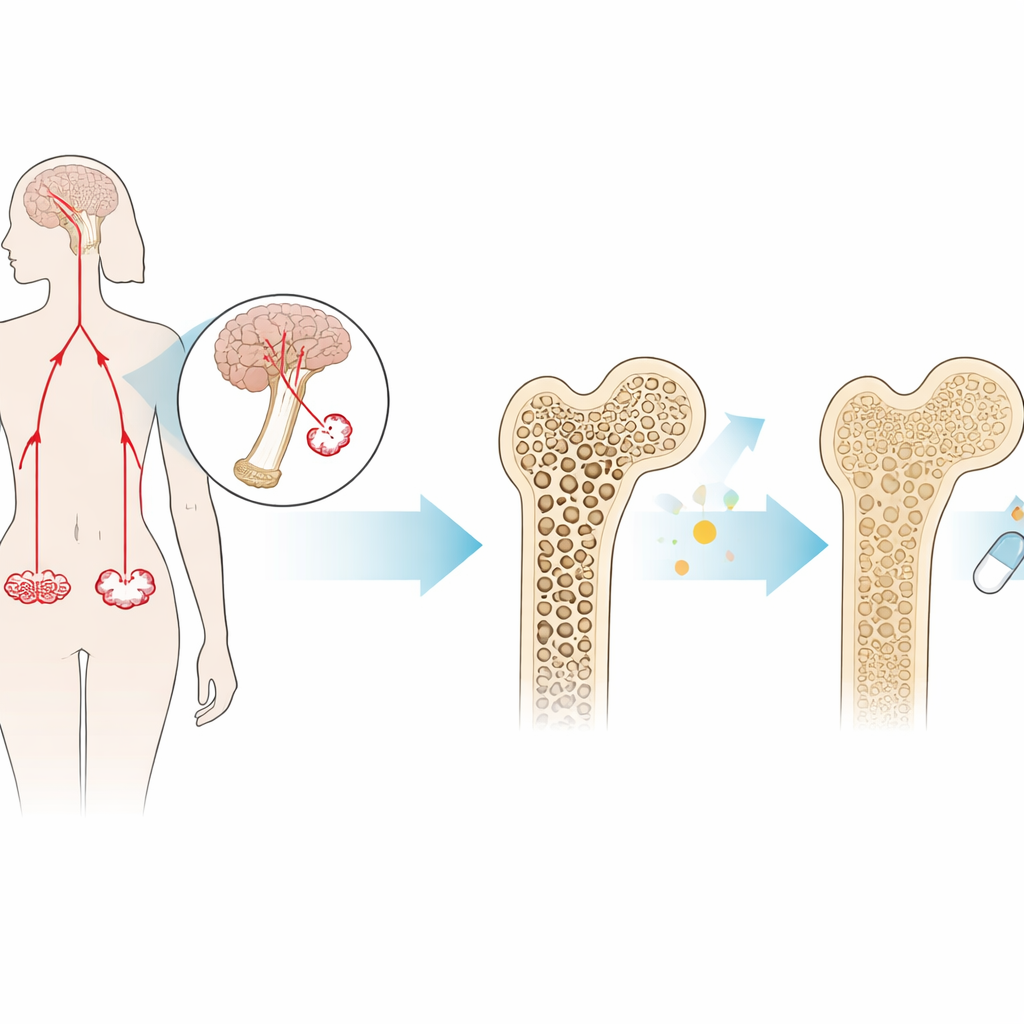
Mniej znany hormon o dużym wpływie na kości
FSH jest produkowany w przysadce i jest najlepiej znany z roli w płodności. U kobiet zbliżających się do menopauzy jego poziom gwałtownie wzrasta na kilka lat przed ostatnim krwawieniem miesiączkowym. Poza rolą rozrodczą FSH może działać bezpośrednio na kości: wiąże się z receptorami na komórkach odpowiedzialnych za resorpcję kości (osteoklastach), pobudzając je do szybszego rozkładania tkanki kostnej niż jest ona odbudowywana. Wcześniejsze prace wykazały, że myszy pozbawione FSH lub jego receptora są chronione przed ubytkiem kości, nawet przy niskim poziomie estrogenu. Sugerowało to, że sam FSH, a nie tylko niedobór estrogenu, może napędzać osteoporozę pomenopauzalną.
Przełącznik kontrolny w przysadce
Nowe badanie koncentruje się na C/EBPβ, białku wiążącym DNA, które włącza lub wyłącza geny. Autorzy odkryli, że C/EBPβ wiąże się bezpośrednio z regionem kontrolnym genu podjednostki beta FSH — części hormonu definiującej jego tożsamość — i zwiększa jego produkcję w przysadce. W hodowlach komórek przysadkowych zwiększenie poziomu C/EBPβ podnosiło FSH, podczas gdy wyciszenie C/EBPβ zmniejszało FSH, zwłaszcza gdy komórki były stymulowane przez mózgowy sygnał rozrodczy, GnRH. U myszy po ovariektomii, które naśladują menopauzę przez usunięcie jajników produkujących estrogen, zwierzęta z obniżonym poziomem C/EBPβ wytwarzały znacznie mniej FSH w przysadce i we krwi. Te eksperymenty ukazują C/EBPβ jako kluczowy przełącznik decydujący o tym, jak silny jest wzrost FSH po spadku estrogenu.
Samonasilająca się pętla i nowy cel terapeutyczny
C/EBPβ kontroluje także inne białko zwane AEP, enzym tnący, który może aktywować lub dezaktywować inne molekuły. W mózgu łańcuch C/EBPβ–AEP był powiązany z uszkodzeniami przypominającymi chorobę Alzheimera. Tutaj zespół sprawdził, czy ten sam łańcuch oddziałuje na FSH i kości. U myszy pozbawionych AEP poziomy zarówno C/EBPβ, jak i FSH spadły w przysadce, a utrata kości po usunięciu jajników była zmniejszona. Zablokowanie AEP za pomocą małocząsteczkowego leku nazwanego #11a dało podobny efekt: po miesiącach leczenia myszy po ovariektomii miały niższe FSH, mocniejsze kości w badaniach wysokiej rozdzielczości i mniej nadaktywności komórek resorbujących kość. Inna klasa związków — aktywatory TrkB, które pośrednio tłumią AEP — pomagała komórkom kostnym w hodowlach, ale nie potrafiła obniżyć FSH u zwierząt, głównie dlatego, że receptor docelowy jest rzadki w przysadce. Ten kontrast wzmocnił wniosek, że bezpośrednia inhibicja AEP jest skuteczniejszym sposobem zdławienia osi C/EBPβ–FSH u jej źródła.
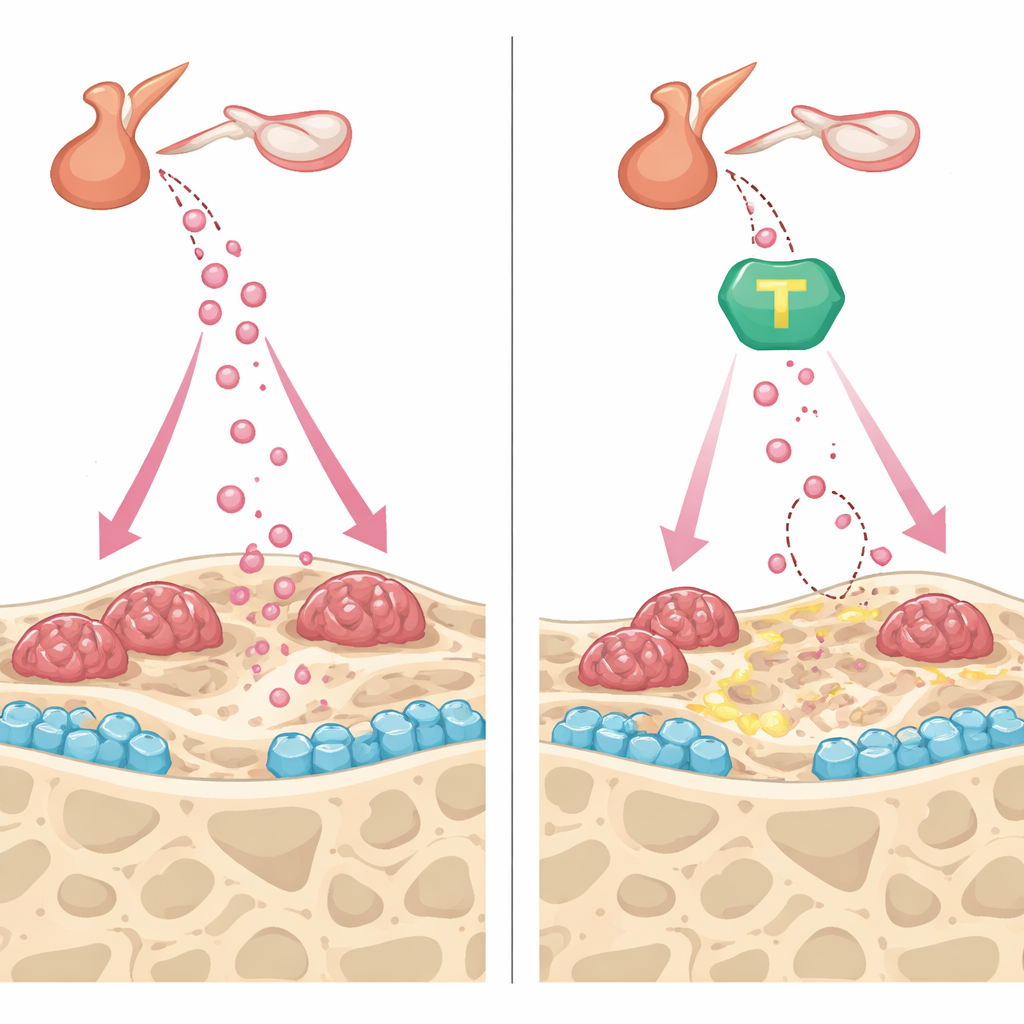
Ochrona kości z dwóch stron
Poza obniżeniem FSH, #11a i aktywator TrkB o nazwie CF3CN wykazały uzupełniające korzyści wewnątrz kości. W hodowlach komórek tworzących kość oba związki przyspieszały dojrzewanie i odkładanie minerału, częściowo przez zachowanie fibryonektyny — białka strukturalnego, które AEP zwykle tnie — oraz przez wzmocnienie sygnałów sprzyjających kościom, takich jak osteoprotegeryna. W komórkach resorbujących kość leki osłabiały efekty kluczowego sygnału resorpcji, zmniejszając liczbę dużych, wielojądrzastych komórek i ich zdolność do wycinania wgłębień w plasterkach kostnych. U żywych myszy zarówno #11a, jak i CF3CN ograniczały szybki obrót kostny wywołany usunięciem jajników, stabilizując gęstość i mikroarchitekturę kości. Co uderzające, kiedy #11a porównano bezpośrednio z teriparatydem, zatwierdzonym przez FDA lekiem w formie zastrzyku, który buduje kość, eksperymentalna pigułka dorównywała teriparatydowi w przywracaniu objętości i wytrzymałości kości w tym modelu.
Co to może znaczyć dla przyszłej opieki nad osteoporozą
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że praca ta identyfikuje wielozadaniowy szlak łączący związane z menopauzą stany zapalne ze wzrostem FSH i uszkodzeniem kości, i pokazuje, że celowanie w AEP może przerwać ten łańcuch. U myszy doustny inhibitor AEP nie tylko obniża nadmiar FSH napędzający utratę kości, lecz także bezpośrednio przesuwa równowagę w kości w stronę budowy zamiast rozkładu. Choć wyniki te wymagają potwierdzenia u ludzi, sugerują, że przyszłe terapie osteoporozy mogą wykraczać poza proste zastępowanie estrogenu czy stymulowanie tworzenia kości i zamiast tego wyciszać ten nowo opisany hormonalny i enzymatyczny obwód odpowiedzialny za łamliwość kości po menopauzie.
Cytowanie: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
Słowa kluczowe: osteoporoza pomenopauzalna, hormon folikulotropowy, szlak C/EBPβ AEP, remodeling kości, terapia celowana na hormony