Clear Sky Science · pl
Tworzenie blizny włóknistej indukowane przez TGF-β ogranicza regenerację po urazie rdzenia kręgowego
Dlaczego blizny w rdzeniu kręgowym mają znaczenie
Gdy rdzeń kręgowy doznaje poważnego urazu, wiele osób pozostaje z trwałym paraliżem lub utratą czucia, ponieważ uszkodzone włókna nerwowe nie odrastają. W tym badaniu postawiono proste, lecz kluczowe pytanie: co dokładnie hamuje to odrastanie — i czy można bezpiecznie usunąć tę barierę? Odkrywając, jak rodzaj blizny tworzy się wewnątrz uszkodzonego rdzenia, autorzy wskazują nową drogę, która może pomóc układowi nerwowemu w naprawie.
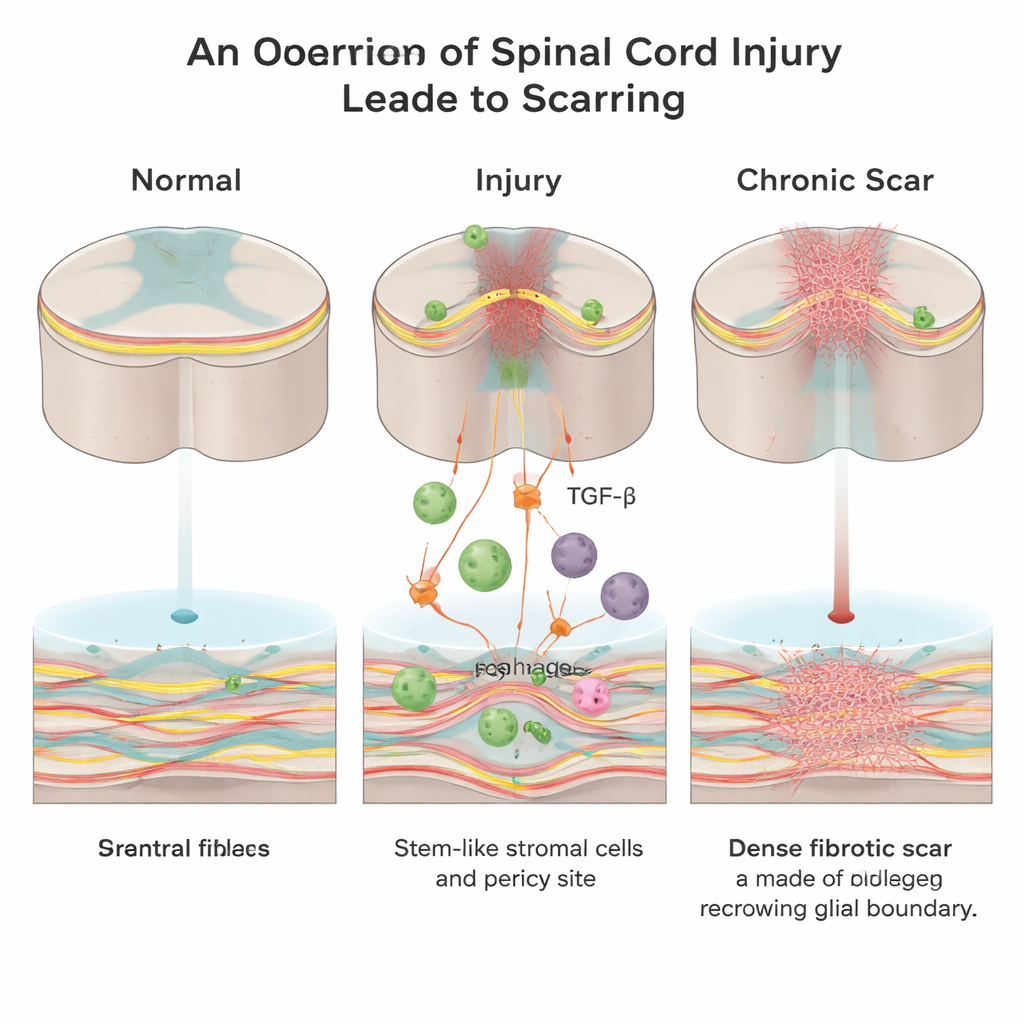
Ukryta ściana wewnątrz urazu
Po urazie rdzenia kręgowego organizm szybko usiłuje zamknąć ranę. Tworzą się dwa główne rodzaje tkanki bliznowatej: „glejowa” blizna tworzona przez komórki wspierające zwane astrocytami oraz „włóknista” blizna bogata w kolagen, fibrynę i komórki fibroblastopodobne. Podczas gdy blizna glejowa może pełnić role ochronne, blizna włóknista tworzy gęstą barierę fizyczną i chemiczną, której rosnące włókna nerwowe trudno pokonać. Dotychczas naukowcy wiedzieli znacznie mniej o tym, jak powstaje ten włóknisty rdzeń i jakie sygnały napędzają jego formowanie.
Rola komórek układu odpornościowego i silnego sygnału
Pracując na dorosłych myszach, badacze skupili się na cząsteczce sygnalizacyjnej zwanej transformującym czynnikiem wzrostu beta (TGF-β), która koordynuje naprawę ran w całym organizmie i często jest nadmiernie aktywna w chorobach włóknienia. Stwierdzili, że po urazie rdzenia napływające komórki odpornościowe znane jako makrofagi stają się głównym źródłem aktywnego TGF-β1 w miejscu uszkodzenia. Ten wzrost poziomu TGF-β1 rekrutuje lokalne mezenchymalne komórki stromalne/pnia oraz komórki związane z naczyniami zwane perycytami i skłania je do przejścia w fibroblasty — dokładnie te komórki, które deponują kolagenową, włóknistą bliznę.
Przytłumienie sygnału, by otworzyć drogę
Aby sprawdzić, czy ta droga rzeczywiście powoduje szkodliwe bliznowacenie, zespół zastosował kilka genetycznych sztuczek u myszy. Gdy usunięto makrofagi lub usunięto gen TGF-β1 tylko w komórkach linii makrofagów, ilość tkanki włóknistej w uszkodzonym rdzeniu znacznie spadła, a więcej włókien nerwowych i szlaków zawierających serotoninę zdołało przekroczyć strefę urazu. Podobnie usunięcie receptora TGF-β specyficznie w perycytach zmniejszyło ich reakcję na TGF-β, doprowadziło do mniejszego nagromadzenia kolagenu i poprawiło sprawność ruchową oraz czuciową w testach behawioralnych. Co ważne, perycyty i pokrewne komórki o cechach macierzystych wciąż istniały, ale rzadziej przekształcały się w fibroblasty tworzące bliznę.
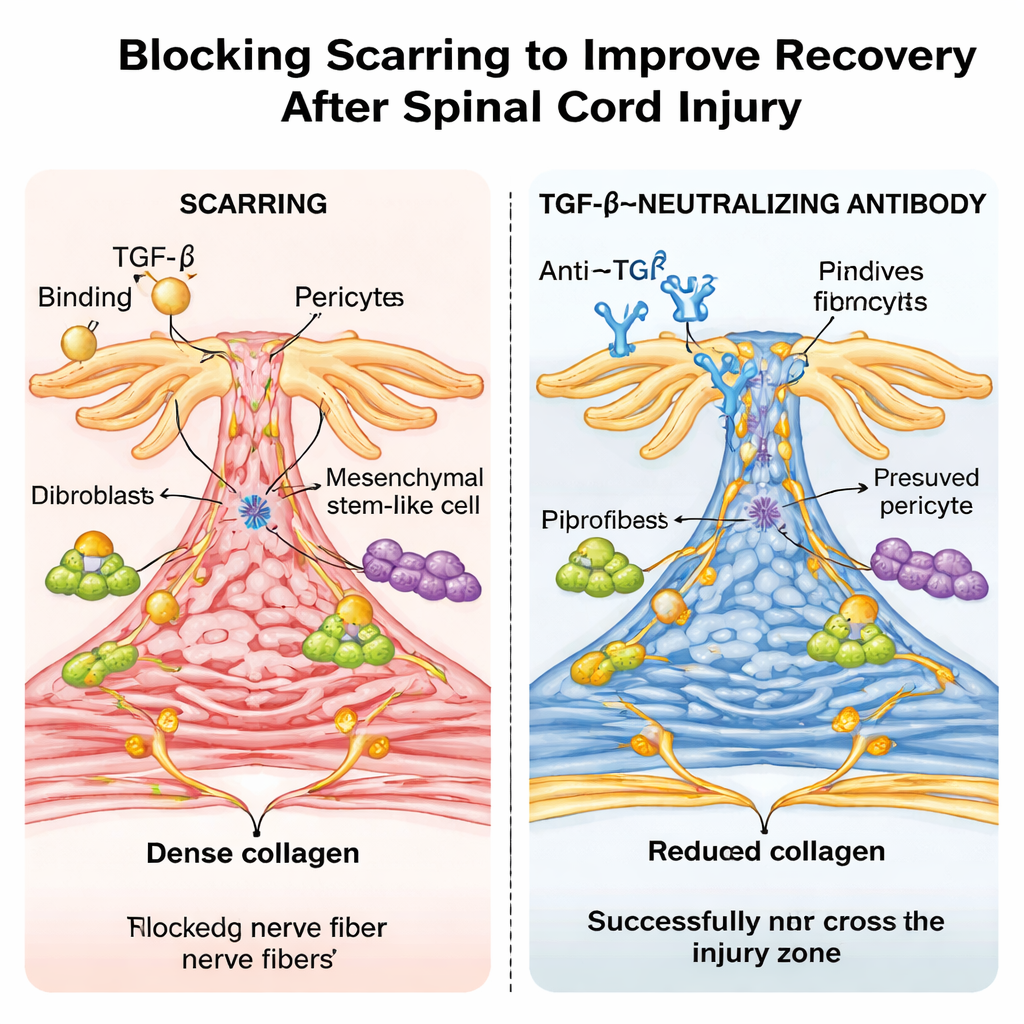
Przeciwciało przypominające lek i zaskakujący efekt wieku
Następnie badacze przetestowali podejście bardziej istotne klinicznie: leczenie zwykłych myszy laboratoryjnym przeciwciałem neutralizującym TGF-β. Powtarzane dawki po urazie obniżyły poziomy aktywnego TGF-β we krwi i rdzeniu kręgowym, zmniejszyły włóknistą bliznę i pozwoliły włóknom nerwowym skuteczniej mostkować okolice urazu, co przełożyło się na wyraźne poprawy w chodzeniu i funkcjach sensorycznych. Sekwencjonowanie RNA pojedynczych komórek potwierdziło, że geny reagujące na TGF-β były wysoko aktywne w typach komórek tworzących bliznę u myszy nieleczonych, a przeciwciało je stłumiało. Co uderzające, gdy ten sam rodzaj uszkodzenia rdzenia wykonano u noworodków, zwierzęta goiły się prawie bez włóknistego bliznowacenia, nie wykazywały wykrywalnej aktywacji TGF-β w miejscu urazu i odzyskiwały niemal normalną sprawność ruchową — przypominając naprawę bez blizn obserwowaną u niektórych zwierząt nienaczelnych.
Co to może oznaczać dla przyszłych terapii
Łącznie wyniki sugerują, że nadmierna aktywacja TGF-β po urazie rdzenia kręgowego odciąga pomocne komórki naprawcze w kierunku budowy sztywnej, włóknistej ściany, która blokuje odrost nerwów i odzyskiwanie funkcji. Zapobiegając tej nadmiernej aktywacji — poprzez celowanie w produkcję TGF-β w makrofagach, blokowanie jego receptora w perycytach i komórkach stromalnych lub stosowanie neutralizującego przeciwciała — może być możliwe ograniczenie szkodliwej blizny przy jednoczesnym zachowaniu lub nawet wzmocnieniu bardziej korzystnych reakcji tkankowych. Chociaż przeniesienie tych strategii na ludzi będzie wymagać ostrożnych badań, aby uniknąć działań niepożądanych, praca podkreśla włókniste bliznowacenie napędzane przez TGF-β jako centralną i potencjalnie możliwą do zaadresowania barierę w naprawie rdzenia kręgowego.
Cytowanie: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Słowa kluczowe: uraz rdzenia kręgowego, blizna włóknista, TGF-beta, makrofagi, regeneracja nerwów