Clear Sky Science · pl
HIF-1α i BMAL1 w regeneracji kości: dialog między reakcją na hipoksję a rytmem dobowym
Dlaczego złamane kości goją się lepiej, niż myślisz
Kiedy łamiemy kość lub usuwany jest ząb, nasze ciało cicho uruchamia wyjątkowo dobrze zorganizowany program naprawczy. Głęboko w uszkodzonym obszarze spada poziom tlenu, a nasz wewnętrzny zegar dobowy nadal tyka. Ten artykuł bada, jak dwa główne przełączniki — HIF‑1α, wyczuwający niskie stężenie tlenu, oraz BMAL1, podstawowy białkowy element zegara — współpracują, prowadząc komórki kostne przez zapalenie, tworzenie nowej tkanki i przywracanie ostatecznej wytrzymałości. Zrozumienie tego partnerstwa może poprawić leczenie złamań, osteoporozy, artretyzmu, a nawet implantów stomatologicznych.
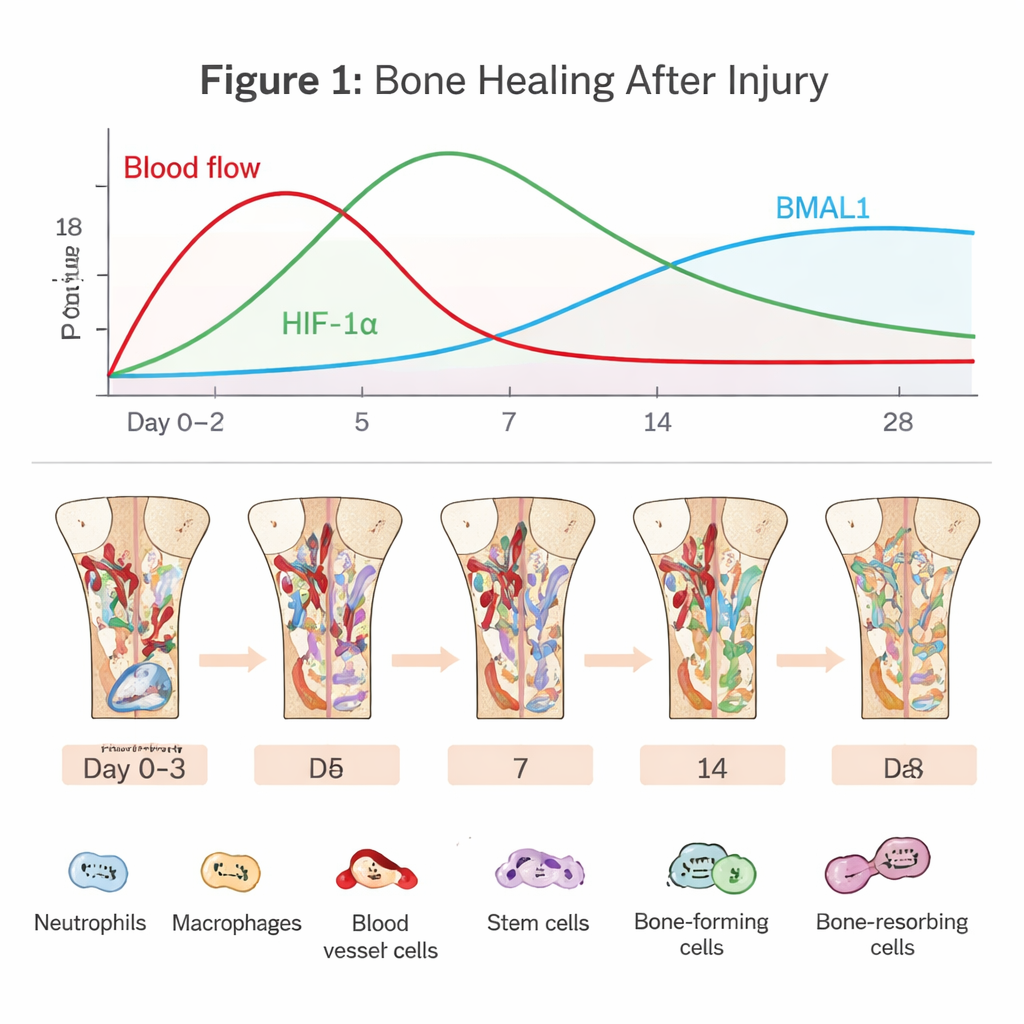
Ukryte dramaty wewnątrz gojącej się kości
Regeneracja kości zaczyna się w chwili, gdy naczynia krwionośne ulegają zerwaniu. Tworzy się skrzep, który odcina znaczną część dopływu tlenu i tworzy surową, ubogą w tlen strefę. Komórki układu odpornościowego, takie jak neutrofile i makrofagi, napływają, by posprzątać resztki i bronić przed drobnoustrojami. Równocześnie rekrutowane są komórki macierzyste szpiku i komórki naczyń krwionośnych, by odbudować obszar. Wczesna „faza zapalna” jest mieczem obosiecznym: krótka, właściwie wyważona reakcja zapalna rozpoczyna naprawę, ale jeśli trwa zbyt długo lub jest zbyt nasilona, gojenie może się zatrzymać lub nie powieść. Artykuł podkreśla, że odnalezienie tej wąskiej ścieżki w dużej mierze zależy od tego, jak komórki wyczuwają tlen i czas.
Jak komórki wykorzystują niski poziom tlenu na swoją korzyść
W strefie złamania ubogiej w tlen białko HIF‑1α stabilizuje się i włącza geny, które pomagają komórkom się przystosować. Pobudza komórki śródbłonka do tworzenia nowych naczyń, zapewniając dopływ świeżego tlenu i składników odżywczych do ubytku. Przeprogramowuje też metabolizm komórek w kierunku glikolizy — sposobu wytwarzania energii działającego także przy niedoborze tlenu. Dla komórek macierzystych i osteoblastów umiarkowana aktywacja HIF‑1α może zwiększać proliferację, migrację i wzrost kości, częściowo przez zwiększenie czynników takich jak VEGF, łączących tworzenie naczyń z formowaniem nowej tkanki kostnej. Jednak gdy hipoksja jest zbyt głęboka lub przedłużona, gromadzą się cząsteczki stresu i reaktywne formy tlenu, co skłania osteoblasty do śmierci i pobudza osteoklasty resorbujące kość. Ten sam sygnał hipoksyczny może zatem albo wspierać, albo sabotować gojenie — w zależności od jego natężenia i długości trwania.
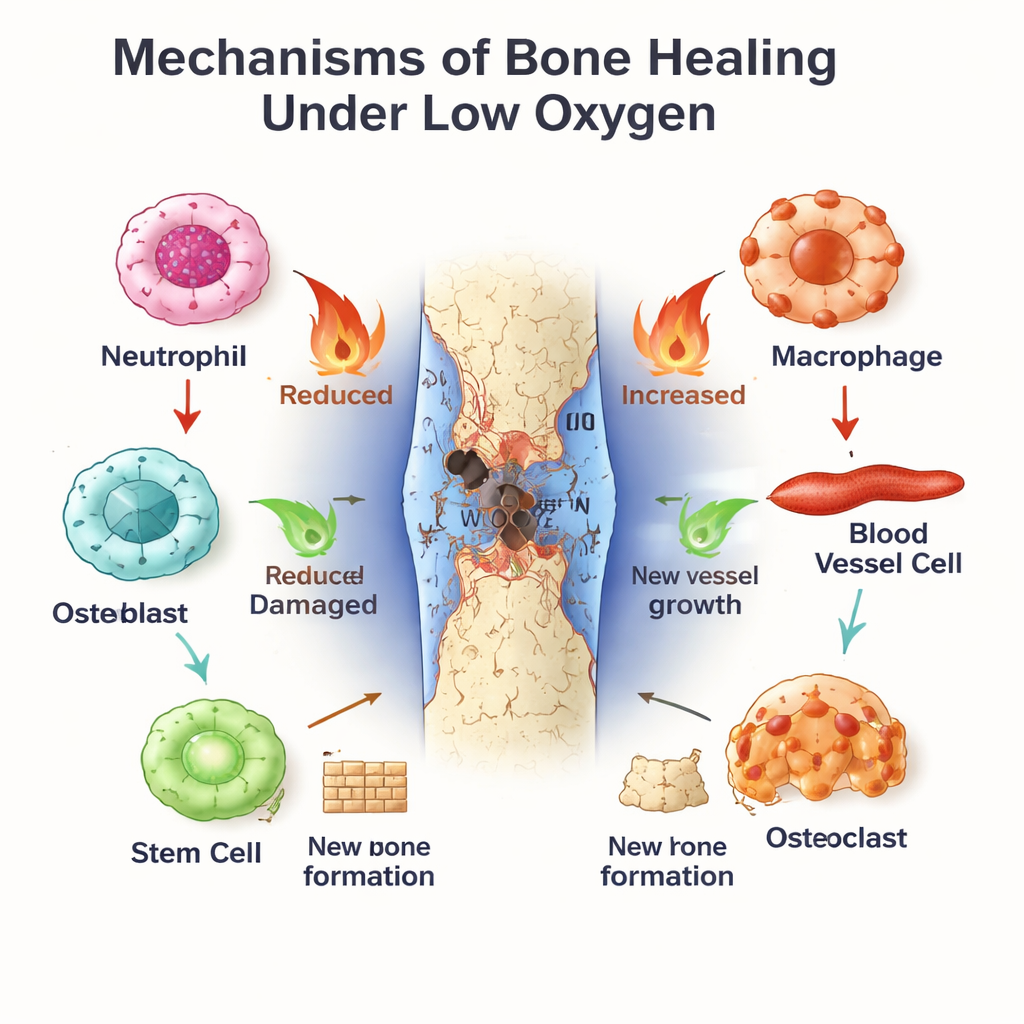
Wewnętrzny zegar ciała jako menedżer naprawy kości
Równolegle działa zegar dobowy, molekularny stoper obecny praktycznie w każdej komórce. BMAL1, jeden z jego centralnych składników, pomaga ustalać dobowe rytmy aktywności odpornościowej, zachowania naczyń krwionośnych i różnicowania komórek macierzystych. Neutrofile i makrofagi wykazują różnice zależne od pory dnia w sile odpowiedzi na uraz i w szybkości starzenia się lub przełączania z stanów zapalnych (podobnych do M1) na stany sprzyjające gojeniu (podobne do M2). W komórkach naczyń i komórkach macierzystych szpiku BMAL1 sprzyja zdrowej proliferacji i uporządkowanemu tworzeniu kości, częściowo przez strojeniem szlaków wzrostu, takich jak Wnt i TGF‑β/SMAD. Gdy BMAL1 zostaje zaburzony — przez defekty genetyczne, pracę zmianową lub choroby metaboliczne — kości mają tendencję do utraty masy, komórki macierzyste wyczerpują się, a równowaga między tworzeniem a resorpcją kości przesuwa się w stronę ubytku.
Rozmowa między wyczuwaniem tlenu a zegarem biologicznym
Rdzeniem przeglądu jest pojawiający się „dialog” między HIF‑1α i BMAL1. Te dwa białka mają podobne struktury i mogą fizycznie wchodzić ze sobą w interakcje, tworząc nawet mieszane dimery wiążące DNA i kontrolujące pokrywające się zestawy genów. Każde z nich może wpływać na produkcję i stabilność drugiego, tworząc pętle sprzężenia zwrotnego, które łączą rytm dobowy z reakcją komórek na hipoksję. Wspólnie zarządzają także balansem redoks komórki — ile szkodliwych reaktywnych form tlenu jest produkowanych w stosunku do dostępnych mechanizmów antyoksydacyjnych — i współregulują kluczowe enzymy decydujące, czy komórki polegają bardziej na oddychaniu zależnym od tlenu, czy na glikolizie niezależnej od tlenu. Ta wspólna kontrola pomaga określić, czy środowisko złamania sprzyja konstruktywnej odbudowie, czy nadmiernemu zapaleniu i resorpcji kości.
Co to oznacza dla chorób i terapii
To samo partnerstwo HIF‑1α–BMAL1 pojawia się w wielu chorobach związanych z kośćmi. U pracowników zmianowych zaburzenia snu i ekspozycja na światło prawdopodobnie modyfikują BMAL1, zwiększają stres oksydacyjny i zakłócają naprawę kierowaną przez HIF‑1α, co przyczynia się do osteoporozy. W cukrzycy wysoki poziom cukru osłabia zarówno funkcję zegara, jak i sygnalizację hipoksji, podważając rozwój naczyń krwionośnych i tworzenie kości napędzane przez komórki macierzyste. W chorobie zwyrodnieniowej stawów utrata BMAL1 w komórkach chrząstki zaburza ich rytm i ochronną relację z HIF‑1α, przyspieszając rozpad chrząstki. Wokół implantów tytanowych kontrolowana hipoksja i zdrowy rytm dobowy wydają się wspierać lepszą oseointegrację, co sugeruje, że przyszłe powłoki implantów mogą być projektowane tak, by łagodnie aktywować zarówno HIF‑1α, jak i BMAL1. Ogólnie artykuł wnioskuje, że udana regeneracja kości zależy nie tylko od obecności odpowiednich komórek, lecz także od tego, jak odczytują one tlen i czas — a ukierunkowanie tej rozmowy może otworzyć nowe drogi do szybszego i trwalszego gojenia.
Cytowanie: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Słowa kluczowe: regeneracja kości, rytmy dobowe, hipoksja, osteoporoza, gojenie złamań