Clear Sky Science · pl
Inteligentne biomateriały do naprawy i regeneracji szkieletu w starzejącym się organizmie
Mocniejsze kości w starzejącym się świecie
Wielu ludzi uważa osłabienie kości i bóle stawów za nieuchronne części procesu starzenia. Tymczasem naukowcy projektują teraz „inteligentne” materiały, które potrafią wykryć, kiedy i gdzie kości zawodzą, i wspomóc ich samonaprawę. Materiały te mają na celu bardziej niezawodne leczenie złamań, spowolnienie lub odwrócenie osteoporozy i choroby zwyrodnieniowej stawów oraz zmniejszenie potrzeby powtarzanych operacji — dając starszym osobom większą szansę na zachowanie aktywności i niezależności.
Jak kości się starzeją i dlaczego łatwiej pękają
Kość to żywa tkanka, która nieustannie się odbudowuje, lecz z wiekiem równowaga ta zaburza się. Komórki macierzyste w szpiku przesuwają się od produkcji komórek tworzących kość ku wytwarzaniu komórek tłuszczowych; osteoblasty (komórki budujące kość) tracą wydajność, a osteoklasty (komórki niszczące kość) stają się nadaktywne. Macierz wspierająca z kolagenu i minerałów staje się bardziej sucha i krucha, a mikroskopowe „rusztowanie” ulega przerzedzeniu. Zmiany hormonalne, przewlekłe, niskiego stopnia zapalenie, nadmiar reaktywnych form tlenu i kwaśne lokalne środowisko dodatkowo obciążają tkankę. Z zewnątrz objawia się to cieńszymi, bardziej porowatymi kośćmi, sztywniejszymi stawami, skrzywieniem kręgosłupa oraz wyższym ryzykiem złamań i chorób takich jak osteoporoza i choroba zwyrodnieniowa stawów.
Dlaczego istniejące terapie nie wystarczają
Obecne główne metody leczenia obejmują leki hamujące ubytek kości lub stymulujące jej tworzenie, a także zabiegi chirurgiczne i implanty z metalu lub ceramiki stabilizujące złamania czy zastępujące uszkodzone stawy. Podejścia te ratowały wiele osób, ale mają istotne wady. Leki podawane ogólnoustrojowo często docierają tylko do bardzo małej części tkanki kostnej i mogą powodować działania niepożądane, takie jak problemy z żuchwą, zakrzepy krwi czy nawet zwiększone ryzyko nowotworów przy długotrwałym stosowaniu. Terapie komórkowe z użyciem komórek macierzystych w badaniach na zwierzętach dają obiecujące wyniki, ale napotykają problemy z przeżywalnością komórek, ich nieprzewidywalnym zachowaniem i potencjalnym tworzeniem się guzów. Konwencjonalne implanty zapewniają wytrzymałość, ale są „głupimi” obiektami: nie czują otoczenia, nie dostosowują uwalniania leków i mogą zawieść w kruchych kościach starszych pacjentów.
Inteligentne nośniki leków patrolujące ciało
Inteligentne biomateriały wprowadzają do tego obrazu elementy „inteligencji”. Jedną z głównych strategii jest ogólnoustrojowe „inteligentne dostarczanie” leków za pomocą nanocząstek lub miękkich żeli, które krążą w krwiobiegu i aktywują się tylko w miejscach problematycznych. Nośniki te mogą być zaprojektowane tak, by reagować na sygnały wewnętrzne, takie jak kwasowość, wysokie stężenia szkodliwych form tlenu czy enzymy rozpuszczające kość; albo na zewnętrzne bodźce, takie jak światło, ultradźwięki, ciepło czy pole magnetyczne. Na przykład niektóre cząstki pozostają nienaruszone w normalnej tkance, ale otwierają się i uwalniają zawarty lek w kwaśnych, bogatych w enzymy kieszonkach, gdzie nadaktywne komórki resorbujące kość niszczą tkankę. Inne pochłaniają nadmiar reaktywnych form tlenu, jednocześnie powoli uwalniając lek przeciwzapalny, lub niosą barwniki do obrazowania, by lekarze mogli śledzić ich przebieg w czasie rzeczywistym. Łącząc wiele wyzwalaczy — na przykład pH i utleniacze — badacze mogą zaostrzyć celowanie i zmniejszyć działania niepożądane.
Miejscowe rusztowania działające jak tymczasowe inteligentne kości
Gdy starzejące się kości mają duże ubytki lub złożone złamania, miejscowo wszczepiane „inteligentne rusztowania” mogą wypełnić wady. Te trójwymiarowe struktury, wykonane z metali, ceramik, polimerów lub ich kombinacji, są zaprojektowane tak, by odpowiadać wytrzymałości, porowatości i elastyczności kości. Ich gąbczasta architektura pozwala na wzrost naczyń krwionośnych i nowej tkanki kostnej, podczas gdy materiał stopniowo rozpuszcza się i jest zastępowany przez własną tkankę pacjenta. 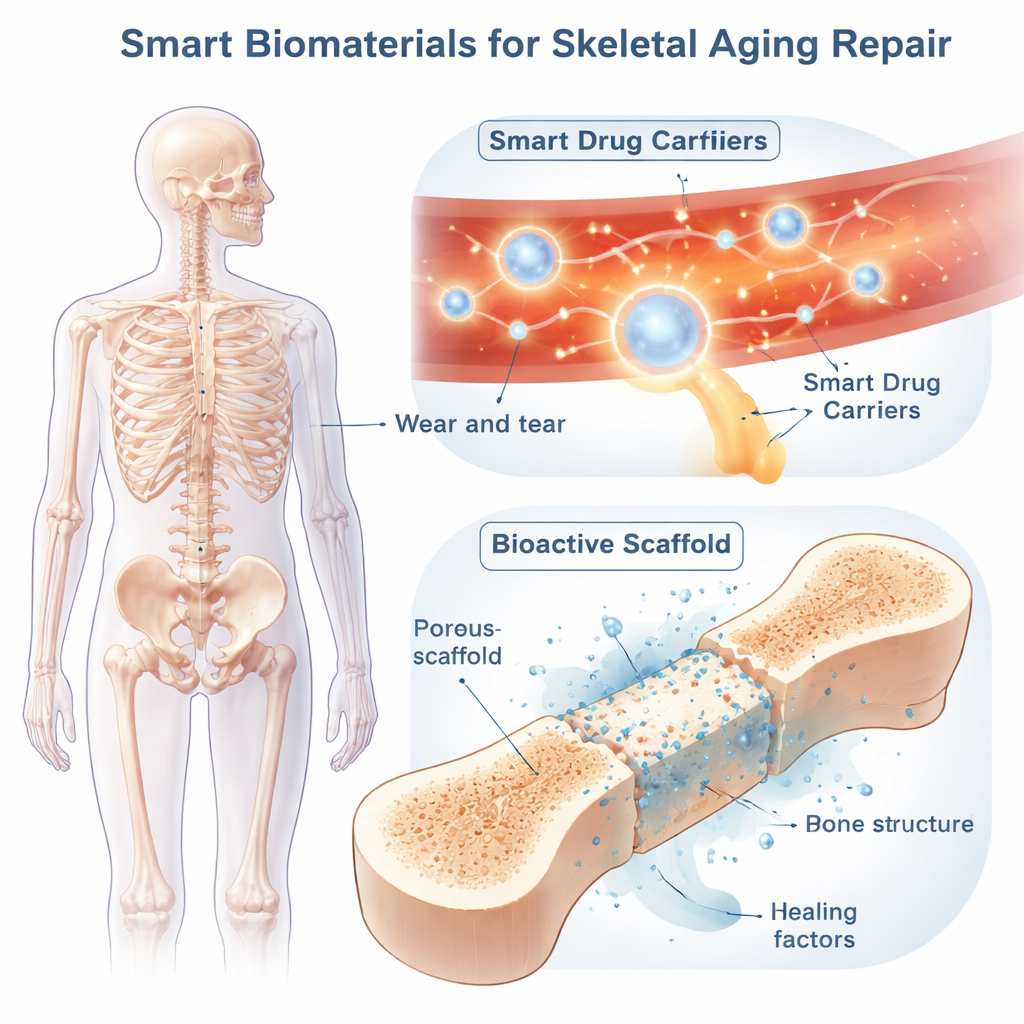
Z laboratorium do kliniki: narzędzia, przeszkody i kierunki rozwoju
Aby tworzyć te złożone systemy, naukowcy korzystają z zaawansowanych technologii wytwarzania, takich jak druk 3D i produkcja addytywna, aby precyzyjnie dostosować wielkość porów, sztywność i ładunek leków. Mimo to przekształcenie inteligentnych biomateriałów w rutynowe terapie jest wyzwaniem. Większość wstrzykiwanych cząstek nadal kumuluje się w narządach takich jak wątroba i śledziona zamiast w kości, a wiele modeli zwierzęcych nie oddaje złożoności starzejących się ludzi. Produkcja na dużą skalę, kontrola jakości, zatwierdzenia regulacyjne i koszty pozostają istotnymi barierami. Badacze upatrują nadziei w łączeniu inteligentnych materiałów ze sztuczną inteligencją w celu personalizacji projektu rusztowań i dawkowania leków, a także w dodawaniu wbudowanych czujników, które mogą śledzić gojenie i automatycznie dostosowywać terapię w trybie „zamkniętej pętli”. 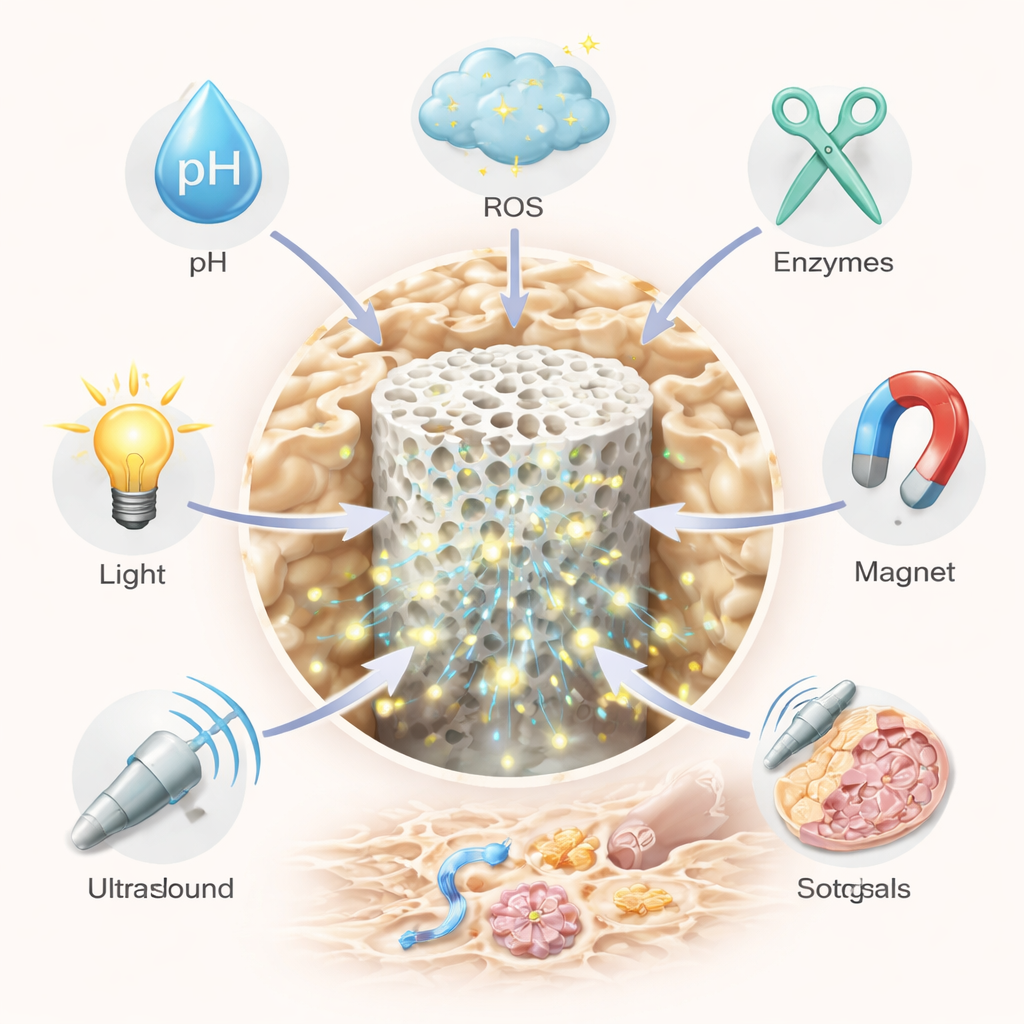
Co to może znaczyć dla pacjentów
W istocie ta praca pokazuje, że kruchość kości w podeszłym wieku nie jest jedynie nieodwracalnym spadkiem, lecz złożonym problemem inżynieryjnym, który być może da się rozwiązać. Inteligentne biomateriały działają jak maleńkie, programowalne brygady naprawcze: patrolują krwiobieg, osiadają w uszkodzonych miejscach i uwalniają dokładnie to, co jest potrzebne, kiedy jest to potrzebne, aby przywrócić strukturę i funkcję kości. Chociaż technologie te wciąż pozostają w dużej mierze na etapie badań, wskazują drogę ku przyszłości, w której złamania goją się szybciej, implanty dłużej wytrzymują, a terapie są dostosowane do unikalnej biologii kości każdego pacjenta — pomagając większej liczbie osób zachować mobilność i niezależność nawet w zaawansowanym wieku.
Cytowanie: Liang, D., Wang, H., Jiang, Y. et al. Smart biomaterials for skeletal aging repair and regeneration. Bone Res 14, 24 (2026). https://doi.org/10.1038/s41413-026-00505-9
Słowa kluczowe: inteligentne biomateriały, starzenie się szkieletu, regeneracja kości, osteoporoza, rusztowania reagujące na bodźce