Clear Sky Science · pl
Strukturalne warianty genomowe wpływają na prognozowanie u pacjentów z cytogenetycznie prawidłową ostrą białaczką szpikową
Dlaczego drobne zmiany w DNA mają znaczenie dla pacjentów z białaczką
U dorosłych z rozpoznaną ostrą białaczką szpikową (AML) lekarze coraz częściej korzystają z badań genetycznych, by oszacować skuteczność leczenia. Jednak u prawie połowy tych pacjentów standardowe badania chromosomalne wyglądają „normalnie”, a prognoza pozostaje trudna do przewidzenia. W badaniu wykazano, że ukryte, drobne przestawienia w DNA — zbyt małe, by je dostrzec pod mikroskopem — mogą wyraźnie wyróżnić grupę pacjentów, u których choroba przebiega znacznie agresywniej niż sugerują obecne narzędzia.
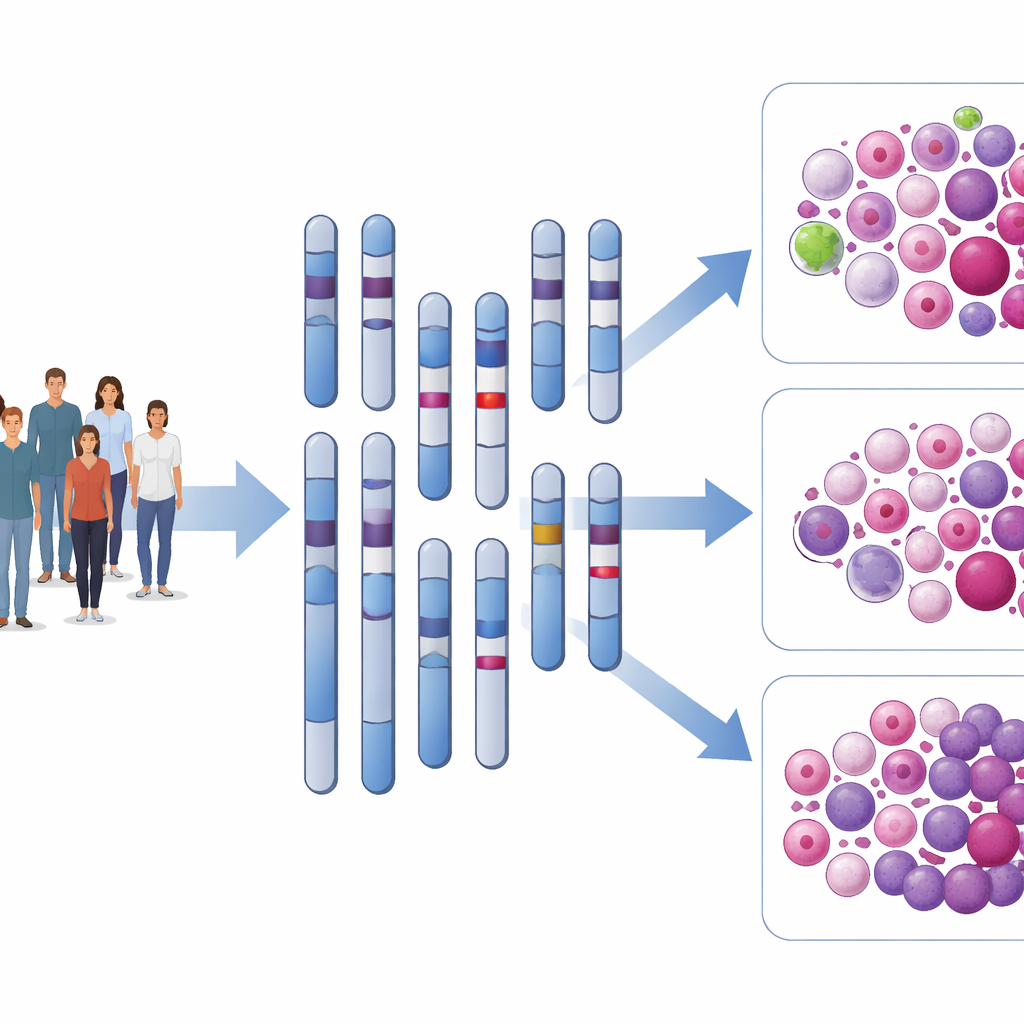
Widzieć dalej niż pozornie normalne chromosomy
AML to nowotwór krwi, w którym niedojrzałe białe krwinki wypierają zdrowe komórki w szpiku kostnym. Lekarze rutynowo analizują chromosomy i znane mutacje genowe, aby zakwalifikować pacjentów do grup o korzystnym, pośrednim lub niekorzystnym rokowaniu, co wpływa na decyzje, np. o wczesnym przeszczepieniu komórek macierzystych. Jednak około 45% pacjentów ma „cytogenetycznie prawidłową” AML — ich chromosomy wydają się niezmienione — mimo że wyniki leczenia wahają się od długotrwałego przeżycia po szybki nawrót. Autorzy przypuszczali, że subwizyjne przestawienia DNA, znane jako warianty strukturalne, mogą wyjaśniać tę ukrytą różnorodność.
Wykorzystanie sekwencjonowania długich odczytów jako genetycznej lupy
Aby odnaleźć te kryptczne zmiany, zespół zastosował sekwencjonowanie całego genomu długimi odczytami — technologię odczytującą bardzo długie fragmenty DNA, dobrze nadającą się do wykrywania insercji, delecji i innych przestawień. Zastosowano ją do komórek białaczkowych od 162 intensywnie leczonych dorosłych z cytogenetycznie prawidłową AML włączonych do dwóch badań klinicznych. Po rygorystycznym odfiltrowaniu wariantów dziedzicznych i artefaktów technicznych wyselekcjonowano ponad dwa tysiące surowych ustaleń do 118 wiarygodnych wariantów strukturalnych rozmieszczonych na autosomach. Większość stanowiły niewielkie insercje lub delecje zlokalizowane w niekodujących obszarach genomu, takich jak introny i regulatory, zamiast bezpośrednio w sekwencjach kodujących białka.
Pięć drobnych zmian definiuje grupę bardzo wysokiego ryzyka
Następnie badacze sprawdzili, które z tych 118 wariantów korelują z długością przeżycia pacjentów i czasem wolnym od zdarzeń, takich jak nawrót lub brak odpowiedzi na leczenie. Z użyciem uczenia maszynowego i modeli przeżycia zidentyfikowali pięć konkretnych wariantów strukturalnych, które niezależnie sygnalizowały znacznie gorsze rokowanie. Pacjenci noszący co najmniej jeden z tych „wariantów wysokiego ryzyka” — około 13–15% badanych — mieli mniejsze szanse na osiągnięcie całkowitej remisji, częściej doświadczali nawrotów i mieli wyraźnie krótsze przeżycie, zwykle poniżej roku. Efekt utrzymywał się po uwzględnieniu dobrze znanych mutacji, takich jak FLT3 i NPM1, i pozostał istotny w drugiej, realnej kohorcie 149 dodatkowych pacjentów badanych przy użyciu ukierunkowanych testów.
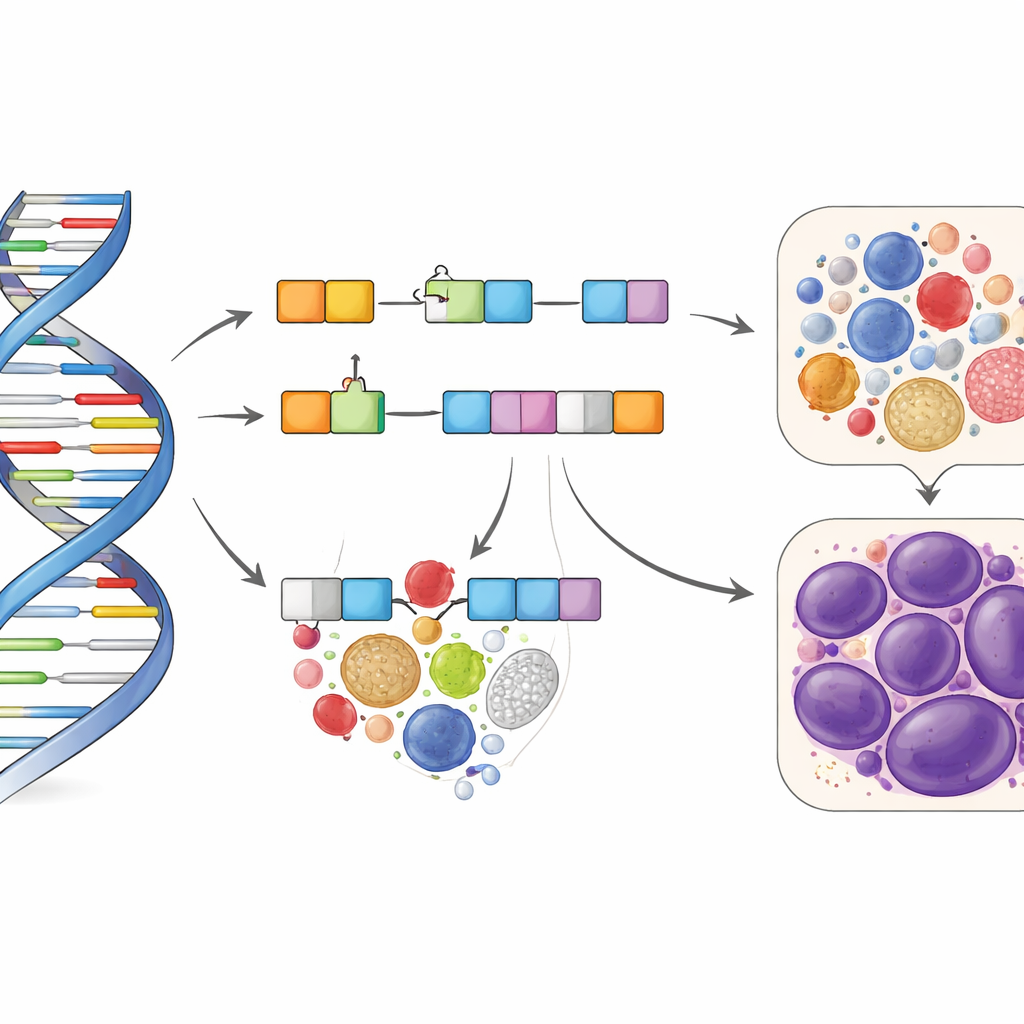
Udoskonalenie istniejących ocen ryzyka i wyjaśnienie mechanizmu
Obecne europejskie wytyczne dotyczące ryzyka klasyfikują wszystkich pacjentów z cytogenetycznie prawidłową AML do szerokich kategorii na podstawie niektórych mutacji, ale często nie rozdzielają wyraźnie ryzyka pośredniego od niekorzystnego. Dodając obecność któregokolwiek z pięciu wariantów wysokiego ryzyka jako nowy poziom „bardzo niekorzystny”, autorzy opracowali zaktualizowany czteropoziomowy schemat. Ulepszony wskaźnik przewidywał ogólne i bezzdarzeniowe przeżycie dokładniej niż model standardowy, szczególnie dla pacjentów z mutacjami NPM1, którzy zwykle są oznaczani jako korzystni, ale radzili sobie bardzo źle, gdy równocześnie mieli te zmiany strukturalne. Badania laboratoryjne potwierdziły biologiczne podłoże: warianty wysokiego ryzyka wiązały się ze zmienioną aktywnością pobliskich genów, a eksperymentalne zmiany poziomów niektórych z tych genów w modelach komórkowych zakłócały normalny wzrost komórek i kontrolę cyklu komórkowego — cechy zgodne z bardziej agresywnym przebiegiem białaczki.
Co to oznacza dla pacjentów i opieki
Mówiąc prosto, badanie sugeruje, że niektórzy pacjenci z AML, których chromosomy wyglądają normalnie i którzy obecnie otrzymują etykietę „pośredni” lub nawet „korzystny”, mogą faktycznie mieć znacznie groźniejszą postać choroby. Mały zestaw drobnych przestawień DNA — wykrywalnych przy użyciu nowoczesnego sekwencjonowania lub ukierunkowanych badań uzupełniających — potrafi wcześnie zidentyfikować tych pacjentów. Rozpoznanie tej ukrytej grupy bardzo wysokiego ryzyka mogłoby pomóc lekarzom skierować ich do bardziej intensywnych lub eksperymentalnych terapii oraz do bliższego monitorowania, z celem poprawy wyników, które obecnie są złe.
Cytowanie: Bartalucci, N., Mannelli, F., Tarantino, D. et al. Genomic structural variations contribute to inform prognosis in patients with cytogenetically normal acute myeloid leukemia. Blood Cancer J. 16, 37 (2026). https://doi.org/10.1038/s41408-026-01465-3
Słowa kluczowe: ostra białaczka szpikowa, wariant strukturalny, genomowa stratyfikacja ryzyka, sekwencjonowanie długich odczytów, mutacja NPM1