Clear Sky Science · pl
Mechanizmy ucieczki przed układem odpornościowym i postępy terapeutyczne w wirusowo związanych nowotworach krwi
Wirusy i ukryte nowotwory krwi
Większość z nas myśli o wirusach jako o przyczynach krótkotrwałych chorób, takich jak przeziębienie czy grypa. Jednak kilka wirusów może cicho osiedlać się w naszych organizmach przez długie lata i w końcu przyczynić się do powstania poważnych nowotworów krwi, takich jak chłoniaki i białaczki. Ten przegląd syntetyzuje aktualną wiedzę naukową na temat tego, jak te wirusy wymykają się naszej odporności oraz jak ta wiedza otwiera drogę do bardziej precyzyjnych, mniej toksycznych terapii.
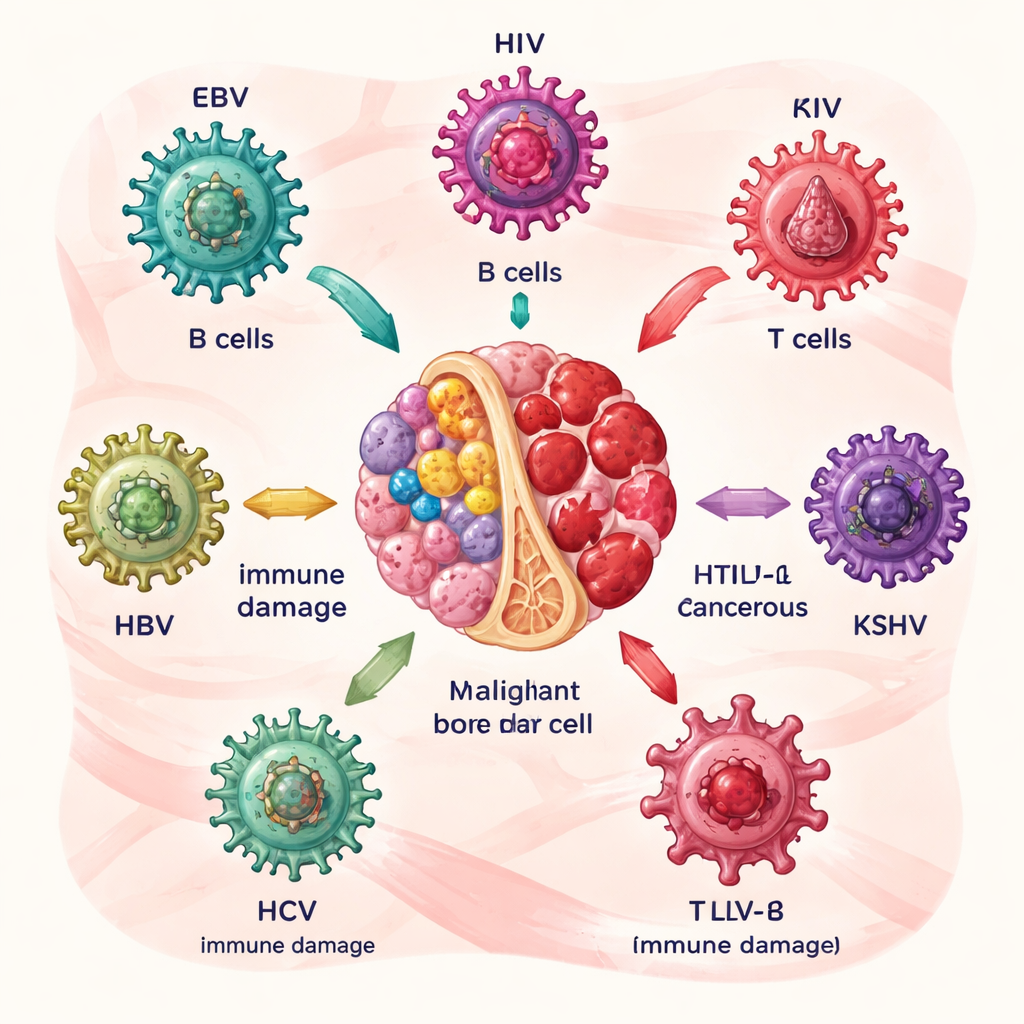
Jak niektóre wirusy przygotowują podłoże do nowotworu krwi
Autorzy opisują najpierw sześć głównych winowajców: wirusa Epsteina–Barra (EBV), wirusa niedoboru odporności człowieka (HIV), ludzki wirus białaczki limfocytów T typu 1 (HTLV‑1), wirusa związanego z mięsakami Kaposiego (KSHV) oraz wirusy zapalenia wątroby typu B i C (HBV i HCV). Każdy z nich atakuje komórki krwi lub układu odpornościowego na swój sposób. EBV i HCV głównie zakłócają funkcję limfocytów B, czyli komórek produkujących przeciwciała; HTLV‑1 atakuje limfocyty T; HIV osłabia ogólną odporność; KSHV sprzyja nieprawidłowemu wzrostowi pewnych białych krwinek; a HBV i HCV mogą ukrywać się w limfocytach i komórkach macierzystych. Na przestrzeni lat białka wirusowe popychają zainfekowane komórki do namnażania, unikania fizjologicznej śmierci komórkowej i gromadzenia uszkodzeń DNA, co stopniowo zwiększa ryzyko rozwoju chłoniaków i powiązanych chorób.
Jak komórki nowotworowe uczą się ukrywać przed układem odpornościowym
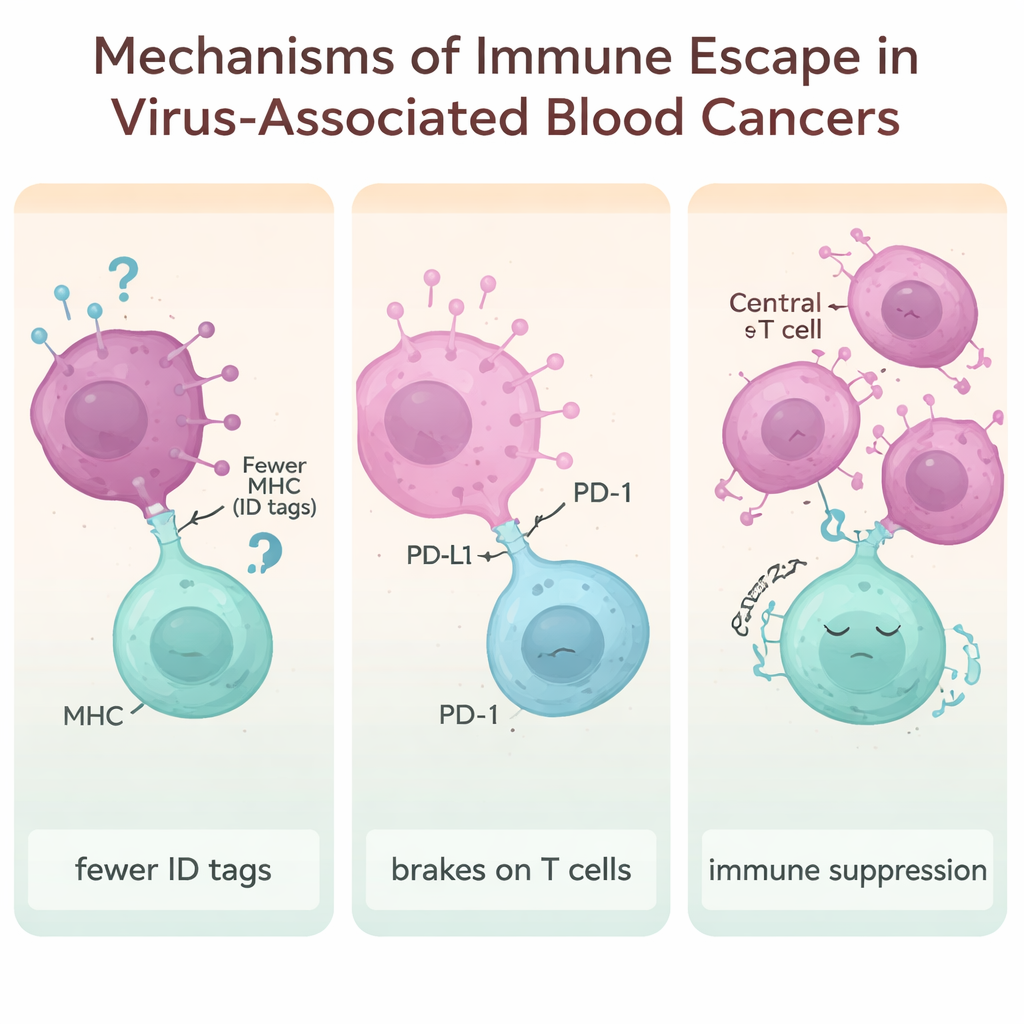
Centralnym motywem artykułu jest „ucieczka immunologiczna” – sztuczki, których używają nowotwory wywołane przez wirusy, żeby pozostać niewidocznymi lub nietkniętymi przez obronę gospodarza. Jedną ze strategii jest zmniejszenie molekularnych „identyfikatorów” (zwanych cząsteczkami MHC) na powierzchni komórki, które limfocyty T normalnie skanują w poszukiwaniu zagrożeń. Białka wirusowe EBV, HTLV‑1, HIV i HBV mogą obniżać ekspresję tych identyfikatorów, dzięki czemu złośliwe komórki są mniej rozpoznawalne i atakowane. Inną taktyką jest wykorzystywanie „hamulców” immunologicznych, takich jak PD‑1, PD‑L1, CTLA‑4, LAG‑3 i TIM‑3. Gdy te molekularne punkty kontrolne są nadaktywne, limfocyty T ulegają wyczerpaniu i stają się ospałe. Wiele chłoniaków związanych z wirusami wykazuje bardzo wysokie poziomy tych hamulców, zwłaszcza w guzach powiązanych z EBV i HBV.
Komórki odpornościowe przemienione z bojowników w strażników pokoju
Przegląd podkreśla także subtelniejszy manewr: przekształcenie mikrośrodowiska immunologicznego tak, aby sprzyjało nowotworowi. Limfocyty T regulatorowe – podgrupa limfocytów T, które normalnie zapobiegają nadmiernemu zapaleniu – mogą być rozszerzane i aktywowane przez przewlekłe infekcje wirusowe. Sygnały takie jak cytokiny IL‑10 i TGF‑β zachęcają te komórki regulatorowe do namnażania i tłumienia pobliskich „zabójczych” limfocytów T. W przewlekłych zakażeniach, takich jak HTLV‑1, HBV i HIV, ten zaburzony balans tworzy ochronną bańkę wokół powstających komórek nowotworowych, utrudniając organizmowi wywołanie skutecznej odpowiedzi.
Nowe taktyki leczenia oparte na słabych punktach wirusów
Posiadając jaśniejszy obraz tych mechanizmów, badacze opracowują terapie celujące w wirusową maszynerię lub zdeformowane środowisko immunologiczne. Leki małocząsteczkowe są projektowane, aby blokować kluczowe białka wirusowe EBV i HTLV‑1, a nawet oznaczać je do zniszczenia wewnątrz komórki. Inhibitory punktów kontrolnych – przeciwciała uwalniające hamulce PD‑1/PD‑L1 lub CTLA‑4 – są badane w szeregu chłoniaków związanych z wirusami, często w połączeniu ze standardową chemioterapią. Wiroterapia onkolityczna, polegająca na inżynieryjnym modyfikowaniu wirusów tak, by selektywnie zakażały i niszczyły komórki nowotworowe, jednocześnie pobudzając nową odpowiedź immunologiczną, wchodzi w pierwsze próby kliniczne. Równocześnie bardziej złożone podejścia, takie jak przetoczenia komórek T specyficznych dla wirusa, terapia CAR‑T i szczepionki terapeutyczne, mają na celu odbudowę lub przeszkolenie układu odpornościowego, aby wydajniej i dłużej rozpoznawał cele wirusowe oraz komórki nowotworowe.
Co to oznacza dla pacjentów i przyszłej opieki
W sumie artykuł argumentuje, że nowotwory krwi związane z wirusami to nie tylko zwykłe guzy z przyczepionym wirusem. To choroby, których istnienie zależy od długotrwałej przepychanki między wirusami, komórkami krwi i układem odpornościowym. Rozumiejąc dokładnie, jak wirusy pomagają komórkom nowotworowym ukrywać się i rozwijać, lekarze mogą projektować mądrzejsze kombinacje terapii, które blokują drogi ucieczki, pobudzają wyczerpane komórki odpornościowe i bezpośrednio eliminują zainfekowane wirusem komórki. Chociaż wiele z tych strategii wciąż znajduje się w badaniach klinicznych, wskazują one na przyszłość, w której pacjenci z tymi złożonymi nowotworami będą otrzymywać bardziej spersonalizowane, skuteczne terapie – a w niektórych przypadkach długotrwałą kontrolę choroby, a nawet wyleczenie.
Cytowanie: Li, T., Wang, C., Xiao, Q. et al. Immune escape mechanisms and therapeutic advances in virus-associated hematological malignancies. Blood Cancer J. 16, 24 (2026). https://doi.org/10.1038/s41408-026-01453-7
Słowa kluczowe: limfoma związana z wirusem, ucieczka przed układem odpornościowym, terapia inhibitorami punktów kontrolnych immunologicznych, CAR‑T i terapia komórkowa T, terapeutyczne szczepionki przeciwnowotworowe