Clear Sky Science · pl
Ekspresja APOE3-Christchurch w astrocytach łagodzi patologię amyloidu-β w mózgach myszy 5xFAD
Dlaczego ta wariacja mózgu ma znaczenie
Choroba Alzheimera bywa zwykle przedstawiana jako niepowstrzymane gromadzenie się szkodliwych grudek białkowych w mózgu. Tymczasem kilka osób wykazuje wyjątkową odporność i zachowuje sprawność umysłową mimo posiadania silnych czynników genetycznych ryzyka. Badanie to koncentruje się na jednym z takich ochronnych wariantów w powszechnie występującym genie odpowiadającym za metabolizm cholesterolu i stawia praktyczne pytanie: czy jeśli dostarczymy do mózgu więcej tej ochronnej wersji — konkretnie z komórek wspierających zwanych astrocytami — czy możemy uczynić zmiany podobne do tych w Alzheimerze mniej szkodliwymi?
W centrum uwagi ochronny wariant genu
Praca skupia się na rzadkiej wersji genu APOE, nazwanej APOE3-Christchurch. W wyjątkowym przypadku klinicznym kobieta nosząca silną mutację powodującą wczesny początek choroby Alzheimera zachowała sprawność poznawczą przez dekady dłużej niż przewidywano, a ten wariant APOE wydawał się być kluczowym powodem. Wcześniejsze badania na zwierzętach sugerowały, że APOE3-Christchurch może spowalniać rozprzestrzenianie się innego charakterystycznego białka Alzheimera, tau. Jego wpływ na amyloid-beta — białko tworzące klasyczne płytki w mózgach chorych na Alzheimera — nie był jednak w pełni wyjaśniony. Naukowcy postanowili sprawdzić, jak ten wariant zachowuje się, gdy jest eksprymowany specyficznie przez astrocyty, gwiaździste komórki, które odżywiają i chronią neurony.
Testowanie wariantu na modelu myszy przypominającym Alzheimera
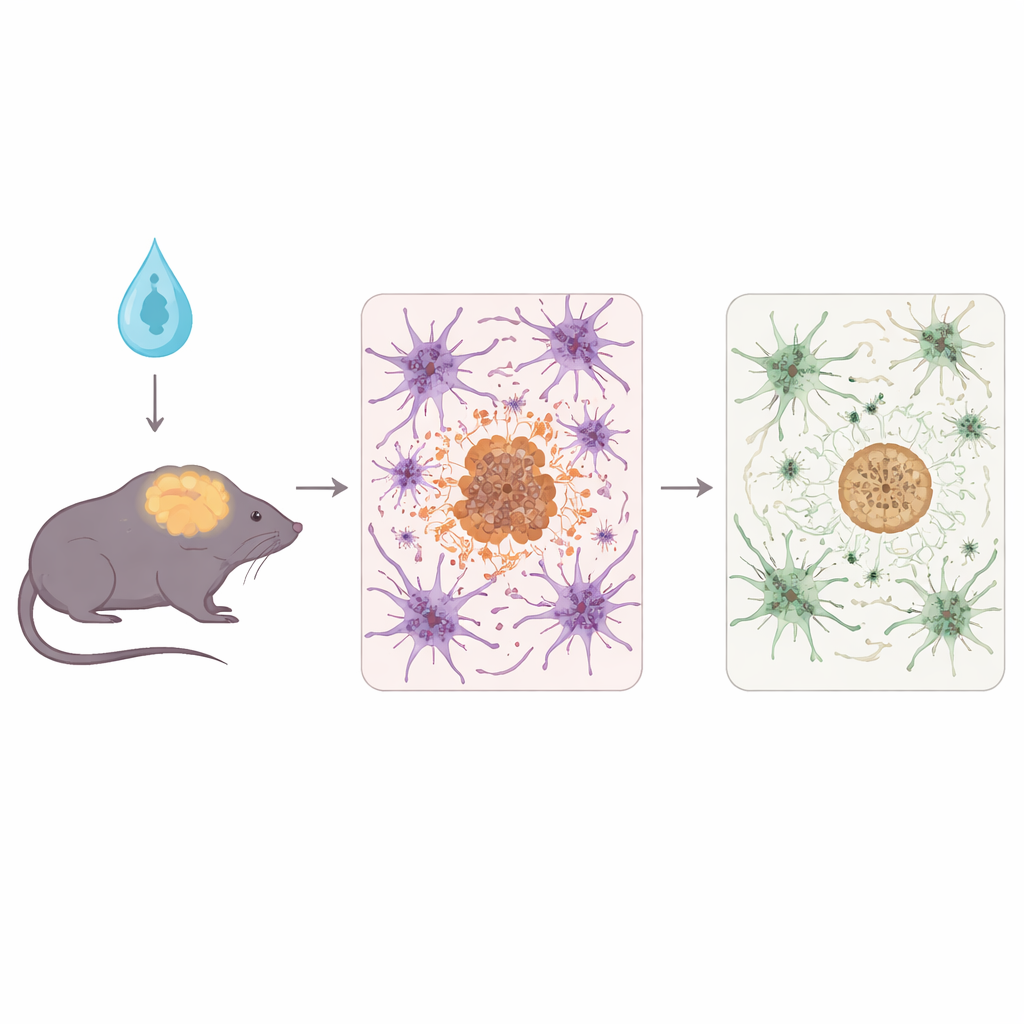
Aby to zbadać, zespół użył myszy 5xFAD, dobrze znanego modelu, który szybko rozwija obfite nagromadzenie amyloidu i związane z tym uszkodzenia mózgu. Krótko po urodzeniu myszy otrzymały nieszkodliwy wektor wirusowy, który spowodował, że ich astrocyty produkowały albo zwykłe ludzkie APOE3, albo ochronną wersję APOE3-Christchurch, albo neutralne białko kontrolne. Naukowcy następnie przeanalizowali zwierzęta na zaawansowanym etapie choroby, badając tkankę mózgową za pomocą testów biochemicznych, mikroskopii fluorescencyjnej i sekwencjonowania RNA, by sprawdzić, jak zmieniły się amyloid, pobliskie wypustki nerwowe i reakcje immunologiczne.
Uczynienie płytek mniej toksycznymi, nie tylko ich redukcja
Obie formy APOE produkowane przez astrocyty zmniejszyły łączne obciążenie płytkami amyloidowymi oraz oznaki uszkodzeń wokół tych płytek w porównaniu z grupą kontrolną. APOE3-Christchurch wykazał jednak istotne różnice jakościowe. Przesunął amyloid w kierunku bardziej zwartych, sferycznych, włókienkowatych płytek i obniżył poziomy niektórych rozpuszczalnych i oligomerycznych form amyloidu‑β — gatunków uważanych za szczególnie toksyczne dla synaps. Neuryty, cienkie wypustki komórek nerwowych w pobliżu płytek, wykazywały mniejsze zniekształcenia i uszkodzenia przy obecności APOE3-Christchurch. Równolegle komórki odpornościowe mózgu, mikroglej i astrocyty, były ogólnie mniej reaktywne, a analizy transkryptomu ujawniły stłumione szlaki immunologiczne i stresu białkowego, co sugeruje spokojniejsze, mniej wrogie środowisko dla neuronów.
Wskazówki z hodowli komórkowych i aktywności genów
Aby potwierdzić, że te efekty nie ograniczają się do myszy, zespół użył też astrocytów pochodzących z ludzkich komórek macierzystych, genetycznie zmodyfikowanych tak, by nosiły albo APOE3, albo wariant Christchurch. Astrocyty z APOE3-Christchurch wydzielały więcej białka APOE, a ich kondycjonowane medium zmniejszało tworzenie oligomerów amyloidu‑β w kontrolowanym układzie probówkowym. W mózgach myszy ekspresja APOE3-Christchurch zmieniała sieci genów zaangażowanych w fałdowanie białek, stres komórkowy i sygnalizację immunologiczną oraz obniżała poziomy białek powiązanych z reakcjami na stres i zaburzeniami metabolizmu lipidów. Razem te dowody sugerują, że APOE3-Christchurch nie tylko zmienia ilość amyloidu — zmienia jego formę i sposób, w jaki komórki mózgu na niego reagują.
Co to może znaczyć dla przyszłych terapii
Choć obserwowane tu efekty ochronne są umiarkowane, a nie cudowne, dostarczają cennych informacji. Badanie pokazuje, że zwiększenie ilości APOE3-Christchurch specyficznie w astrocytach może uczynić złogi amyloidowe bardziej zwarte i wyraźnie mniej toksyczne, zmniejszyć okoliczne uszkodzenia nerwowe oraz osłabić sygnały zapalne i stresowe, nawet bez całkowitego usuwania amyloidu. Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że nie wszystkie płytki są jednakowo szkodliwe: przekształcanie i neutralizowanie ich może być równie ważne jak ich usuwanie. Wyniki te wspierają ideę, że terapie inspirowane APOE3-Christchurch — być może dostarczane za pomocą terapii genowej lub leków naśladujących jego działanie — mogłyby pomóc mózgowi lepiej funkcjonować w obecności amyloidu i potencjalnie spowolnić lub złagodzić przebieg choroby Alzheimera.
Cytowanie: Raulin, AC., Alnobani, A., Rodriguez-Martinez, P. et al. Astrocytic APOE3-Christchurch expression ameliorates brain amyloid-β pathology in 5xFAD mice. Transl Psychiatry 16, 224 (2026). https://doi.org/10.1038/s41398-026-04002-9
Słowa kluczowe: Choroba Alzheimera, APOE3-Christchurch, amyloid-beta, astrocyty, terapia genowa