Clear Sky Science · pl
MicroRNA-132/212 negatywnie modulują nagrodę opioidową poprzez celowanie w transporter dopaminy w brzusznej części nakrywki
Dlaczego te badania mają znaczenie dla codziennego życia
Opioidowe leki przeciwbólowe i pokrewne substancje mogą przynieść ulgę, ale niosą też poważne ryzyko uzależnienia. To badanie zagląda pod maskę systemu nagrody w mózgu, by zidentyfikować drobne genetyczne przełączniki wpływające na to, jak silnie opioidy są odczuwane jako nagradzające. Zrozumienie tych przełączników może pomóc naukowcom zaprojektować mądrzejsze terapie, które uśmierzają ból lub ograniczają zależność bez przejmowania obwodów przyjemności w mózgu.
Małe cząsteczki o dużym wpływie
Nasz mózg polega na chemicznym przekaźniku zwanym dopaminą, który sygnalizuje przyjemność i motywuje do poszukiwania doświadczeń nagradzających, od smacznego jedzenia po substancje uzależniające. Siła i czas trwania tego sygnału są częściowo kontrolowane przez białko zwane transporterem dopaminy, działające jak odkurzacz, wciągający dopaminę z powrotem do komórek nerwowych. Autorzy skupili się na dwóch bardzo małych fragmentach materiału genetycznego, microRNA-132 i microRNA-212, które mogą przyciszać produkcję wybranych białek. Wcześniejsze prace powiązały te microRNA z używaniem kokainy i stresem. W tym badaniu zespół zapytał, czy wpływają one także na to, jak mózg reaguje na opioidy, w szczególności na morfinę.
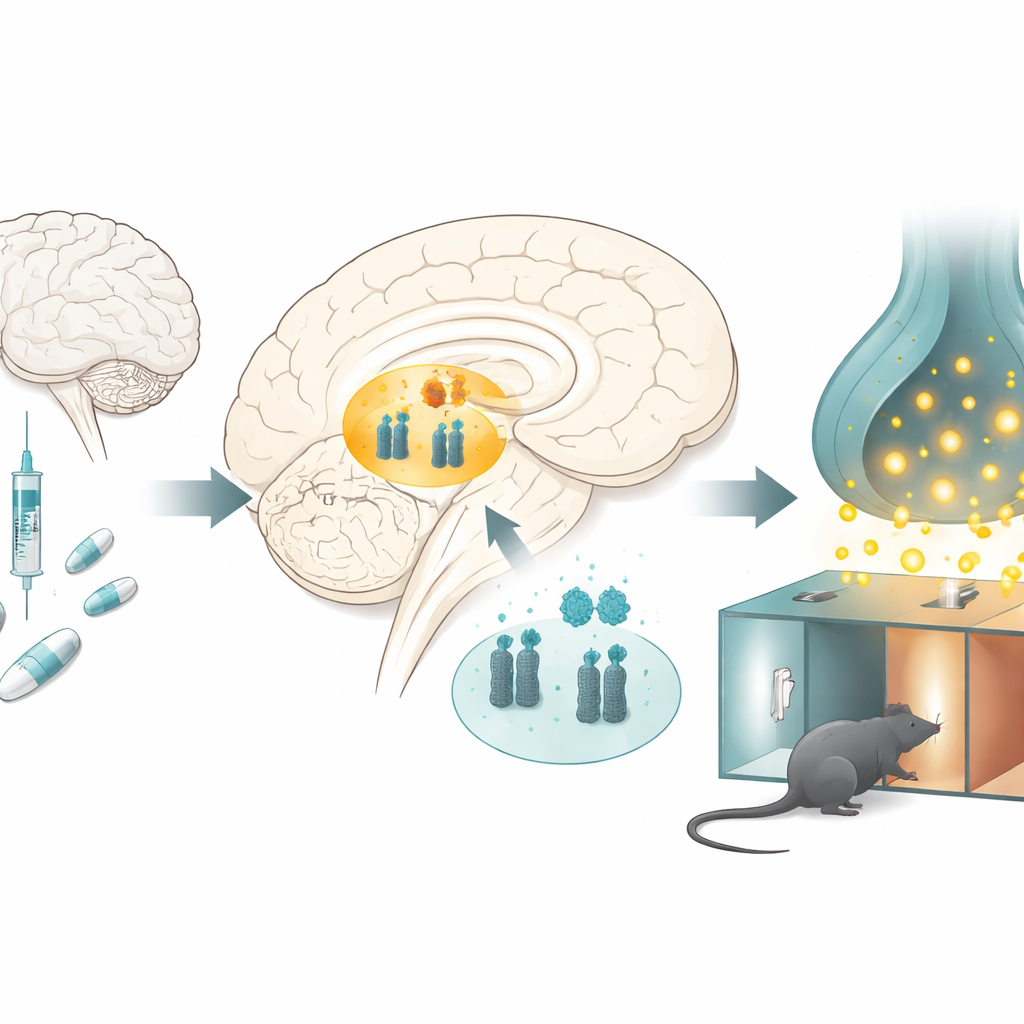
Jak opioidy zmieniają ośrodek nagrody w mózgu
Naukowcy badali szczury otrzymujące powtarzane dawki morfiny w klasycznym teście nagrody narkotykowej, w którym zwierzęta uczą się preferować komorę skojarzoną z lekiem. Po kilku dniach szczury traktowane morfiną spędzały więcej czasu w komorze powiązanej z morfiną, co świadczyło o tym, że lek stał się nagradzający. Kiedy badacze przyjrzeli się kluczowemu obszarowi nagrody głęboko w mózgu, zwanemu brzuszną częścią nakrywki, odkryli uderzający wzorzec: poziomy microRNA-132 i microRNA-212 były obniżone, podczas gdy poziomy transportera dopaminy wzrosły. Podobne zmiany pojawiały się, gdy szczury otrzymywały morfinę bez zadania uczenia się miejsca, co sugeruje, że przewlekła ekspozycja na lek sama w sobie przesuwa tę molekularną równowagę.
Wskazanie bezpośredniego związku molekularnego
Aby sprawdzić, czy te microRNA rzeczywiście kontrolują transporter dopaminy, zespół zwrócił się do komórek ludzkich o cechach nerwowych hodowanych w laboratorium. Poprzez sztuczne zwiększenie poziomu microRNA-132 lub microRNA-212 zaobserwowali spadek zarówno komunikatu genetycznego, jak i białka transportera. Blokowanie microRNA dało efekt przeciwny. Następnie skonstruowali reporter, w którym enzym wytwarzający światło był powiązany z regulacyjnym fragmentem transportera. Dodanie microRNA przygasiło sygnał świetlny, ale efekt ten zniknął, gdy kilka kluczowych zasad w miejscu wiązania zostało zmutowanych. Razem te eksperymenty pokazały, że microRNA-132 i microRNA-212 bezpośrednio przyczepiają się do komunikatu transportera i tłumią jego produkcję.
Od molekuł do poziomów dopaminy i zachowania
Następnie badacze zapytali, jak ta molekularna kontrola przekłada się na żywe komórki mózgowe. W hodowlach neuronów podwyższenie poziomu microRNA zmniejszało wychwyt dopaminy, podczas gdy ich zablokowanie zwiększało klarowanie dopaminy. Gdy sztucznie zwiększano lub zmniejszano poziomy transportera dopaminy, wpływ microRNA odpowiednio rósł lub malał, potwierdzając, że transporter jest głównym pośrednikiem. U żywych szczurów zwiększenie microRNA-132 w brzusznej części nakrywki podniosło poziomy dopaminy wypływające do połączonych regionów, co odzwierciedla słabszą aktywność transportera. Behawioralnie, użycie wirusowych narzędzi do „gąbkowania” microRNA-132 lub microRNA-212 w tym obszarze mózgu sprawiło, że szczury uczyły się silniejszej preferencji dla morfiny, wraz z wyższymi poziomami transportera. Z kolei wymuszenie dodatkowego microRNA-132 w tym samym obszarze obniżyło poziomy transportera i stłumiło preferencję morfinową u samców, samic i osobników w wieku dojrzewania, nie wpływając na ruchliwość ani przyjemność z naturalnych nagród, takich jak słodka woda.
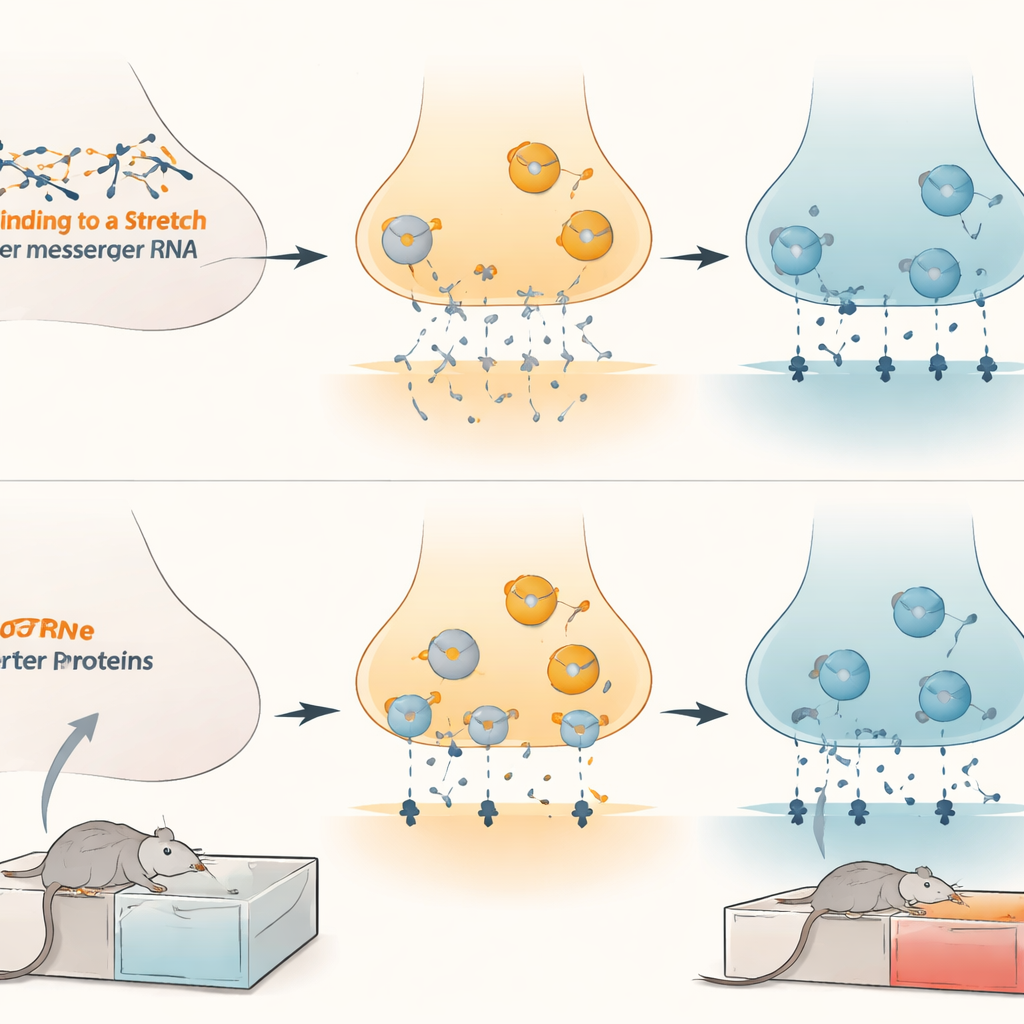
Implikacje dla leczenia uzależnienia od opioidów
Te ustalenia ujawniają precyzyjnie dostrojony system hamowania w obrębie obwodów nagrody mózgu: microRNA-132 i microRNA-212 trzymają transporter dopaminy w ryzach, kształtując, jak silnie opioidy są doświadczane jako nagradzające. Przewlekła morfina wydaje się podnosić hamulec, obniżając poziomy microRNA, co pozwala na wzrost transportera i pomaga utrwalić sygnały związane z nagrodą wywołaną przez lek. Przywrócenie lub naśladowanie działania tych microRNA specyficznie w brzusznej części nakrywki może pozwolić osłabić siłę nagrody opioidowej bez szerokiego tłumienia przyjemności czy ruchu. Choć przed przetestowaniem takich strategii u ludzi czeka jeszcze wiele pracy, badanie wskazuje nową, wysoko ukierunkowaną drogę dla przyszłych terapii, które mogłyby zwalczać uzależnienie na poziomie molekularnych pokręteł mózgu.
Cytowanie: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
Słowa kluczowe: uzależnienie od opioidów, transporter dopaminy, microRNA-132, brzuszna część nakrywki, nagroda morfinowa