Clear Sky Science · pl
Specyficzność celu i powtarzalność w neuro-kardio-kierowanym TMS dla sprzężenia serce‑mózg
Słuchając serca poprzez mózg
Depresję często postrzega się jako zaburzenie nastroju i myślenia, ale wpływa ona także na ciało — w szczególności na serce. Osoby z ciężką depresją często mają szybsze, mniej elastyczne bicie serca, co wiąże się z gorszym stanem zdrowia. Badanie stawia intrygujące pytanie: czy formę nieinwazyjnej stymulacji mózgu, już stosowaną w leczeniu depresji, można dostroić i ukierunkować w czasie rzeczywistym za pomocą reakcji serca, aby znaleźć lepsze, bardziej spersonalizowane miejsca stymulacji w mózgu?
Jak impulsy magnetyczne komunikują się z mózgiem i sercem
Powtarzalna przezczaszkowa stymulacja magnetyczna (rTMS) wykorzystuje impulsy magnetyczne przykładane na skórę głowy, aby wpłynąć na aktywność określonych obszarów mózgu. Głównym celem w depresji jest lewa grzbietowo-boczna kora przedczołowa, region zaangażowany w myślenie, emocje i kontrolę funkcji automatycznych organizmu. Ta część czołowa jest połączona z głębszym obszarem zwanym podbrzeżnym przednim zakrętem obręczy oraz, poprzez ścieżki nerwowe w tym nerw błędny, z sercem. Gdy ten obwód jest stymulowany, serce może chwilowo zwolnić, a następnie wrócić do normy — efekt, który może wskazywać, że „oś serce–mózg” została skutecznie zaangażowana. Neuro-kardio-kierowany TMS (NCG-TMS) próbuje wykorzystać te szybkie zmiany tętna jako fizjologiczny kompas do wyboru najbardziej efektywnych miejsc stymulacji.
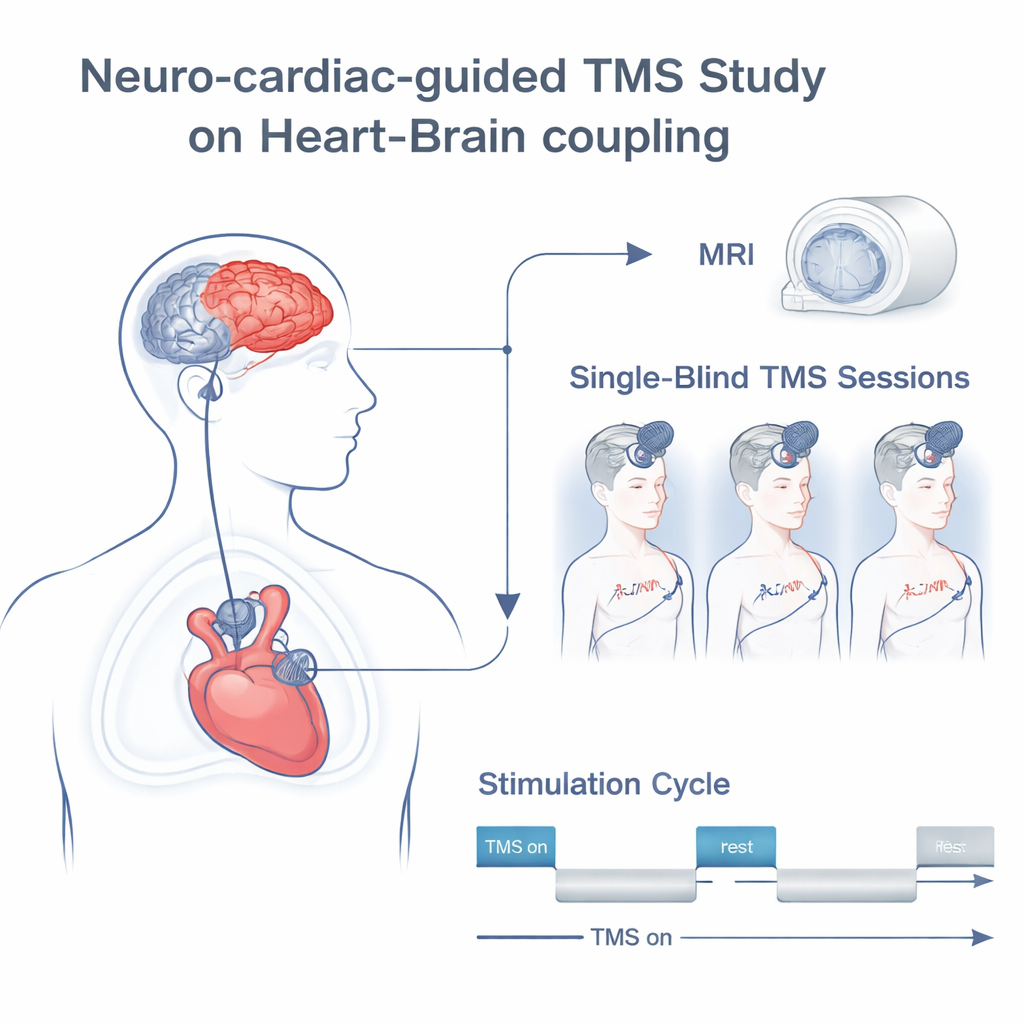
Wnętrze eksperymentu na zdrowych ochotnikach
Naukowcy przetestowali udoskonalony protokół „NCG-TMS 2.0” na 19 zdrowych dorosłych w trakcie trzech osobnych wizyt. Najpierw każda osoba przeszła skan mózgu, aby zmapować anatomię i precyzyjnie zlokalizować kilka nieco różnych punktów w lewej korze czołowej wokół standardowej pozycji F3 używanej w klinikach. Podczas późniejszych sesji zespół stosował rytmiczny rTMS o częstotliwości 10 Hz w krótkich seriach, z stopniowo rosnącą intensywnością, jednocześnie rejestrując elektrokardiogram, aby śledzić zmiany międzyskurczowe w aktywności serca. Porównano sześć aktywnych celów czołowych i warunek pozorowany (sham), w którym procedura naśladowała TMS bez dostarczania skutecznej stymulacji. Aby uchwycić, jak mocno serce podążało za rytmem stymulacji, mierzono „sprzężenie serce–mózg” (HBC) — zasadniczo siłę zmian tętna związanych z wzorem włączania i wyłączania pociągów TMS.
Znajdowanie najlepszych punktów na płacie czołowym
Używając zaawansowanych modeli statystycznych, zespół zbadał, jak HBC zależało od miejsca stymulacji, intensywności i efektów ubocznych, takich jak ból czy drgania mięśni. Okazało się, że zależność nie była prosta — „mocniejsze impulsy dają silniejsze efekty.” Zamiast tego HBC zmieniało się nieliniowo w zależności od intensywności i mocno zależało od umiejscowienia cewki. Kilka miejsc czołowych wokół F3 wykazywało wyraźnie silniejsze sprzężenie serce–mózg niż sham, a pozycje boczne i tylne wyróżniały się szczególnie dużymi wzrostami. Przy wyższych intensywnościach te miejsca wywoływały reakcje serca wielokrotnie silniejsze niż obserwowane w warunku sham lub przy powszechnie stosowanym celu według „reguły 5 cm”. Efekty uboczne miały znaczenie — łagodny dyskomfort mógł zwiększać reakcje serca, podczas gdy silniejsze efekty uboczne miały tendencję do ich tłumienia — ale nie wyjaśniały w pełni zaobserwowanego wzorca. Wspiera to ideę, że zaobserwowane zmiany były napędzane autentyczną komunikacją mózg–serce, a nie tylko bólem.
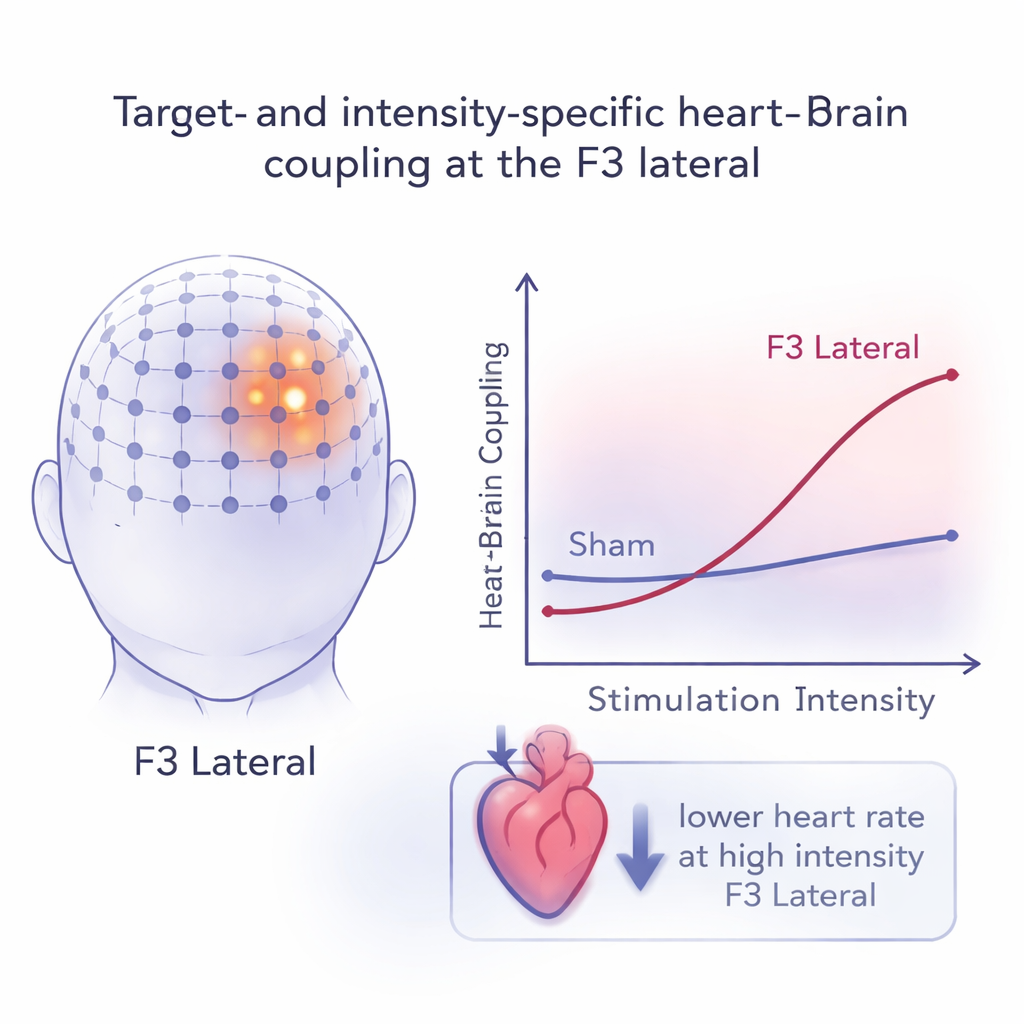
Powtarzalność w czasie i kierunek zmiany tętna
Aby każdy biomarker był użyteczny w terapii, musi być stosunkowo stabilny między sesjami. Badacze ocenili powtarzalność, porównując sprzężenie serce–mózg w trzech wizytach. Większość celów czołowych wykazywała znaczne zmienności, ale miejsca F3 boczne i F3 przednie wykazywały umiarkowaną do wysokiej spójność, zwłaszcza przy wyższych intensywnościach stymulacji i między drugą a trzecią wizytą. Gdy zespół spojrzał na kierunek zmiany — czy serce przyspieszało, czy zwalniało — stwierdzono, że w różnych warunkach przesunięcia tętna były małe (w granicach około dwóch uderzeń na minutę). Jednak wyraźny wzorzec się pojawił: stymulacja o dużej intensywności w miejscu F3 bocznym konsekwentnie prowadziła do niewielkiego, lecz stałego zwolnienia serca, co zgadza się z ideą, że to miejsce mocno angażuje uspokajającą, błędną (wagalną) stronę autonomicznego układu nerwowego.
Co to oznacza dla przyszłych terapii depresji
Dla osoby niebędącej specjalistą główne przesłanie jest takie: nie każda „frontalna TMS” jest taka sama. Badanie pokazuje, że niewielkie przesunięcia pozycji cewki na lewej skroni i staranne kontrolowanie siły stymulacji mogą sprawić, że serce odpowie zupełnie inaczej. Pozycja boczna bliska tradycyjnej lokalizacji F3 wyłoniła się jako szczególnie obiecujący cel: silnie i niezawodnie łączyła stymulację mózgu ze zwolnieniem tętna, nawet po uwzględnieniu efektów ubocznych. Choć eksperymenty przeprowadzono na zdrowych ochotnikach i nie mierzono długoterminowych zmian nastroju, wytyczają one potencjalną mapę drogową. Wykorzystując informację zwrotną z serca w czasie rzeczywistym jako biologiczny przewodnik, klinicyści mogą pewnego dnia dostroić cele i dawki TMS dla każdej osoby, co może poprawić wyniki leczenia u pacjentów z depresją, u których komunikacja mózg–serce jest zakłócona.
Cytowanie: Feng, ZJ., Martin, S., Numssen, O. et al. Target-Specificity and repeatability in neuro-cardiac-guided TMS for heart-brain coupling. Transl Psychiatry 16, 79 (2026). https://doi.org/10.1038/s41398-026-03879-w
Słowa kluczowe: przezczaszkowa stymulacja magnetyczna, sprzężenie serce–mózg, leczenie depresji, autonomiczny układ nerwowy, spersonalizowana neuromodulacja