Clear Sky Science · pl
Obrazowanie funkcjonalne hamowania hydrolazy amidów kwasów tłuszczowych w zaburzeniu stresowym pourazowym: randomizowane badanie kliniczne
Dlaczego chemia mózgu ma znaczenie dla powrotu po traumie
Wiele osób, które doświadczyły traumy, rozwija zaburzenie stresowe pourazowe (PTSD) — stan charakteryzujący się koszmarami, nawracającymi flashbackami i stałym napięciem. Najsilniej udokumentowane terapie to formy terapii poznawczo-behawioralnej oparte na kontrolowanym, bezpiecznym wystawieniu na wspomnienia traumatyczne, które pomagają mózgowi nauczyć się, że przeszłe zagrożenie już nie istnieje. Naukowcy liczyli, że dodanie leku zwiększającego poziom własnych, uspokajających, przypominających kannabinoidy substancji mózgowych może ułatwić to uczenie się i uczynić terapię bardziej skuteczną. To badanie poddało tę ideę rygorystycznej weryfikacji i dodatkowo zajrzało do wnętrza mózgu, aby zobaczyć, co rzeczywiście się dzieje.
Nadzieja z „kannabinoidowego” systemu mózgu
Organizm wytwarza własne substancje podobne do kannabinoidów, zwane endokannabinoidami, które pomagają regulować stres, lęk i uczenie się emocjonalne. Jednym z nich, anandamidem, wydaje się szczególnie ważny dla „wygaszania lęku” — procesu uczenia się, że sygnał wcześniej zwiastujący zagrożenie jest teraz bezpieczny. U zwierząt i zdrowych ochotników podnoszenie poziomu anandamidu poprawia to uczenie się bezpieczeństwa i osłabia reakcje na stres. Kluczowy enzym, hydrolaza amidów kwasów tłuszczowych (FAAH), rozkłada anandamid. Blokowanie FAAH lekiem podnosi stężenie anandamidu w organizmie i, jak przypuszczano, w obszarach mózgu kontrolujących lęk i emocje.
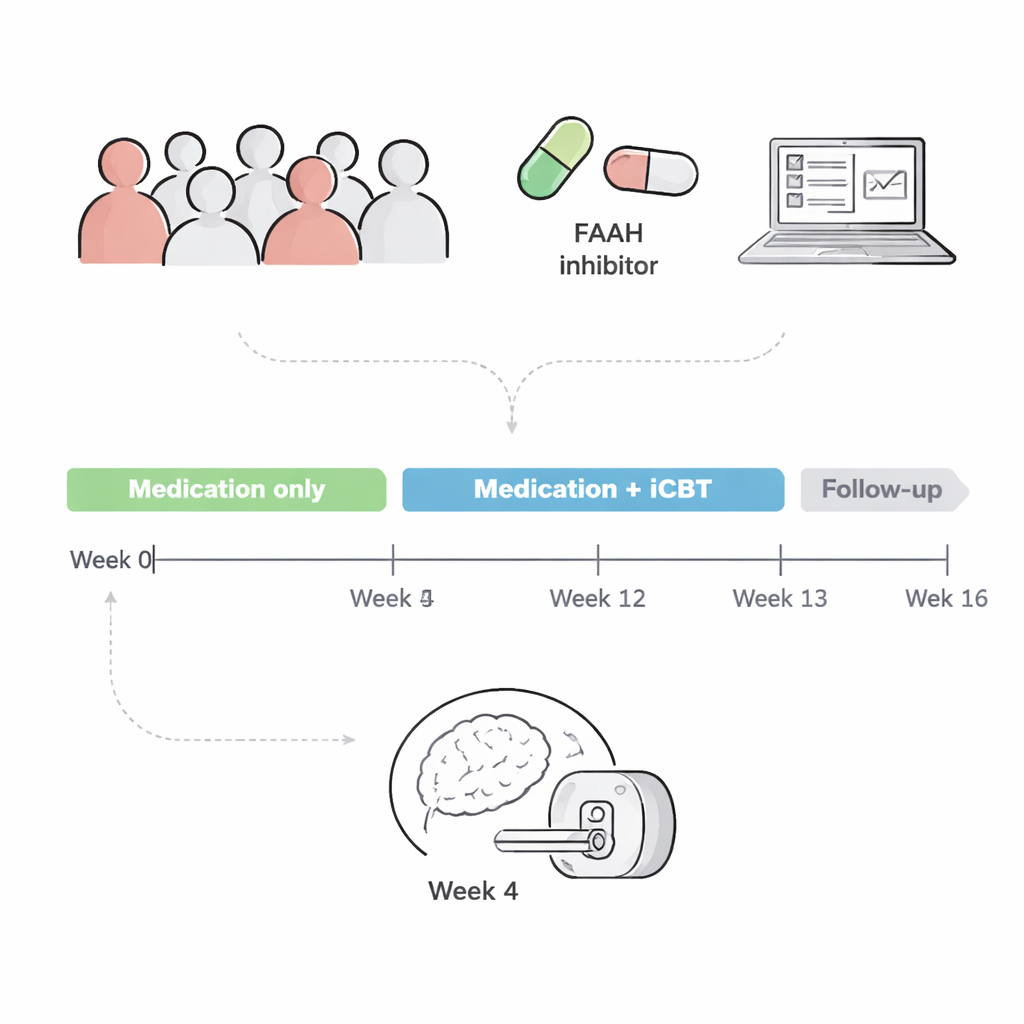
W oparciu o te przesłanki zespół przeprowadził podwójnie ślepą, randomizowaną próbę kliniczną u 100 dorosłych z PTSD. Przez 12 tygodni uczestnicy otrzymywali albo lek blokujący FAAH, albo placebo, a po 4 tygodniach wszyscy rozpoczęli internetowy program terapii poznawczo-behawioralnej (iCBT) skoncentrowany na traumie. Wcześniejsze raporty z tej próby wykazały, że wbrew oczekiwaniom inhibitor FAAH nie zmniejszał objawów PTSD bardziej niż placebo w czasie leczenia. Niniejszy artykuł zagląda w skany mózgu, aby zapytać: czy lek przynajmniej zmienił aktywność mózgu lub komunikację między kluczowymi obszarami emocjonalnymi, nawet jeśli objawy się nie poprawiły?
Zaglądanie w mózgi w spoczynku i podczas emocji
Siedemdziesięciu sześciu uczestników przeszło funkcjonalne MRI po 4 tygodniach przyjmowania leku lub placebo, tuż przed rozpoczęciem terapii. Badacze zebrali dwa rodzaje danych mózgowych. Po pierwsze, skan „stanu spoczynkowego” mierzył, jak silnie aktywność różnych obszarów mózgu współzmieniała się ze sobą, co wskazuje na ich funkcjonalne powiązanie. Po drugie, podczas zadania „konfliktu emocjonalnego” uczestnicy oglądali twarze i słowa opisujące emocje, które czasem pasowały do siebie, a czasem się ze sobą ścierały — coś w rodzaju emocjonalnej wersji testu Stroopa. To zadanie wcześniej wiązano z tym, jak dobrze ludzie reagują na terapię PTSD.
Zespół skupił się na sieci długo powiązanej z PTSD: ciałku migdałowatym (amygdala), które wykrywa zagrożenie i emocjonalne znaczenie; przyśrodkowej części kory przedczołowej brzuszno-przyśrodkowej (vmPFC), zaangażowanej w uczenie się bezpieczeństwa i regulację emocji; oraz grzbietowo-bocznej kory przedczołowej (dlPFC), związanej z wysiłkową kontrolą i radzeniem sobie. Badano także obszar zwany przednią wyspą (anterior insula), który integruje odczucia z ciała z stanami emocjonalnymi. Łącząc miary z mózgu z ocenami PTSD wykonywanymi przez klinicystów oraz samoopisami pacjentów, badacze szukali wzorców wyróżniających osoby, które poprawiły się bardziej w trakcie próby.
Co uległo zmianie w mózgu — a co nie
Lek blokujący FAAH ewidentnie wykonał swoje zadanie biochemiczne: poziomy anandamidu we krwi były wyższe u osób, które go otrzymały. Jednak przy porównaniu grupy przyjmującej lek z grupą placebo nie stwierdzono istotnych różnic w łączności w spoczynku ani w aktywacji mózgu podczas zadania. Oczekiwane wzmocnienie obwodów związanych z lękiem i emocjami po prostu nie pojawiło się w skanach. Zamiast tego wyłoniły się inne wzorce powiązane z ciężkością objawów i stopniem poprawy w czasie, niezależnie od tego, którą pigułkę ktoś brał.
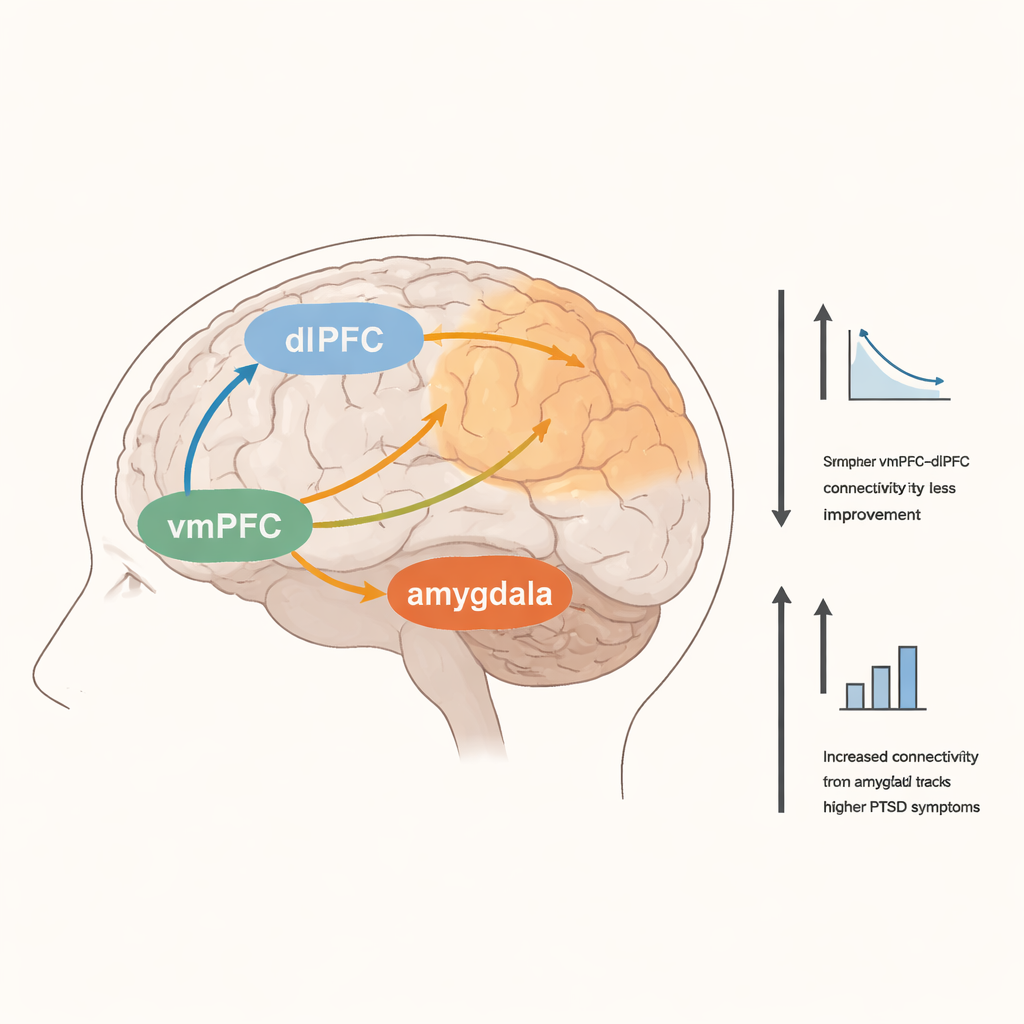
Osoby zgłaszające silniejsze objawy PTSD w chwili skanowania wykazywały silniejsze funkcjonalne połączenia między vmPFC a szeroko rozproszonymi obszarami związanymi z uwagą oraz między amygdalą a rejonami zaangażowanymi w odbieranie i poruszanie ciałem. Silniejsze powiązania między vmPFC a przednią wyspą również wiązały się z wyższymi samoopisanymi objawami. Co ciekawe, większa poprawa kliniczna w ciągu pełnych 12 tygodni próby była związana z niższą aktywacją prawej dlPFC podczas zadania konfliktu emocjonalnego oraz ze słabszą łącznością w spoczynku między vmPFC a tą samą okolicą dlPFC. Sugeruje to, że pacjenci, którzy ostatecznie lepiej się czuli, mogli polegać mniej na wysiłkowej, wysokopoziomowej kontroli, a bardziej na innych, być może bardziej automatycznych formach przetwarzania emocjonalnego.
Co to znaczy dla przyszłych terapii PTSD
Główne przesłanie w codziennym ujęciu jest takie: samo podniesienie jednego z własnych, przypominających kannabinoidy związków mózgowych — anandamidu — nie wystarczyło, by poprawić efekty terapii lub przekształcić kluczowe obwody lęku i emocji u osób z PTSD, przynajmniej w tej w większości kobiecej, niebojowej próbie. Badanie wskazuje jednak dlPFC jako możliwy marker tego, kto ma większe szanse skorzystać z terapii opartej na ekspozycji, i podkreśla, że PTSD wiąże się z szerokimi zmianami w sposobie, w jaki sieci uwagi i emocji ze sobą rozmawiają. Dla pacjentów i klinicystów wyniki te przypominają, że obiecujące wnioski z badań na zwierzętach i wstępnych badań z ludźmi nie zawsze przekładają się bezpośrednio na skuteczne terapie, oraz że zrozumienie złożonej reakcji mózgu na traumę wymaga patrzenia poza pojedyncze związki chemiczne — ku wzorcom obejmującym cały mózg i różnice indywidualne.
Cytowanie: Tansey, R., Perini, I., Petrie, G.N. et al. Functional neuroimaging of fatty acid amide hydrolase inhibition in posttraumatic stress disorder: a randomized clinical trial. Transl Psychiatry 16, 95 (2026). https://doi.org/10.1038/s41398-026-03864-3
Słowa kluczowe: PTSD, endokannabinoidy, inhibitor FAAH, funkcjonalny rezonans magnetyczny, wygaszanie lęku