Clear Sky Science · pl
Biologiczne podstawy i predyspozycja genetyczna do schizofrenii w szlakach regulacyjnych mikroRNA-137 w przebiegu rozwoju mózgu
Jak mała cząsteczka może kształtować ryzyko schizofrenii
Schizofrenia często bywa postrzegana jako tajemnicze zaburzenie mózgu ujawniające się w późnym okresie dojrzewania lub we wczesnej dorosłości, ale jej korzenie mogą sięgać jeszcze przed narodzeniem. Ten artykuł bada, jak mała cząsteczka regulacyjna zwana microRNA-137 (miR-137) może wpływać na rozwój i komunikację komórek mózgowych, kształtując zarówno prawdopodobieństwo rozwoju schizofrenii, jak i rodzaje występujących objawów. Śledząc efekty miR-137 od mózgu prenatalnego aż do dorosłości, badacze starają się wyjaśnić, dlaczego niektórzy ludzie są bardziej podatni na psychozę i powiązane choroby psychiczne.
Mały regulator o dużym znaczeniu
MiR-137 to krótki fragment RNA, który sam w sobie nie koduje białek, lecz działa jako regulator wielu innych genów. Pomaga decydować, kiedy i z jaką siłą wiele genów związanych z mózgiem jest włączanych lub wyłączanych. Wcześniejsze badania genetyczne wykazały, że powszechne warianty w pobliżu genu MIR137 są jednymi z najsilniejszych znanych czynników ryzyka dla schizofrenii. Wiele genów będących pod kontrolą miR-137 bierze udział w budowie neuronów, kształtowaniu ich wypustek i tworzeniu synaps — miejsc, przez które komórki mózgowe się komunikują. Jednak większość wcześniejszych prac opierała się na przewidywaniach komputerowych lub uproszczonych modelach komórkowych, które mogą nie uchwycić faktu, że miR-137 może działać inaczej na różnych etapach rozwoju mózgu i w różnych regionach mózgu.
Sprawdzając bezpośrednio w ludzkim mózgu
Aby uzyskać bardziej realistyczny obraz, autorzy skupili się na „bezpośrednich celach” miR-137 zidentyfikowanych w rzeczywistej tkance mózgowej przy użyciu metody fizycznie mapującej miejsca wiązania miRNA z ich genami docelowymi. Połączyli dane z dwóch kluczowych okresów: wczesnego rozwoju prenatalnego oraz dorosłości. Pozwoliło to na zbudowanie dwóch odrębnych zestawów genów: grupy celów prenatalnych i grupy celów dorosłych. Następnie porównali je z kilkoma bardziej tradycyjnymi zestawami pochodzącymi z narzędzi predykcyjnych lub z eksperymentów na komórkach. Przy użyciu różnych metod statystycznych zbadali, jak każdy zestaw genów był ekspresjonowany w różnych regionach mózgu i etapach życia, w jakich typach komórek się pojawiał oraz jak silnie pokrywał się z genetycznym ryzykiem schizofrenii i powiązanych schorzeń.
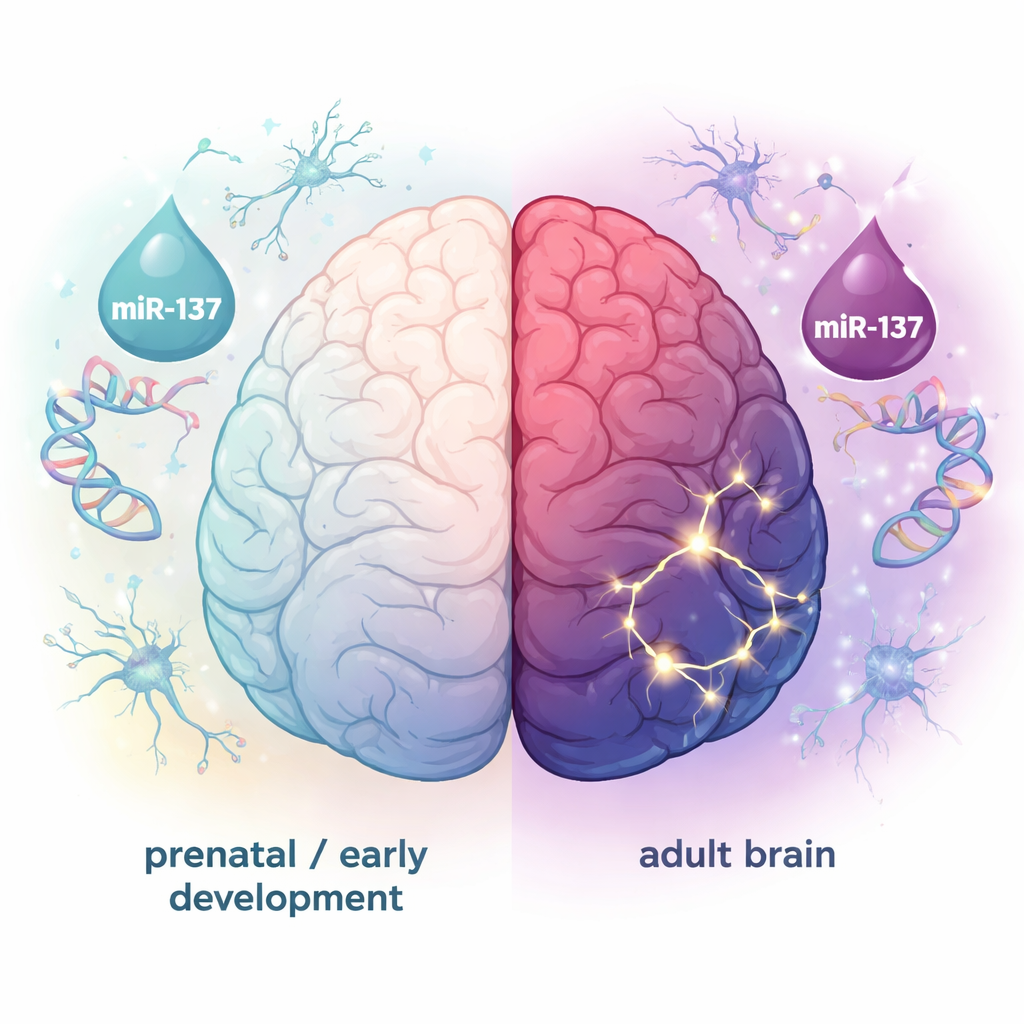
Różne etapy, różne zadania w mózgu
Zestawy celów miR-137 w okresie prenatalnym i dorosłym okazały się w dużej mierze odrębne, dzieląc tylko niewielką liczbę genów. Cele prenatalne były najsilniej powiązane z wczesnymi zadaniami budowy mózgu, takimi jak generowanie nowych neuronów i komórek glejowych oraz kierowanie ich początkowym rozwojem. Ich aktywność była relatywnie wysoka we wczesnym życiu, a następnie malała, z zauważalnym wyjątkiem w móżdżku dorosłych. Natomiast cele dorosłe były wzbogacone o geny uczestniczące w funkcjach synaptycznych, wypustkach neuronów i komunikacji międzykomórkowej. Te geny były wysoce aktywne w wielu rejonach mózgu dorosłych, szczególnie w neuronach i oligodendrocytach, a ich ekspresja miała tendencję do szczytowania we wczesnej dorosłości — w czasie, gdy schizofrenia często po raz pierwszy się pojawia. Inne, szerzej przewidywane zestawy genów nie wykazywały tak wyraźnego wzorca zależnego od etapu rozwoju i typu komórek.
Łączenie regulacji genów z chorobą i objawami
Porównując osoby ze schizofrenią z osobami bez zaburzenia, zespół odkrył, że wiele dorosłych genów będących celami miR-137 było konsekwentnie mniej aktywnych w tkance mózgowej pacjentów. Podobne obniżenia zauważono w chorobie afektywnej dwubiegunowej i autyzmie, co sugeruje wspólny sygnaturowy wzorzec molekularny w głównych chorobach psychiatrycznych. Analizy genetyczne potwierdziły ten wzorzec: zarówno cele prenatalne, jak i dorosłe miR-137 nosiły niezwykle wysokie obciążenie powszechnymi wariantami ryzyka dla schizofrenii, a cele dorosłe również obejmowały wspólne ryzyko genetyczne rozciągające się na schizofrenię, chorobę afektywną dwubiegunową, depresję i autyzm. Co ważne, gdy badacze obliczyli poligeniczne wyniki ograniczone do tych genów celów w dużej hiszpańskiej próbce, wyniki oparte na celach dorosłych pomagały odróżnić pacjentów od kontroli, podczas gdy wyniki oparte na celach prenatalnych były szczególnie powiązane z nasilením objawów „negatywnych”, takich jak spłycenie afektu, brak motywacji i wycofanie społeczne.
Co to oznacza dla rozumienia schizofrenii
Dla osób niebędących specjalistami, główny wniosek jest taki, że miR-137 nie działa jako prosty włącznik/wyłącznik schizofrenii, lecz jako część ruchomej tablicy kontrolnej, której wpływ zmienia się od życia prenatalnego do dorosłości. We wczesnym rozwoju miR-137 wydaje się kształtować podstawowy układ obwodów mózgowych, a dziedziczne warianty w jego prenatalnych celach mogą predysponować niektóre osoby do silniejszych objawów negatywnych w późniejszym życiu. W mózgu dorosłym cele miR-137 skupiają się w synapsach i szlakach komunikacyjnych, które są genetycznie współdzielone przez kilka zaburzeń psychiatrycznych. Skupiając się na bezpośrednich, specyficznych czasowo celach w ludzkiej tkance mózgowej, ta praca wyostrza nasze spojrzenie na to, jak jedna ścieżka regulacyjna może przyczyniać się zarówno do ryzyka psychozy, jak i do specyficznego sposobu jej przejawu, otwierając możliwości bardziej ukierunkowanej prewencji i terapii.
Cytowanie: Stella, C., De Hoyos, L., Mora, A. et al. Biological underpinnings and genetic predisposition to schizophrenia within microrna-137 regulatory pathways across brain development. Transl Psychiatry 16, 91 (2026). https://doi.org/10.1038/s41398-026-03859-0
Słowa kluczowe: schizofrenia, microRNA-137, rozwój mózgu, ryzyko genetyczne, funkcja synaptyczna