Clear Sky Science · pl
Zmiana m6A zależna od METTL3 reguluje CDKN1A, łagodząc upośledzenie pamięci i apoptozę neuronów wywołane przewlekłym niedoborem snu u szczurów
Dlaczego bezsenne noce mogą szkodzić pamięci
Wielu ludzi lekceważy przewlekły brak snu jako normalny element współczesnego życia, ale badania pokazują, że utrata snu może potajemnie uszkadzać obszary mózgu odpowiedzialne za uczenie się i pamięć. To badanie na szczurach zagląda na poziomie pojedynczych molekuł w neuronach hipokampa i identyfikuje konkretny przełącznik chemiczny — METTL3 — który wydaje się chronić komórki mózgowe przed szkodliwymi skutkami przewlekłego pozbawienia snu. Zrozumienie tego mechanizmu może w przyszłości wskazać nowe sposoby ochrony pamięci u osób, które nie mogą łatwo uniknąć utraty snu, takich jak pracownicy zmianowi, opiekunowie czy pacjenci z zaburzeniami snu.
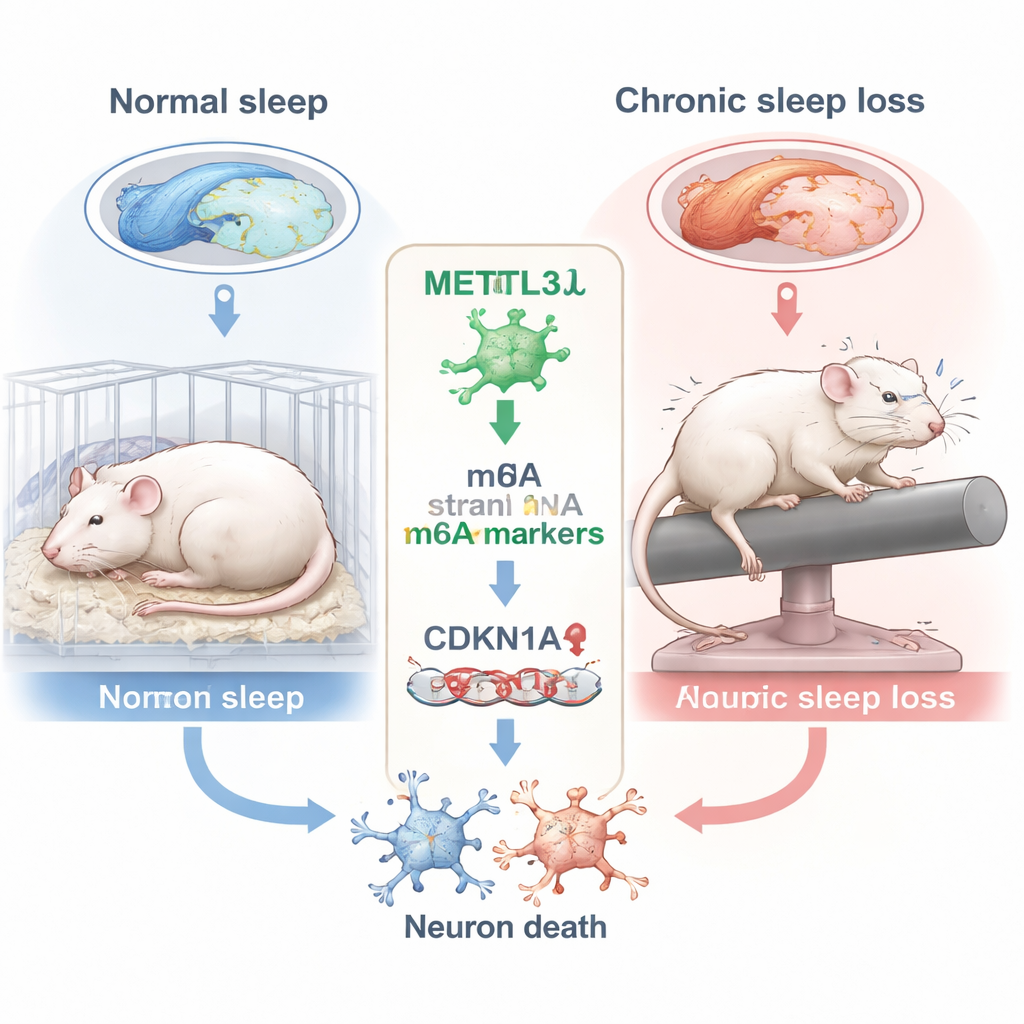
Jak długotrwały brak snu uszkadza centrum pamięci
Naukowcy skupili się na hipokampie, regionie mózgu o kształcie morskiego konika, niezbędnym do tworzenia nowych wspomnień. W hipokampie przyjrzeli się podobszarowi CA3, który pomaga kodować i odzyskiwać informacje przestrzenne — umiejętności testowane w zadaniach takich jak odnalezienie ukrytej platformy w wodzie. Szczury utrzymywano przytomne przez 10 godzin dziennie przez sześć tygodni za pomocą łagodnego obracającego się wałka, który wielokrotnie budził zwierzęta. W teście znanym jako Morris Water Maze szczury pozbawione snu wybierały mniej bezpośrednie trasy, rzadziej przecinały miejsce, w którym wcześniej znajdowała się platforma, i spędzały mniej czasu w docelowym kwadrancie — wszystkie te objawy wskazywały na upośledzenie pamięci przestrzennej w porównaniu z wypoczętymi zwierzętami.
Chemiczna etykieta na RNA, która zanika
Aby zrozumieć, co działo się wewnątrz neuronów CA3, zespół przeanalizował chemiczny znak na RNA zwany m6A, jeden z najczęstszych wewnętrznych znaczników na mRNA. Te znaki pomagają kontrolować czas życia cząsteczek RNA i efektywność ich wykorzystania do produkcji białek. Kluczowym enzymem dodającym markery m6A jest METTL3. Przy użyciu wysokoprzepustowego sekwencjonowania m6A i analizy ekspresji genów naukowcy stwierdzili, że przewlekły brak snu znacząco obniża poziom METTL3 w rejonie CA3. Spadek ten potwierdzono zarówno na poziomie RNA, jak i białka. Wzorzec dotkniętych genów sugerował zaburzenia kontroli cyklu komórkowego i odpowiedzi na stres, co wskazuje, że utrata snu może popychać neurony w kierunku stanów niezdrowych.
Od zmiany molekularnej do śmierci neuronu
Aby sprawdzić, jak obniżenie METTL3 może bezpośrednio wpływać na neurony, badacze użyli hodowanych w naczyniach komórek hipokampa mysiego. Kiedy zastosowali małe interferujące RNA do wyciszenia METTL3, komórki stały się znacznie bardziej podatne na uszkodzenia wywołane rapamycyną, lekiem stresującym neurony. Komórki pozbawione METTL3 wykazywały podwyższone poziomy klasycznych białek „samobójstwa komórkowego”, takich jak Bax i pocięty kaspaza-3, a większa liczba komórek została oznaczona jako apoptotyczna w cytometrii przepływowej. Głębsze analizy RNA wskazały na pojedynczy gen, CDKN1A (kodujący białko p21), jako kluczowego gracza: po wyciszeniu METTL3 poziomy CDKN1A gwałtownie wzrosły.
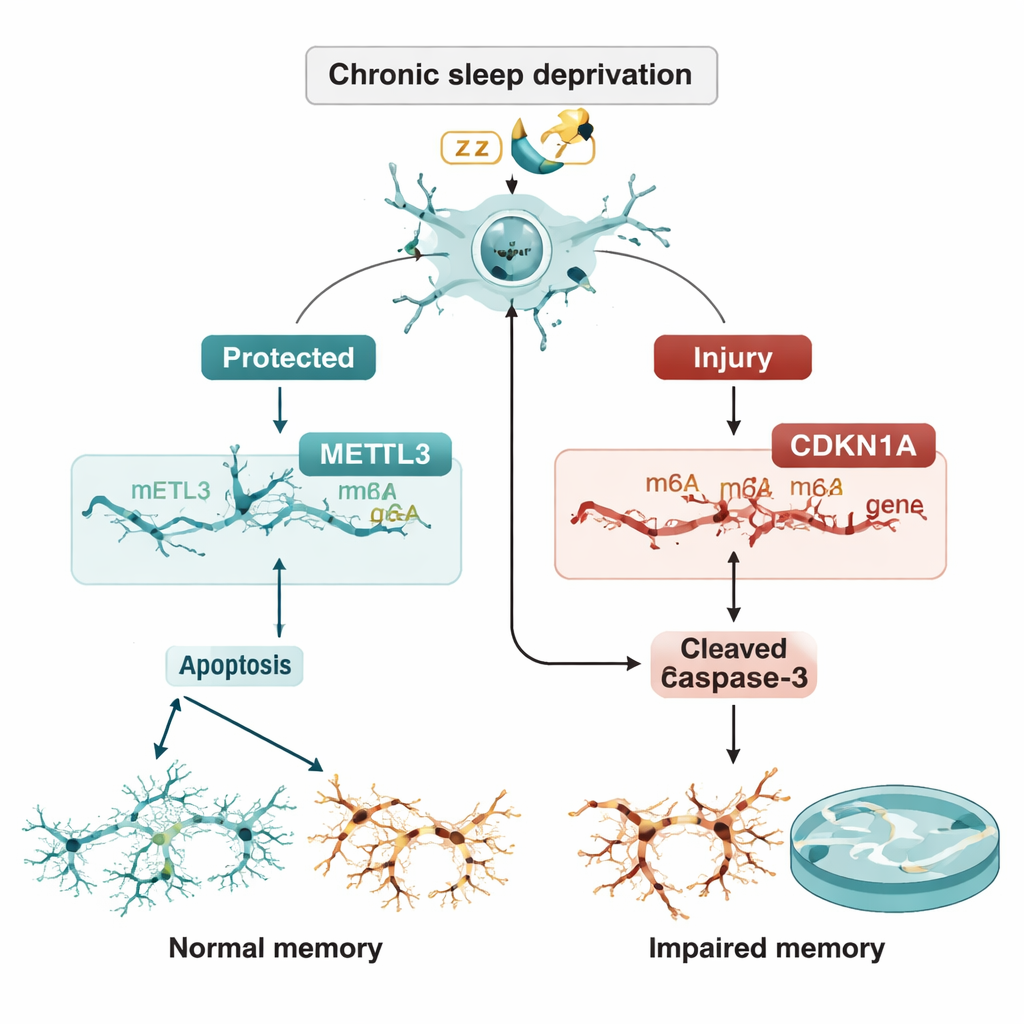
Kruchy balans między ochroną a autodestrukcją
Zespół następnie zapytał, czy METTL3 kontroluje CDKN1A poprzez znakowanie m6A. Wykazali, że redukcja METTL3 obniżała oznakowanie m6A na RNA CDKN1A i sprawiała, że to RNA stawało się bardziej stabilne, więc jego poziom narastał zamiast być rozkładanym. Wyższe poziomy CDKN1A z kolei kierowały neurony w stronę apoptozy. Co ważne, gdy sam CDKN1A został wyciszony, dodatkowa śmierć komórek spowodowana utratą METTL3 została w dużej mierze odwrócona. U żywych szczurów dostarczenie dodatkowego METTL3 bezpośrednio do rejonu CA3 za pomocą wektora wirusowego obniżyło poziomy CDKN1A, zmniejszyło obfitość białek apoptozy, zachowało strukturę neuronów w barwieniach tkankowych i poprawiło wyniki w teście wodnym, mimo trwającego niedoboru snu.
Co to oznacza dla osób, które nie śpią wystarczająco
Mówiąc krótko, przewlekły niedobór snu wydaje się tłumić ochronny enzym METTL3 w krytycznym obwodzie pamięci mózgu. Gdy METTL3 spada, nie może on właściwie oznaczać pewnych RNA, szczególnie tego kodującego CDKN1A. To RNA następnie gromadzi się, popychając neurony do zaprogramowanej śmierci i przyczyniając się do problemów z pamięcią. Przywrócenie METTL3 pozwoliło badaczom obniżyć CDKN1A, zmniejszyć utratę neuronów i przywrócić pamięć u szczurów pozbawionych snu. Choć prace te są nadal na etapie badań na zwierzętach, identyfikują szlak METTL3–CDKN1A jako obiecujący cel dla przyszłych leków mających chronić mózg przed poznawczymi skutkami przewlekłego braku snu.
Cytowanie: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Słowa kluczowe: przewlekły niedobór snu, hipokamp, metylacja RNA, apoptoza neuronów, upośledzenie pamięci