Clear Sky Science · pl
Różnorodne i specyficzne dla lokalizacji role PlexinA2, PlexinA4 i NCAM w rozwijających się włóknach mchu hipokampa
Jak ścieżki nerwowe kształtują obwody pamięci
Hipokamp, obszar mózgu kluczowy dla tworzenia i odtwarzania wspomnień, jest łączał przez drobne włókna nerwowe, które w okresie wczesnego rozwoju muszą nawigować bardzo precyzyjnie. W tym badaniu stawiane jest pozornie proste pytanie: jak rosnące włókna wiedzą dokładnie, dokąd mają zmierzać — i co się dzieje, gdy ich system wskazówek zawodzi, potencjalnie przyczyniając się do takich schorzeń jak schizofrenia, autyzm czy padaczka?
Dwie autostrady do centra pamięci
W hipokampie komórki nerwowe w rejonie zwanym zakrętem zębatym wysyłają długie włókna, znane jako włókna mchu, w kierunku innego obszaru zwanego CA3. Wchodząc do CA3, włókna te zwykle rozdzielają się na dwie odrębne „autostrady”: jedną biegnącą nad warstwą ciał komórek CA3 i drugą poniżej niej. Każda z tych dróg łączy się z różnymi częściami komórek CA3 i pomaga ustalić równowagę aktywności w tym obwodzie pamięci. Jeśli te szlaki nie rozdzielą się prawidłowo, włókna mogą znaleźć się w niewłaściwym miejscu, co może zaburzać przepływ informacji przez hipokamp.
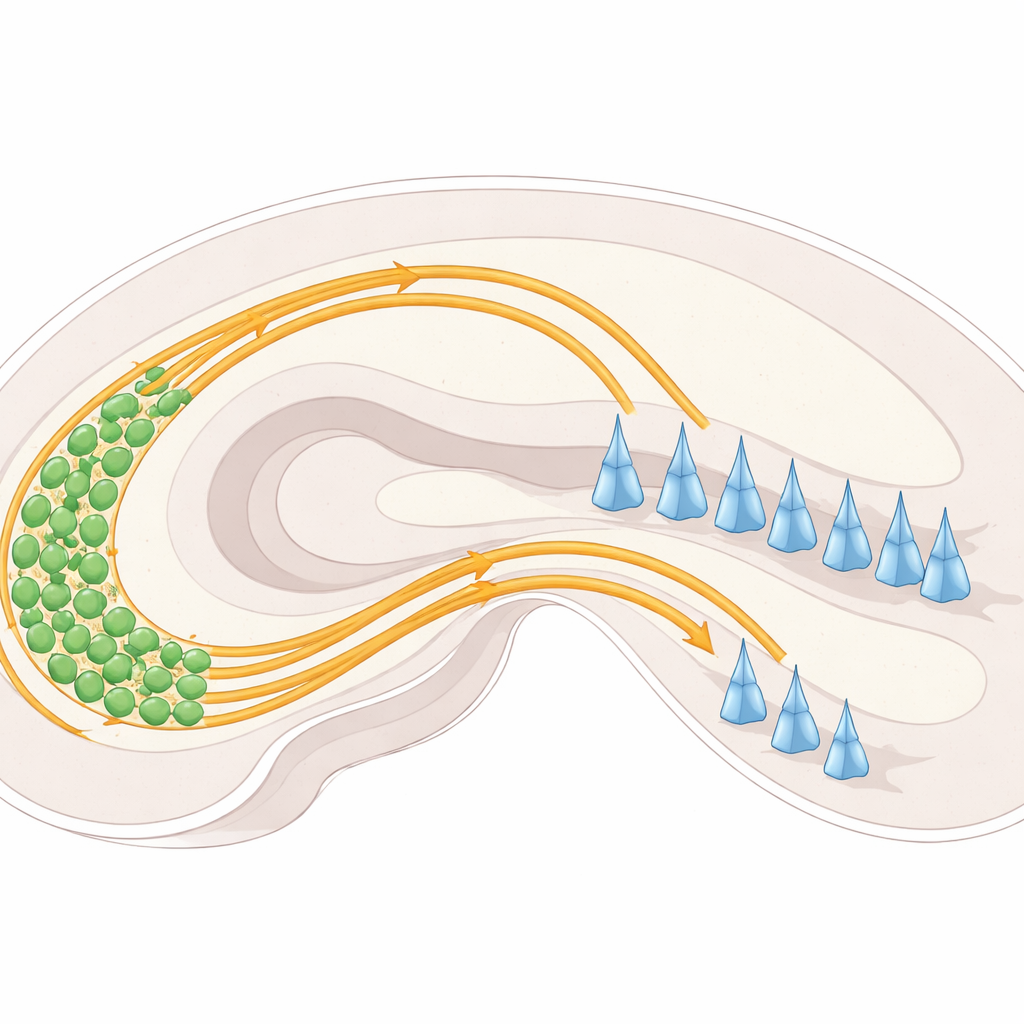
Wskazówki prowadzenia: pchnięcia, przyciągania i uchwyty międzykomórkowe
Naukowcy skupili się na zestawie molekularnych znaków i powierzchniowych „uchwytów” na komórkach nerwowych, które kierują włóknami mchu. Rodzina białek zwana plexynami (PlexinA2 i PlexinA4) znajduje się na powierzchni komórek nerwowych i reaguje z partnerami znanymi jako semaforyny, zwłaszcza Sema6A. Te interakcje mogą działać jak sygnały „wstęp wzbroniony”, odsuwając włókna od określonych obszarów, albo precyzować, jak mocno sąsiednie włókna do siebie przylegają. Inne białko powierzchniowe, NCAM, zachowuje się bardziej jak rzep, promując adhezję i pomagając wiązkom włókien utrzymać spójność. Badając, gdzie te białka są wyrażane i co się dzieje, gdy są usuwane lub modyfikowane u myszy, zespół opracował mapę ich współdziałania w żywym mózgu, zamiast jedynie w izolowanych komórkach.
Rozdzielanie ról za pomocą zaprojektowanych myszy
Aby rozpoznać rolę każdego składnika, naukowcy stworzyli i zestawili 27 różnych linii myszy. Niektóre nie miały w ogóle Sema6A, inne pozbawione były PlexinA2 albo PlexinA4, a jeszcze inne nosiły subtelne mutacje punktowe wyłączające tylko konkretną „jądrową” część enzymatyczną plexyn, pozostawiając resztę cząsteczki nienaruszoną. Usuwano także selektywnie Sema6A lub NCAM jedynie w wybranych typach komórek, takich jak komórki ziarniste zakrętu zębatego, aby sprawdzić, gdzie sygnał naprawdę ma znaczenie. U myszy pozbawionych Sema6A w tych komórkach ziarnistych włókna mchu nie dzieliły się czysto na górne i dolne pęki, a dolny pęk rósł za daleko, przekraczając swoje normalne zakończenie. Podobne, choć nie identyczne błędy połączeń zaobserwowano u myszy pozbawionych PlexinA2 lub PlexinA4, co ujawniło, że te białka działają na odrębnych punktach kontrolnych wzdłuż tej samej ścieżki.
Zbliżenie na mechanizmy i partnerstwa
Gdy autorzy wyłączyli katalityczne jądro PlexinA4, pojawiło się wiele — choć nie wszystkie — defektów obserwowanych w pełnych knockoutach PlexinA4. Pokazało to, że PlexinA4 często polega na tym rdzeniu, aby przekształcać wewnętrzny szkielet rosnących włókien nerwowych, pomagając im właściwie się zrastać i zatrzymać na odpowiedniej warstwie. PlexinA2 okazał się inny: niektóre jego role zależały od rdzenia katalitycznego, inne nie, co wskazuje na dodatkowe, niezależne od enzymu ścieżki sygnałowe. Zespół zastosował następnie technikę znakowania w pobliżu, aby zidentyfikować białka sąsiadujące z PlexinA2 w młodych neuronach hipokampa. Pojawiło się kilka molekuł adhezji komórkowej, z NCAM wyróżniającym się spośród nich. Genetycznie, jednoczesne zmniejszenie ilości PlexinA2 i NCAM powodowało silniejsze błędy trasowania włókien mchu niż zmniejszenie któregokolwiek z nich osobno, pokazując, że te dwa systemy współpracują: NCAM zapewnia adhezję, podczas gdy repulsja pochodząca z PlexinA2 kalibruje, jak włókna rozdzielają się na górne i dolne tory i jak daleko sięga dolny tor.
Gdy sygnały biegną w odwrotnym kierunku
Ciekawie, Sema6A nie działa jedynie jako zewnętrzny „znak”, który plexyny odczytują; może też pełnić funkcję odbiornika na samych włóknach mchu. Badacze analizowali myszy, u których wewnętrzny ogon Sema6A został usunięty, podczas gdy zewnętrzna część pozostała nienaruszona. U tych zwierząt niektóre defekty prowadzenia utrzymywały się — szczególnie przerost dolnego pęku — co wskazuje, że sygnały płynące do wewnątrz przez ogon Sema6A („odwrotna sygnalizacja”) są konieczne do normalnego przycinania i kształtowania włókien mchu. Ten odwrotny tryb prawdopodobnie działa obok bardziej znanej sygnalizacji opartej na plexynach w sposób zależny od etapu rozwoju i lokalizacji.
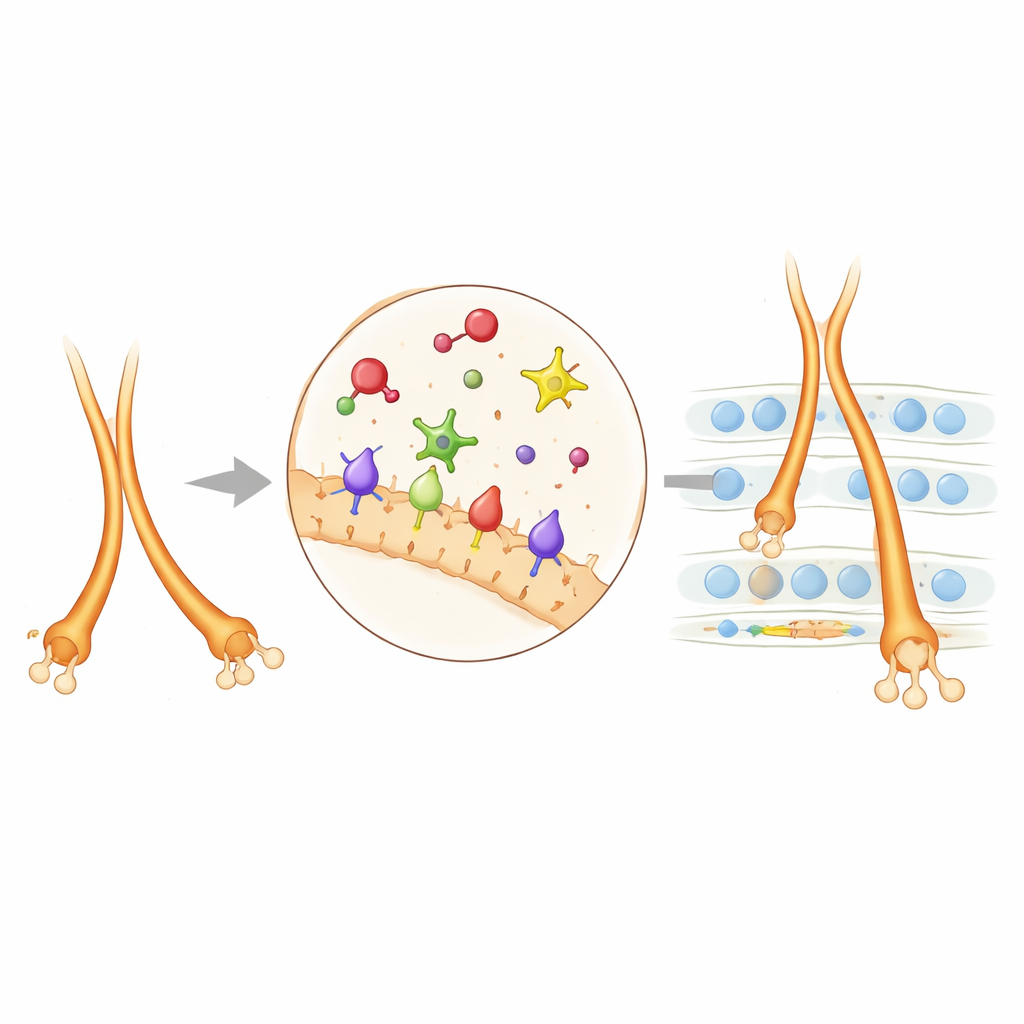
Dlaczego to okablowanie ma znaczenie dla zdrowia mózgu
Mutacje w ludzkich wersjach PLXNA2, SEMA6A i NCAM1 zostały powiązane z zaburzeniami rozwoju nerwowego i chorobami psychiatrycznymi, od niepełnosprawności intelektualnej po schizofrenię i autyzm. Pokazując, w jaki sposób te molekuły współdziałają, aby rzeźbić szlaki włókien mchu u myszy, to badanie dostarcza konkretnego modelu, jak subtelne zmiany genetyczne mogą zaburzyć tworzenie, rozdzielanie i przycinanie kluczowych obwodów pamięci. W codziennych słowach praca sugeruje, że zestaw narzędzi prowadzących mózgu wykorzystuje starannie wyważoną kombinację sygnałów „pchnięcia”, „przyciągania” i „lepkości”, aby zbudować diagram okablowania hipokampa — i że nawet niewielkie zaburzenia w tym zestawie mogą rozlać się na zmiany w uczeniu się, pamięci i zdrowiu psychicznym.
Cytowanie: Zhao, XF., Kohen, R., Van Battum, E.Y. et al. Diverse and location-specific roles of PlexinA2, PlexinA4, and NCAM in developing hippocampal mossy fibers. Transl Psychiatry 16, 126 (2026). https://doi.org/10.1038/s41398-026-03846-5
Słowa kluczowe: włókna mchu hipokampa, prowadzenie aksonów, sygnalizacja semaforyn-plexyn, NCAM i adhezja komórkowa, zaburzenia rozwoju nerwowego