Clear Sky Science · pl
Wczesne zmiany czynnościowe i stężenie GFAP w surowicy w szwedzkich rodzinach z mutacjami autosomalnie dominującej choroby Alzheimera
Dlaczego to badanie ma znaczenie dla rodzin
Choroba Alzheimera często wydaje się pojawiać nagle, ale w rzeczywistości szkodliwe zmiany w mózgu kumulują się cicho przez wiele lat. W rzadkich rodzinach noszących dziedziczne mutacje („autosomalnie dominujące”) naukowcy mogą oszacować, kiedy prawdopodobnie wystąpią objawy, i obserwować, jak rozwijają się te wczesne zmiany. W tym badaniu śledzono szwedzkie rodziny z takimi mutacjami, aby zrozumieć, jak wykorzystanie energii w mózgu, zdolności poznawcze i marker krwi związany z komórkami wspierającymi mózg (GFAP) zmieniają się na długo przed pojawieniem się problemów z pamięcią — oraz jak te zmiany różnią się między genami.
Śledzenie zegara choroby w rodzinach o wysokim ryzyku
Ponieważ u osób z autosomalnie dominującą chorobą Alzheimera (ADAD) objawy zwykle rozwijają się w dość przewidywalnym wieku, badacze mogą obliczyć „szacunkowe lata do wystąpienia objawów” (EYO) — ile lat ktoś ma do spodziewanego początku choroby lub ile już od niego minęło. Zespół badał 45 dorosłych z szwedzkich rodzin z mutacjami w genach APP lub PSEN1 oraz krewnych bez mutacji. Przez średnio ponad siedem lat uczestnicy poddawani byli badaniom obrazowym mózgu mierzącym zużycie glukozy (FDG PET), szczegółowym testom poznawczym i pamięci oraz, w części przypadków, badaniom krwi na GFAP — białko uwalniane, gdy komórki wspierające mózg zwane astrocytami stają się reaktywne. Taki układ pozwolił naukowcom uporządkować różne zmiany biologiczne wzdłuż wspólnej linii czasu choroby, zamiast jedynie porównywać osoby w jednym momencie.
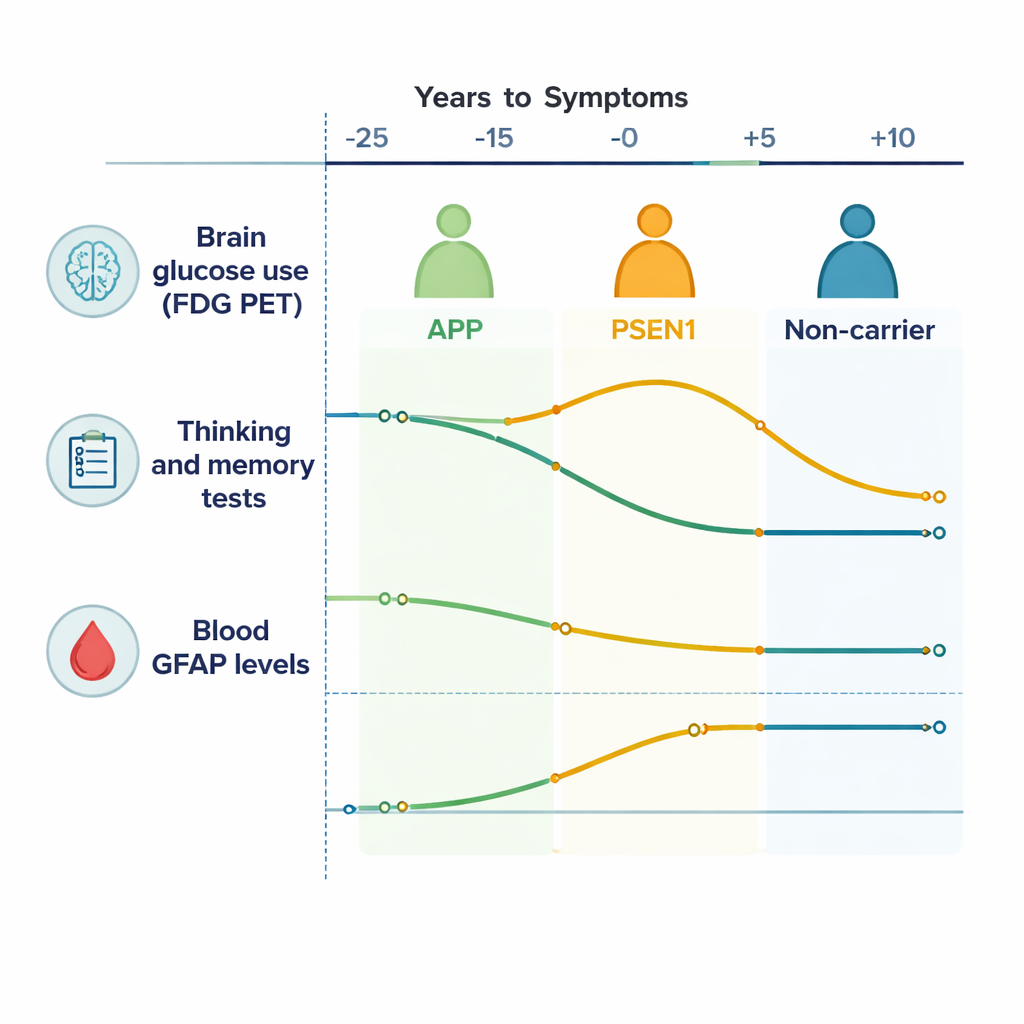
Śledzenie energii mózgu i funkcji poznawczych w czasie
W korze mózgowej osoby z mutacjami związanymi z Alzheimerem wykazywały stopniowy spadek sygnału FDG PET w porównaniu z członkami rodziny bez mutacji, co oznaczało, że ich mózgi zużywały z czasem mniej glukozy — znak pogarszania się funkcji komórek mózgowych. Obszary podkorowe głęboko w mózgu, zwłaszcza jądro ogoniaste i wzgórze, również wykazywały spadek aktywności, głównie u osób z mutacją APP. Testy myślenia i pamięci pogarszały się w kilku domenach, w tym w pamięci epizodycznej i elastyczności poznawczej, zaczynając mniej więcej 10–15 lat przed spodziewanym początkiem objawów. Innymi słowy, nawet gdy osoby nadal czuły się i funkcjonowały normalnie w codziennym życiu, wrażliwe testy i skany ujawniały, że ich mózgi już pracowały ciężej i mniej efektywnie.
Różne wzorce dla różnych genów Alzheimera
Kluczową obserwacją było to, że dwie główne grupy mutacji — APP i PSEN1 — nie podążały identycznymi ścieżkami. U nosicieli PSEN1 badacze zaobserwowali wczesny okres, około 20–10 lat przed spodziewanymi objawami, kiedy fragmenty mózgu wykazywały nietypowo wysokie zużycie glukozy („hipermetabolizm”), równocześnie z lepszymi wynikami testów, zanim później nastąpił spadek. Prawdopodobnie odzwierciedla to przejściową fazę kompensacji, w której mózg i komórki wspierające zwiększają aktywność, aby poradzić sobie z rosnącymi uszkodzeniami. Nosiciele mutacji APP wykazywali natomiast bardziej bezpośredni, stopniowy spadek metabolizmu mózgu bez tego wczesnego wzrostu. Te zależne od genu wzorce sugerują, że „choroba Alzheimera” nie jest jedną jednolitą historią biologiczną, nawet w formach dziedzicznych, lecz rodziną powiązanych procesów, które rozwijają się inaczej w zależności od konkretnej mutacji.
Co test krwi mówi o wczesnym stresie mózgu
GFAP, mierzony z prostego pobrania krwi, dostarczał wglądu w reakcję astrocytów na wczesne zmiany związane z Alzheimerem. Stężenia GFAP miały tendencję do stopniowego wzrostu w miarę zbliżania się do oczekiwanego wieku wystąpienia objawów zarówno u nosicieli mutacji, jak i u niemających mutacji, ale związki między GFAP, metabolizmem mózgu i funkcjami poznawczymi były specyficzne dla genów. U nosicieli APP wyższe stężenia GFAP wiązały się ze spadającym zużyciem glukozy w głębokich obszarach mózgu i ze słabszymi wynikami w większości testów poznawczych, co sugeruje, że aktywacja astrocytów jest ściśle związana z wczesnym uszkodzeniem i utratą funkcji. U nosicieli PSEN1 te powiązania były słabsze lub ich brakowało, co ponownie wskazuje na różne drogi biologiczne prowadzące do tego samego klinicznego efektu — demencji.
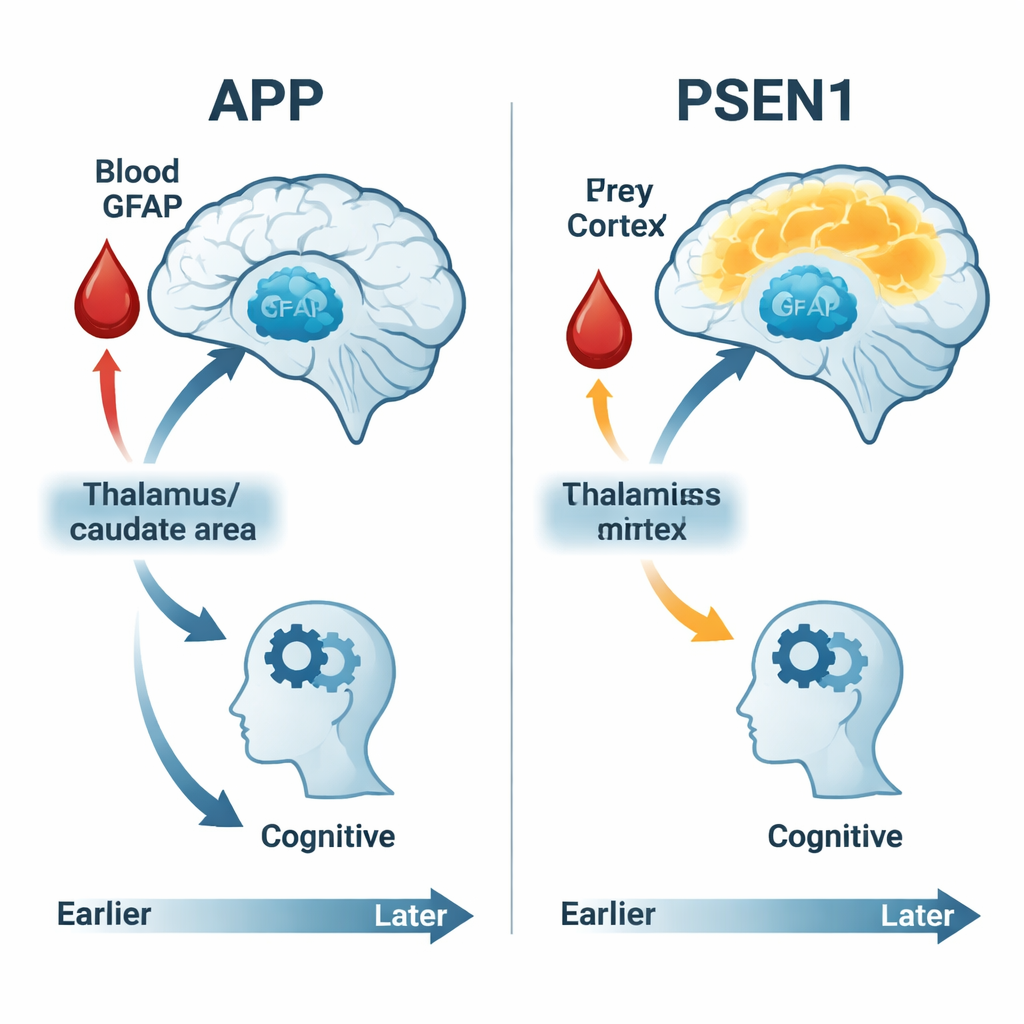
Co to oznacza dla wczesnego wykrywania i leczenia
Dla czytelnika niebędącego specjalistą główny przekaz jest taki, że w tych rodzinach o wysokim ryzyku zmiany związane z Alzheimerem zaczynają się dekady przed oczywistą utratą pamięci — i nie wyglądają tak samo u każdego. Skanowanie zużycia glukozy w mózgu, precyzyjne testy poznawcze oraz pojedynczy marker we krwi, taki jak GFAP, mogą łącznie wskazać, kiedy mózg zaczyna mieć problemy i jak szybko postępuje ten proces. Co ważne, osoby z różnymi formami genetycznymi Alzheimera wykazują różne sekwencje zmian: niektórzy mają wczesną fazę nadaktywności, inni stopniowy spadek, a marker we krwi związany ze stresem astrocytów silniej koreluje z uszkodzeniem w niektórych grupach niż w innych. Rozpoznanie tych odrębnych ścieżek może pomóc w dopasowaniu przyszłych leków i badań klinicznych do właściwych osób we właściwym momencie oraz potwierdza obiecującą rolę testów krwi, takich jak GFAP, w wychwytywaniu choroby Alzheimera wcześniej — zanim objawy pozbawią ludzi niezależności.
Cytowanie: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Słowa kluczowe: autosomalnie dominująca choroba Alzheimera, biomarker GFAP we krwi, metabolizm glukozy w mózgu, astrocyty i neurodegeneracja, wczesne wykrywanie Alzheimera