Clear Sky Science · pl
Receptor histaminowy H3 jako cel terapii zaburzeń używania alkoholu: kwestionowanie przewidywalności modeli zwierzęcych dla tłumaczenia klinicznego w rozwoju leków
Dlaczego te badania mają znaczenie w codziennym życiu
Zaburzenie używania alkoholu dotyka miliony ludzi na całym świecie, a dostępne obecnie leki pomagają tylko części z nich. Ten artykuł opisuje pełną drogę obiecującego kandydata na lek, BP1.3656B, od laboratorium po próby u ludzi. Pokazuje, jak pomysł, który znakomicie działa u zwierząt, może zawieść u ludzi — i dlaczego ta rozbieżność jest istotna dla każdego, kto liczy na lepsze metody leczenia problemowego picia.
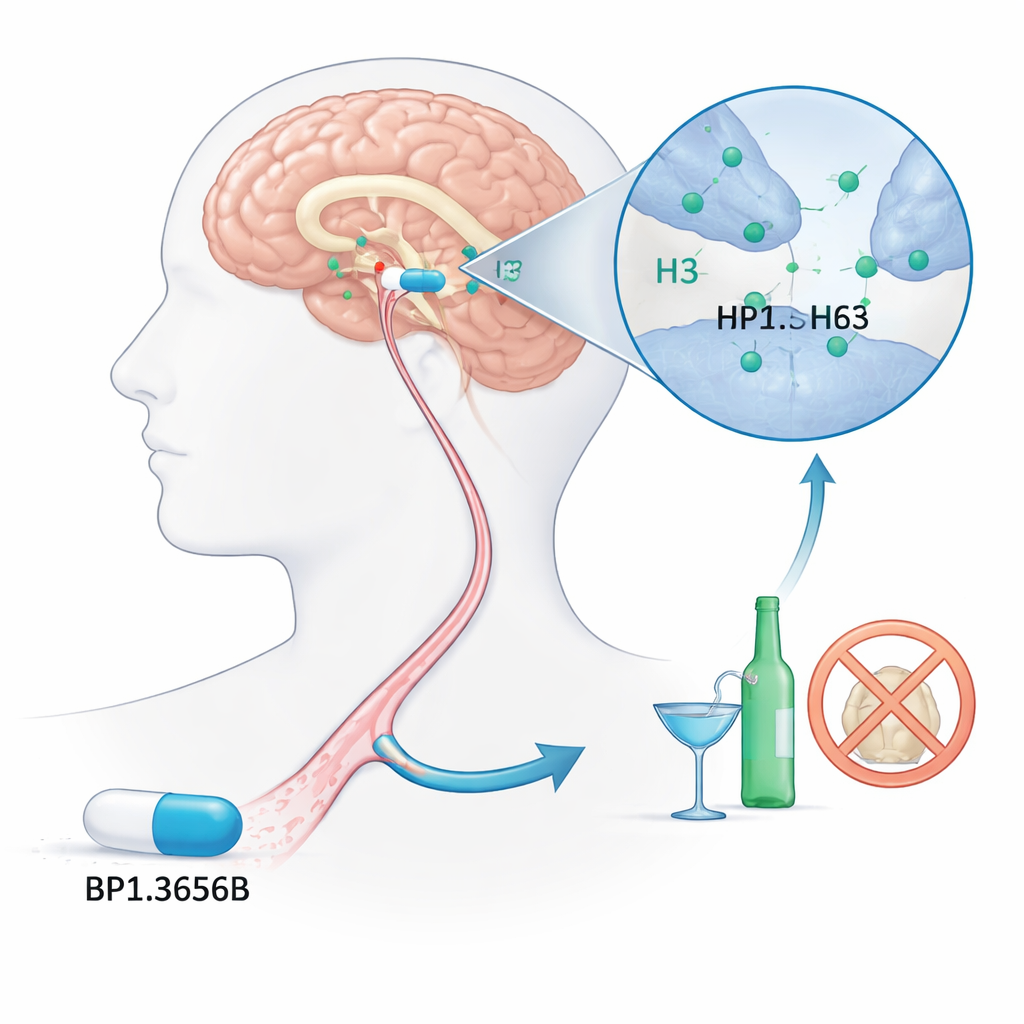
Nowy mózgowy cel w problemowym piciu
Naukowcy skupili się na mniej znanym przełączniku w mózgu zwanym receptorem histaminowym H3. Histamina jest najbardziej znana z roli w reakcjach alergicznych, ale w mózgu pomaga regulować czujność i komunikację między komórkami nerwowymi. Receptor H3 działa jak ściemniacz, zmniejszając uwalnianie histaminy i kilku innych neuroprzekaźników zaangażowanych w system nagrody i motywacji. Ponieważ alkohol silnie oddziałuje z tymi układami mózgowymi, od dawna podejrzewano, że blokowanie receptorów H3 może zmniejszyć chęć picia. BP1.3656B zaprojektowano jako silny bloker H3, z nadzieją, że złagodzi przyciąganie alkoholu do obwodów nagrody w mózgu.
Od chemii do sukcesów na zwierzętach
W wczesnych testach BP1.3656B wykazał profil, o jakim marzą twórcy leków. Wiązał się bardzo mocno i selektywnie z receptorem H3, dobrze przenikał do mózgu i wydawał się bezpieczny w standardowych badaniach laboratoryjnych. U myszy lek zmniejszał nagły wzrost aktywności zwykle następujący po dawce alkoholu i umiarkowanie ograniczał napadowe picie w teście „drinking in the dark”. U szczurów szkolonych do naciskania dźwigni w celu uzyskania alkoholu BP1.3656B znacząco zmniejszał ilość wypijanego alkoholu i wysiłek wkładany w jego zdobycie, zarówno u zwierząt będących ciężkimi pijakami, jak i u tych, które stały się fizycznie zależne. Lek osłabiał też picie nawracające i łagodził niepokój związany z odstawieniem alkoholu. Razem te wyniki sugerowały, że lek mógłby obniżać motywację do picia i pomagać zapobiegać powrotom do intensywnego spożycia.
Wczesne badania u ludzi: czy lek dociera do celu?
Nastąpiły badania fazy I na zdrowych ochotnikach. Pojedyncze i powtarzane dawki do 90 mikrogramów były generalnie dobrze tolerowane, z głównie łagodnymi zaburzeniami snu, co pasuje do działającego pobudzająco charakteru blokerów H3. Pomiary we krwi wykazały wyraźny, przewidywalny wzorzec wchłaniania i eliminacji leku. Aby upewnić się, że trafia on do zamierzonego celu w żyjącym ludzkim mózgu, zespół wykorzystał pozytonową tomografię emisyjną (PET), rodzaj skanu mózgu, który może pokazać, ile receptorów jest zajętych przez lek. Nawet stosunkowo niskie dawki BP1.3656B blokowały większość receptorów H3 w kilku obszarach mózgu istotnych dla motywacji i nagrody, potwierdzając, że przynajmniej na poziomie biologicznym lek robi to, do czego go zaprojektowano.
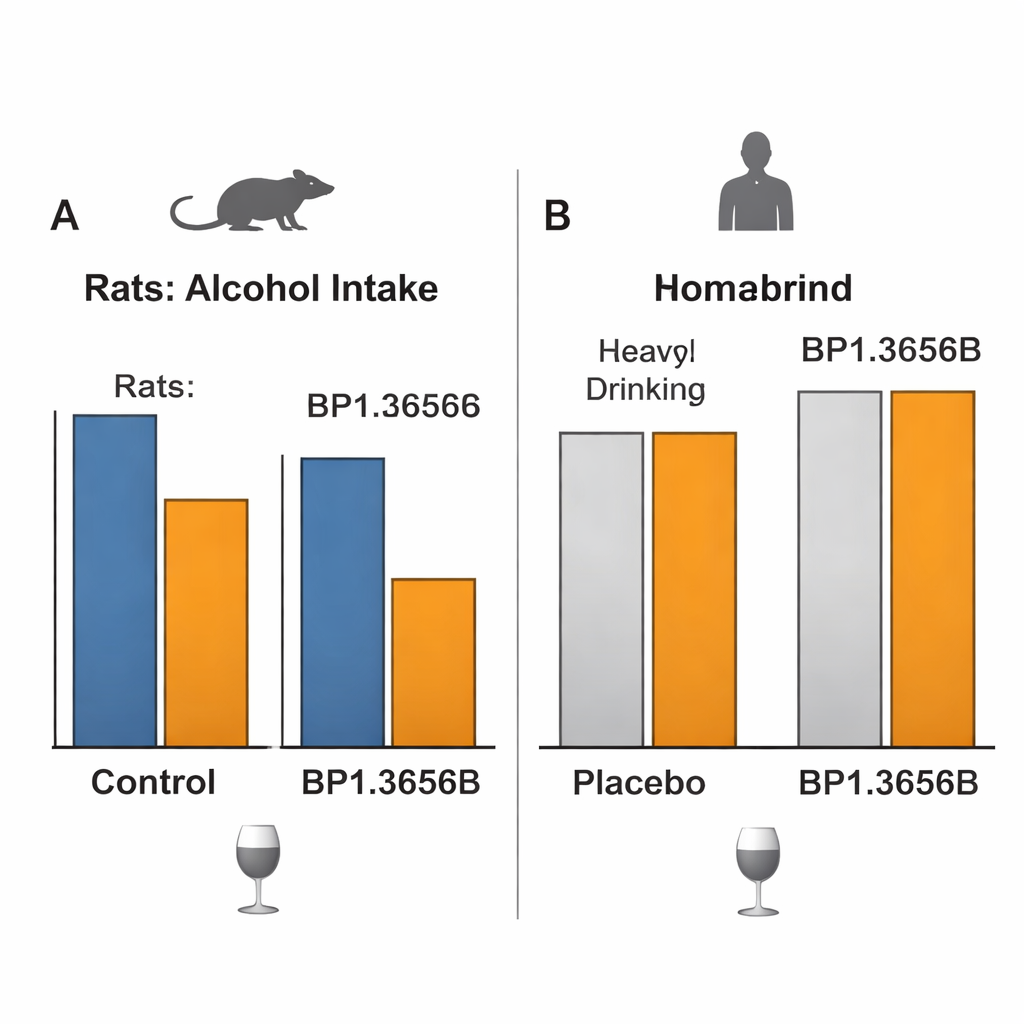
Kiedy obiecujące wyniki na zwierzętach nie przekładają się na ludzi
Kluczowe pytanie brzmiało, czy to wszystko przełoży się na istotne zmiany w piciu u osób z zaburzeniem używania alkoholu. W starannie kontrolowanym badaniu laboratoryjnym dorośli z problemami alkoholowymi, którzy nie szukali leczenia, otrzymywali BP1.3656B lub placebo, a potem uczestniczyli w sesjach, w których mogli samodzielnie podawać sobie alkohol dożylnie przez naciśnięcie przycisku, w warunkach zaprojektowanych do pomiaru zarówno przyjemności, jak i motywacji. Lek nie miał wykrywalnego wpływu na to, ile alkoholu decydowali się otrzymać. Następnie przeprowadzono większe, 12-tygodniowe, wielokrajowe badanie kliniczne wśród pacjentów poszukujących leczenia, testując trzy dawki BP1.3656B podawane codziennie w porównaniu z placebo. Wszystkie grupy, włącznie z placebo, znacząco zmniejszyły dni intensywnego picia i całkowite spożycie alkoholu w czasie, ale lek nie przewyższył placebo w żadnym istotnym wskaźniku dotyczącym picia czy głodu alkoholowego, pomimo dobrej tolerancji i wyraźnego zajęcia celu.
Co to oznacza dla przyszłych terapii
Dla czytelnika niezwiązanego z nauką wniosek jest trzeźwiący, ale ważny: lek, który wyglądał doskonale w komórkach, myszach i szczurach — i wyraźnie osiągał cel w ludzkim mózgu — wciąż nie pomógł ludziom pić mniej. To nie znaczy, że nauka była błędna, ale podkreśla, jak niepewne jest przewidywanie wyników u ludzi na podstawie samych modeli zwierzęcych. Autorzy argumentują, że mniejsze, wczesne badania laboratoryjne u ludzi, które bezpośrednio testują wpływ leku na używanie alkoholu, powinny być stosowane częściej, by „zmniejszać ryzyko” przed dużymi, kosztownymi próbami. Innymi słowy, ta praca pokazuje, że potrzebujemy nie tylko nowych pomysłów na leki, lecz także lepszych sposobów wyboru tych, które rzeczywiście mają szansę pomóc osobom z zaburzeniem używania alkoholu.
Cytowanie: Le Foll, B., Naassila, M., Jeanblanc, J. et al. Histamine H3 Receptor as a target for alcohol use disorder: challenging the predictability of animal models for clinical translation in drug development. Transl Psychiatry 16, 55 (2026). https://doi.org/10.1038/s41398-026-03807-y
Słowa kluczowe: zaburzenie używania alkoholu, receptor histaminowy H3, BP1.3656B, leczenie uzależnienia, badania translacyjne