Clear Sky Science · pl
Tłumienie produkcji energii mitochondrialnej przez fotosyntetyczny bakteryjny peptyd cupredoksyny hamuje wzrost nowotworów
Przekształcanie bakterii w sojuszników w walce z rakiem
Komórki nowotworowe są żarłoczne energetycznie. Polegają na drobnych „elektrowniach” wewnątrz komórek, zwanych mitochondriami, które wytwarzają energię niezbędną do wzrostu, rozprzestrzeniania się i oporności na leczenie. To badanie bada niespodziewanego sojusznika w walce z rakiem: krótki fragment białka pochodzący z bakterii fotosyntetycznych. Naukowcy wykazują, że zaprojektowany peptyd może przenikać do komórek nowotworowych, wyłączać ich dostawy energii u źródła i znacząco poprawiać skuteczność radioterapii — przy jednoczesnym względnym oszczędzaniu komórek prawidłowych.
Malutki peptyd z dużym zadaniem
Zespół rozpoczął pracę od wcześniejszego odkrycia, że bakteryjne białko azuryna może spowalniać wzrost guza działając na słynny supresor nowotworowy p53. Następnie przeszukano bakterie bytujące w i wokół ludzkich guzów, skupiając się na mikrobach fotosyntetycznych wykorzystujących światło do wytwarzania energii. Bakterie te niosą pokrewne białka zwane cupredoksynami. Porównując ich struktury i historię ewolucyjną, badacze zawęzili uwagę do jednej cupredoksyny — auracyaniny B — i wycięli krótki, 28-aminokwasowy fragment nazwany aurB. Ten fragment jest rozpuszczalny w wodzie, potrafi przenikać przez błony komórkowe i ma kształt sugerujący potencjalną interakcję z kluczowymi mechanizmami wytwarzania energii wewnątrz komórki.
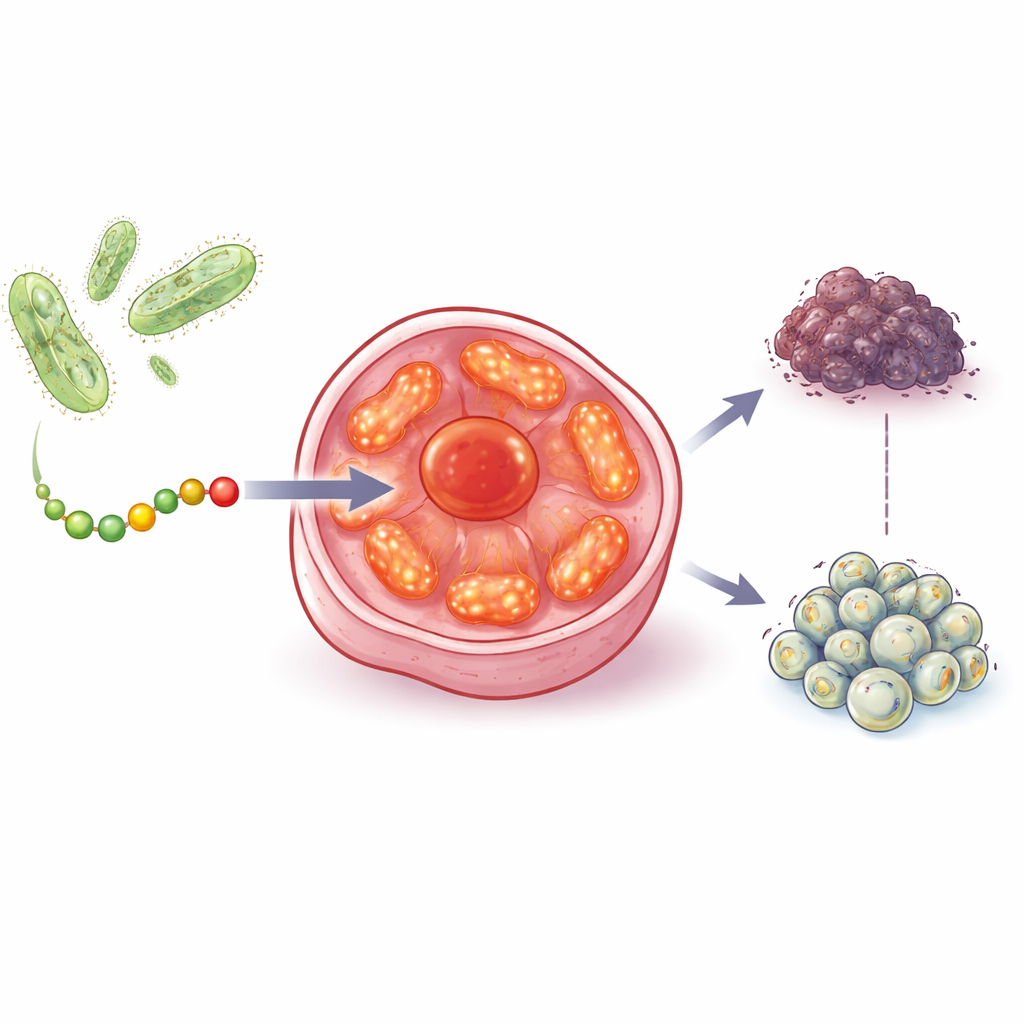
Odnalezienie i zaatakowanie „elektrowni” raka
W testach laboratoryjnych aurB zmniejszał przeżywalność linii komórkowych raka piersi, prostaty, jelita grubego i jajnika, nawet gdy te komórki nie miały funkcjonalnego p53 lub receptorów hormonalnych wymaganych przez wiele obecnych leków. Co istotne, aurB działał znacznie słabiej na prawidłowe komórki prostaty, serca i mięśni, mimo że te zdrowe komórki mają dużo mitochondriów. Badania obrazowe wykazały, że aurB preferencyjnie wnikał do komórek nowotworowych, a następnie kumulował się w ich mitochondriach. Mikroskopia elektronowa, z aurB przyłączonym do drobnych złotych prętów jako uchwytu wizualnego, potwierdziła, że peptyd rzeczywiście gromadzi się w tych organellach.
Odcięcie dopływu energii
Po przedostaniu się do mitochondriów, aurB wiązał się ze specyficznym składnikiem syntazy ATP — molekularnej turbiny produkującej ATP, podstawową walutę energetyczną komórki. Doświadczenia z wyciągiem białkowym i spektrometrią mas zidentyfikowały tego partnera jako ATP5C, część centralnego rdzenia enzymu. Pomiary spektroskopii powierzchniowej (surface plasmon resonance) wykazały, że aurB przyłącza się do ATP5C z umiarkowaną siłą i wolnym odłączeniem, co jest zgodne ze stabilną interakcją. Testy funkcjonalne ujawniły, do czego prowadzi to wiązanie: aurB ostro obniżał poziomy ATP w mitochondriach komórek raka prostaty, spowalniał tempo zużycia tlenu i blokował zarówno oddychanie, jak i zapasową ścieżkę glikolizy. W miarę upadku produkcji energii, komórki nowotworowe wykazywały cechy zaprogramowanej śmierci komórkowej napędzanej przez kaspazę-3, kluczowy enzym egzekucyjny.
Hamowanie guzów i wzmocnienie efektu radioterapii
Naukowcy przetestowali następnie aurB w modelach mysich agresywnego raka prostaty. U zwierząt z wszczepionymi pod skórą ludzkimi guzami prostaty regularne wstrzyknięcia aurB zmniejszały wzrost guza o około dwie trzecie, porównywalnie lub lepiej niż lek chemioterapeutyczny paklitaksel, ale bez widocznej utraty masy ciała czy objawów cierpienia. Próbki guzów od leczonych myszy zawierały mniej komórek dzielących się i znacznie więcej komórek umierających. W drugim modelu, odzwierciedlającym przerzuty do kości — częste i śmiertelne miejsce rozsiewu raka prostaty — aurB samodzielnie spowalniał rozrost guza w kości kończyny i zmniejszał liczbę przerzutów do płuc. Jednak w połączeniu z umiarkowaną dawką promieniowania efekt był dramatyczny: guzy w leczonej kończynie zostały niemal całkowicie zniszczone, a przerzuty płucne zmniejszyły się o ponad 90 procent w porównaniu do kontroli.
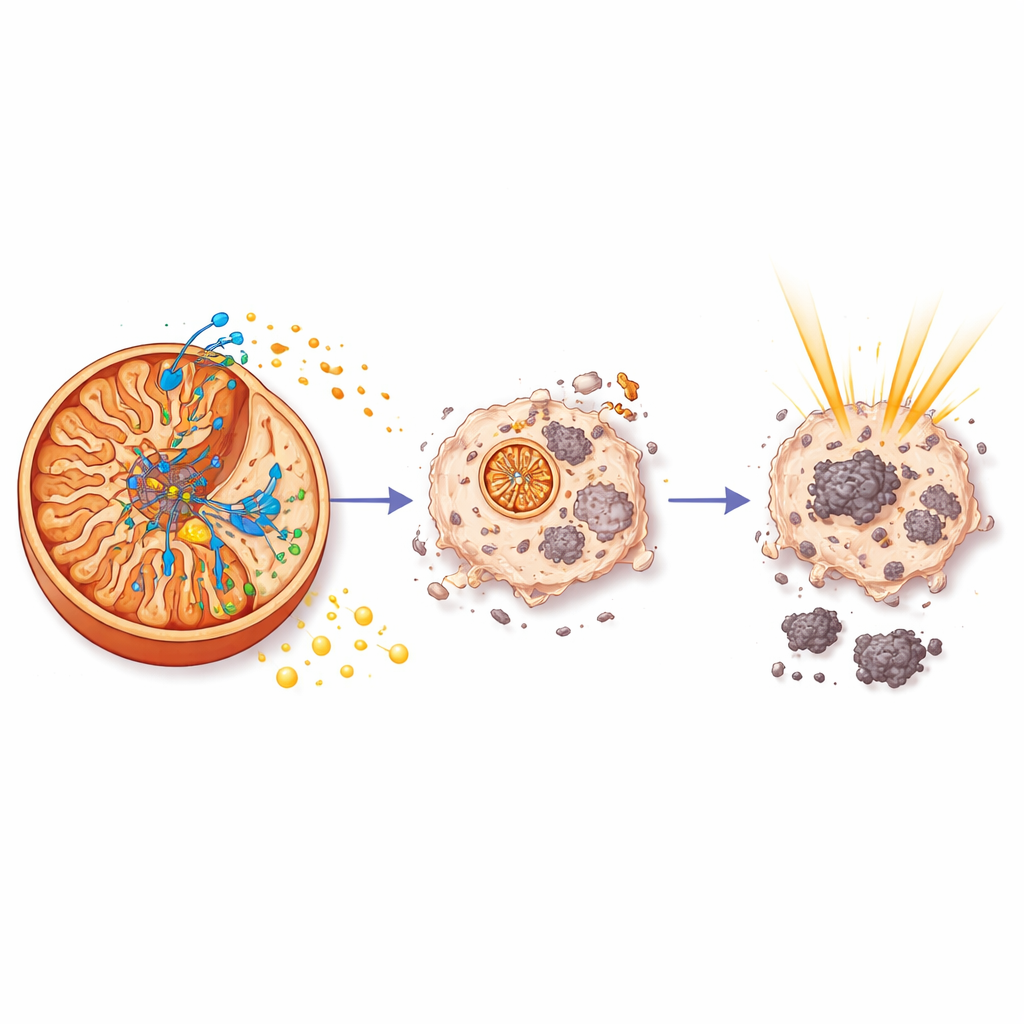
Dlaczego energia ma znaczenie dla radioterapii
Aby zrozumieć, dlaczego aurB zwiększa skuteczność radioterapii, zespół przeanalizował aktywność genów w guzach od leczonych myszy. Odkryto, że aurB, w przeciwieństwie do samego napromieniania, osłabiał sieć genów kontrolowanych przez HIF-1 — głównego regulatora pomagającego komórkom nowotworowym adaptować się do niskiego poziomu tlenu i napędzającego oporność na terapię. W warunkach ubogich w energię wywołanych przez aurB, kluczowe szlaki wzrostu i przeżycia zależne od PI3K i c-Myc zostały stłumione, a także zahamowano aparat glikolityczny, który pozwala guzom przetrwać w niekorzystnych warunkach. Innymi słowy, poprzez sabotowanie produkcji ATP bezpośrednio przy mitochondrialnej turbinie, aurB wpędził komórki nowotworowe w kryzys energetyczny, czyniąc je znacznie bardziej wrażliwymi na uszkodzenia wywołane promieniowaniem.
Nowa klasa precyzyjnych blokujących energię
Ta praca wprowadza nową strategię terapii przeciwnowotworowej: projektowanie małych, inspirowanych bakteriami peptydów, które celują w mitochondrialne systemy energetyczne zmienione w guzach. AurB, wywiedziony z bakteryjnego białka fotosyntetycznego, selektywnie atakuje składnik syntazy ATP, który często jest nadaktywny w nowotworach takich jak rak prostaty, piersi, jajnika i mózgu. Poprzez bezpośrednie pozbawianie komórek nowotworowych energii i osłabianie ich obrony — zwłaszcza wobec promieniowania — takie peptydy mogą uzupełniać istniejące terapie i oferować opcje tam, gdzie podejścia oparte na układzie odpornościowym zawodzą. Choć przed wprowadzeniem tej koncepcji do kliniki wciąż wiele pracy, badanie pokazuje, że pradawne bakteryjne białka energetyczne można przekształcić w nowoczesne, wysoko wyspecjalizowane narzędzia przeciwnowotworowe.
Cytowanie: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
Słowa kluczowe: syntaza ATP mitochondrialna, metabolizm nowotworów, peptydy terapeutyczne, rak gruczołu krokowego, sensytyzacja do napromieniania