Clear Sky Science · pl
Protoonkogen Spi-1 reguluje hipernadpis mRNA i złośliwy rozwój raka głowy i szyi
Dlaczego to badanie nad rakiem ma znaczenie
Raki głowy i szyi są powszechne i często śmiertelne, częściowo dlatego, że wiele guzów rośnie, daje przerzuty i nawraca nawet po intensywnym leczeniu. To badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach: co się dzieje, gdy komórki nowotworowe jednocześnie zwiększają aktywność wszystkich swoich genów, produkując niezwykle duże ilości mRNA — cząsteczek kierujących syntezą białek? Wskazując pojedynczy przełącznik kontrolny, który napędza ten nadaktywowany stan, autorzy odkrywają potencjalne słabe miejsce w niektórych z najbardziej niebezpiecznych guzów głowy i szyi.
Komórki żyjące na przyspieszonych obrotach
Każda komórka potrzebuje mRNA do budowy białek, ale komórki nowotworowe często zachowują się jak fabryki w stanie przeciążenia. Badacze skupili się na „hipernadpisie mRNA”, stanie, w którym komórki globalnie zwiększają produkcję komunikatów kodujących białka, a nie tylko kilku genów powiązanych z nowotworem. Wykorzystując sekwencjonowanie pojedynczych komórek na ponad 100 000 komórek od 12 pacjentów, policzyli cząsteczki mRNA komórka po komórce. Komórki nowotworowe o najwyższej całkowitej produkcji mRNA były mniej dojrzałe, bardziej plastyczne pod względem tożsamości i pełne aktywnych szlaków wspierających wzrost, odporność na stres i migrację. Rozszerzając analizę o dużą publiczną bazę danych nowotworów, badacze stwierdzili, że pacjenci, których guzy wykazywały ten stan wysokiej produkcji, mieli istotnie gorsze przeżycie, nawet po uwzględnieniu czynników takich jak stadium choroby czy zakażenie wirusem brodawczaka ludzkiego. 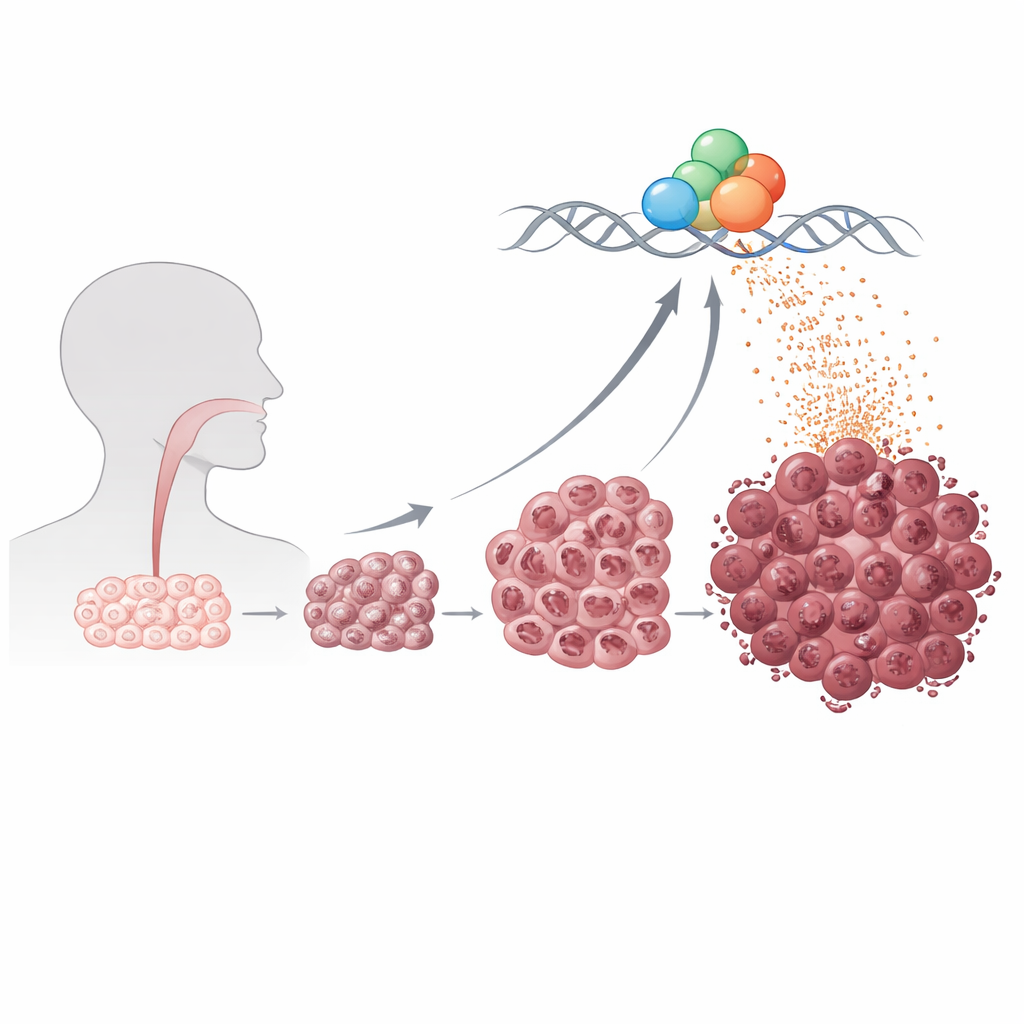
Mistrzowski przełącznik zwany SPI1
Aby zrozumieć, co napędza tę nadaktywność przekazu, zespół poszukał czynników transkrypcyjnych — białek wiążących DNA i kontrolujących, które geny są włączane — które były szczególnie aktywne w komórkach o wysokiej produkcji. Jeden wyróżniał się szczególnie: SPI1, znany też jako PU.1, wcześniej powiązany głównie z nowotworami krwi. W guzach głowy i szyi aktywność SPI1 rosła równolegle z całkowitym poziomem mRNA, zarówno w próbkach pacjentów, jak i w liniach komórkowych nowotworów. Guzy o wyższej aktywności SPI1 były bogatsze w szlaki sprzyjające nowotworzeniu i wiązały się z gorszymi wynikami u pacjentów. W obrębie pojedynczych guzów te same komórki, które wykazywały silne sygnały SPI1, były jednocześnie tymi o najsilniejszej produkcji mRNA, co sugeruje bezpośrednie powiązanie między tym czynnikiem a stanem nadaktywnej transkrypcji.
Regulowanie poziomu SPI1 w laboratorium
Autorzy następnie sprawdzili, czy SPI1 towarzyszy jedynie agresywnej chorobie, czy faktycznie ją powoduje. W hodowanych komórkach raka głowy i szyi, które naturalnie wytwarzają dużo SPI1, użyli narzędzi genetycznych do obniżenia poziomu tego białka. Komórki te spowolniły wzrost, tworzyły mniej kolonii, mniej migrowały i inwadowały oraz wykazywały więcej cech programu śmierci komórkowej. Gdy osłabione komórki wszczepiono myszom, powstałe guzy były mniejsze, rosły wolniej i zawierały mniej komórek dzielących się oraz więcej komórek umierających. Odwrotne eksperymenty potwierdziły tę samą zależność z drugiej strony: zwiększenie ekspresji SPI1 w komórkach o niskim poziomie przyspieszało wzrost i inwazję w hodowlach oraz prowadziło do większych, szybciej rosnących guzów u zwierząt.
Jak SPI1 wzmacnia produkcję genów
Aby zmierzyć wpływ SPI1 na aktywność genów, zespół śledził nowo powstające RNA przy użyciu znacznika chemicznego i bezpośrednio ilościowo oznaczał oczyszczone mRNA na komórkę. Obniżenie poziomu SPI1 zmniejszało zarówno syntezę nowego RNA, jak i całkowitą ilość mRNA, podczas gdy wymuszenie wyższej ekspresji SPI1 je zwiększało. Przy użyciu systemów pozwalających na szybkie włączanie SPI1 pokazano, że produkcja mRNA rośnie w ciągu kilku godzin, ujawniając zależny od czasu efekt. Badania wiązania w skali całego genomu wykazały dodatkowo, że SPI1 lokuje się w pobliżu miejsc startu transkrypcji tysięcy genów i działa jako szeroki aktywator, szczególnie ścieżek związanych z wykorzystaniem energii, ruchem komórek i reakcjami na stres. Razem te wyniki ukazują SPI1 jako mistrzowskiego regulatora, który przesuwa komórki nowotworowe w stan hipernadpisu, a nie jedynie modyfikuje kilka odizolowanych genów. 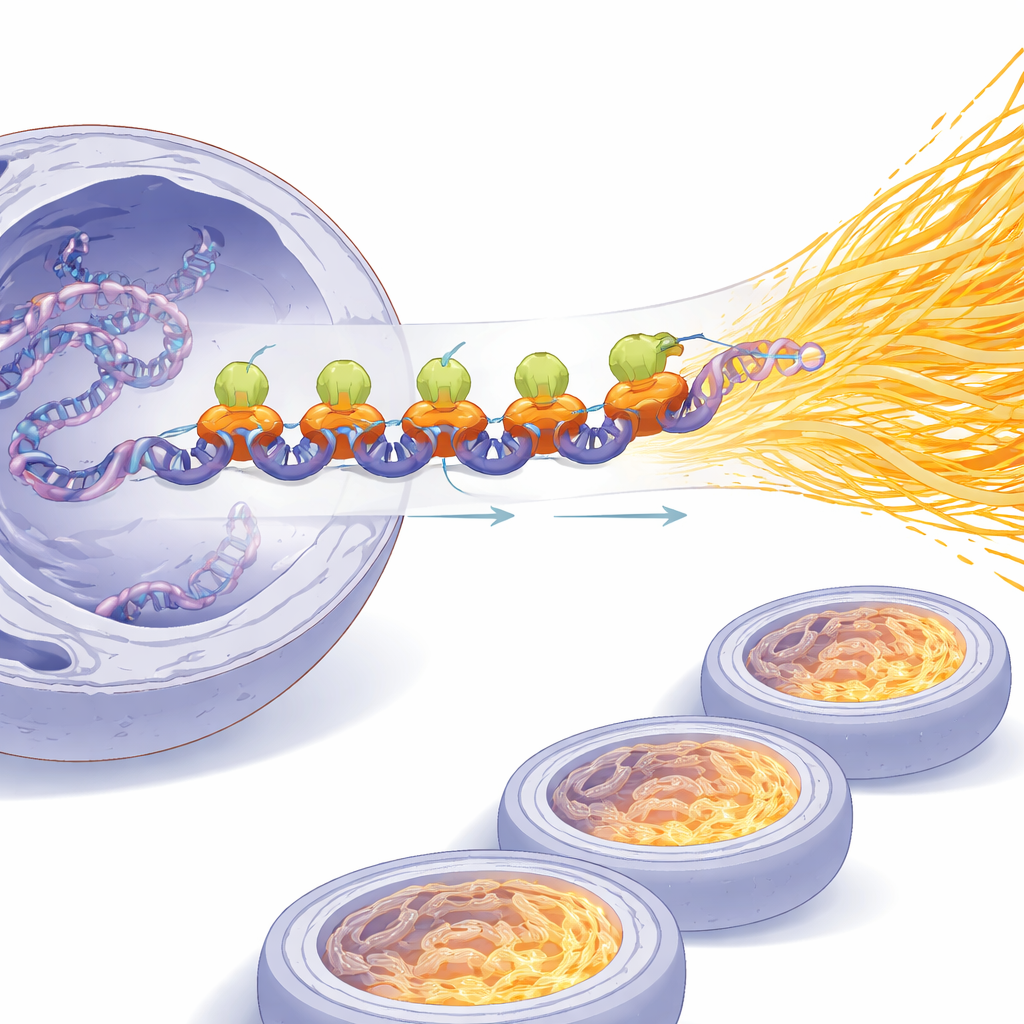
Co to oznacza dla pacjentów
Na koniec badacze przeanalizowali próbki guzów od dwóch niezależnych grup pacjentów leczonych w jednym szpitalu. Zarówno w raku krtani, jak i w raku podnagłośniowym, poziomy białka SPI1 były wyraźnie wyższe w tkance guza niż w sąsiedniej tkance normalnej. Pacjenci, których guzy zawierały więcej SPI1, mieli krótsze całkowite przeżycie, a to powiązanie utrzymywało się nawet po uwzględnieniu standardowych cech klinicznych, takich jak stadium choroby. Chociaż obecnie nie ma leków celujących bezpośrednio w SPI1, praca sugeruje, że zakłócenie jego aktywności — lub zależnego od niego aparatu transkrypcyjnego — mogłoby spowolnić lub okiełznać raki głowy i szyi o wysokim ryzyku. Mówiąc prosto, badanie ujawnia, że niektóre guzy stają się szczególnie niebezpieczne, włączając globalny „pedał gazu” dla aktywności genów, a SPI1 jest jedną z kluczowych stóp naciskających ten pedał.
Cytowanie: Liu, Z., Qin, Z., Li, H. et al. Spi-1 proto-oncogene regulates mRNA hypertranscription and malignant progression in head and neck cancer. Sig Transduct Target Ther 11, 102 (2026). https://doi.org/10.1038/s41392-026-02669-6
Słowa kluczowe: rak głowy i szyi, hipernadpis mRNA, czynnik transkrypcyjny SPI1, progresja guza, biomarkery nowotworowe