Clear Sky Science · pl
Skuteczność i immunomodulujący efekt opancerzonych komórek CAR-T specyficznych dla Claudin18.2 z IL-7/XCL1 w nowotworach przewodu pokarmowego: analiza przedkliniczna i kliniczna
Skierowanie układu odpornościowego przeciwko nowotworom przewodu pokarmowego
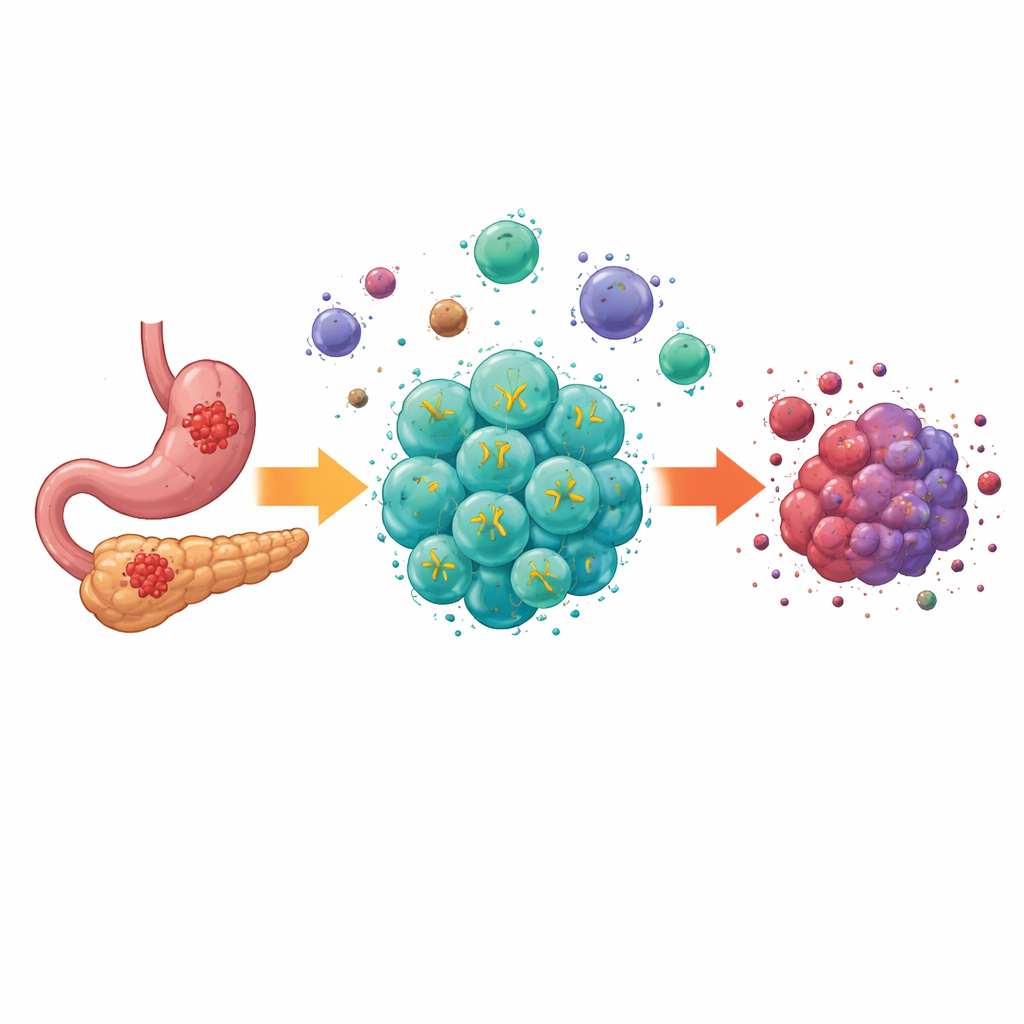
Raki żołądka i trzustki należą do najbardziej śmiertelnych nowotworów, częściowo dlatego, że często opierają się chirurgii, chemioterapii i radioterapii. W badaniu tym zbadano nowe podejście do zwalczania tych nowotworów poprzez wzmocnienie własnych komórek odpornościowych organizmu tak, aby mogły wnikać w guzy lity, przetrwać w nich i przywoływać posiłki. Przeprojektowując komórki T walczące z rakiem tak, by wydzielały pomocne sygnały immunologiczne, badacze dążą nie tylko do bezpośredniego ataku na guzy, ale też do pobudzenia reszty układu odpornościowego w wrogim dla niego mikrośrodowisku guza.
Dlaczego guzy lite są trudne do leczenia
Nowoczesne terapie komórkowe zwane komórkami CAR-T przyniosły spektakularne wyniki w nowotworach krwi, wyleczając niektórych pacjentów nie mających innych opcji. Jednak guzy lite, takie jak te w przewodzie pokarmowym, stawiają dodatkowe przeszkody. Ich komórki są zróżnicowane w różnych miejscach, wnętrze guza jest pozbawione składników odżywczych i tlenu, a mieszanina komórek i cząsteczek o działaniu hamującym tłumi ataki odpornościowe. Wcześniejsze generacje komórek CAR-T potrafiły rozpoznawać cele na komórkach raka przewodu pokarmowego, lecz często nie potrafiły się rozszerzać, utrzymywać i funkcjonować w tym surowym środowisku, co ograniczało ich rzeczywisty wpływ.
Sprytniejszy projekt zmodyfikowanych komórek T
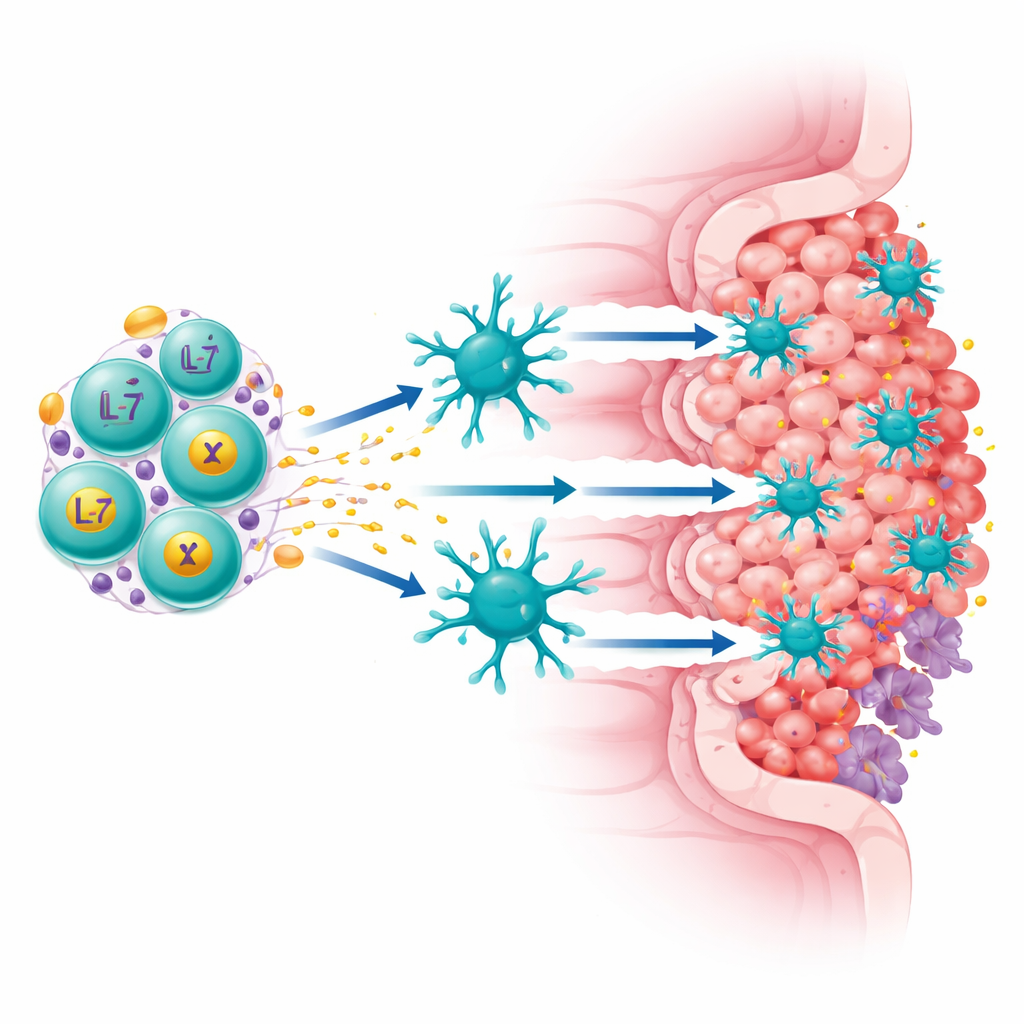
Zespół skupił się na białku o nazwie Claudin18.2, obecnym w dużych ilościach na wielu komórkach raka żołądka i trzustki, a w niewielkim stopniu w tkankach zdrowych. Zbudowali „czwartą generację” komórek CAR-T, które wykonują dwie funkcje jednocześnie: rozpoznają Claudin18.2 na komórkach nowotworowych i ciągle wydzielają dwa czynniki wzmacniające odporność, IL-7 i XCL1. IL-7 wspiera przetrwanie komórek T i utrzymanie długowiecznego, przypominającego komórki macierzyste stanu, podczas gdy XCL1 działa jak sygnał przyciągający rzadki, lecz potężny typ komórek odpornościowych zwanych cDC1, szczególnie skuteczny w aktywacji komórek zabójczych T. Te ulepszone komórki, nazwane ExCAR-T lub RD07, mają nie tylko zabijać to, co rozpoznają, lecz także przekształcać immunologiczny krajobraz guza.
Mocna kontrola guza w modelach przedklinicznych
W modelach mysich nowotworów przewodu pokarmowego komórki ExCAR-T przewyższały konwencjonalne komórki CAR-T pozbawione IL-7 i XCL1. W hodowlach laboratoryjnych zmodyfikowane komórki zabijały więcej komórek nowotworowych i zawierały więcej długowiecznych komórek T o fenotypie pamięci. U zwierząt z guzami pozytywnymi na Claudin18.2 leczenie ExCAR-T prowadziło do głębszego kurczenia się guzów i wydłużenia przeżycia w porównaniu ze standardowymi komórkami CAR-T. Ulepszone komórki lepiej się namnażały we krwi i wywoływały szerszą aktywność immunologiczną, w tym sygnały rekrutujące dodatkowe komórki odpornościowe przy jednoczesnym zmniejszeniu czynników powiązanych z rozprzestrzenianiem się guza. Co istotne, myszy, które zostały wyleczone za pomocą ExCAR-T, odrzucały ponowne podanie komórek nowotworowych pozbawionych celu Claudin18.2, co wskazuje, że terapia wywołała trwałą, ogólnoguza pamięć immunologiczną, a nie wąsko ukierunkowaną odpowiedź na jeden cel.
Wczesne wyniki badania klinicznego u pacjentów
Zachęceni tymi danymi badacze rozpoczęli pierwsze w populacji pacjentów badanie RD07 u 12 osób z zaawansowanym rakiem żołądka, połączenia przełyku z żołądkiem lub trzustki, które zawiodły po standardowych terapiach. Działania niepożądane były na ogół możliwe do opanowania: większość poważnych problemów wynikała ze spadków parametrów krwi po chemioterapii podanej przed infuzją, występowały tylko łagodne reakcje związane z uwalnianiem cytokin; nie odnotowano poważnych toksyczności mózgowych. Spośród 10 pacjentów możliwych do oceny u 7 stwierdzono widoczne zmniejszenie guza, a 2 osiągnęli częściową odpowiedź. Pacjenci, których guzy wykazywały umiarkowany lub wysoki poziom Claudin18.2, radzili sobie szczególnie dobrze — każdy z nich miał co najmniej stabilizację choroby, a niektórzy żyli wiele miesięcy dłużej niż przewidywano. U tych osób zmodyfikowane komórki T silniej się namnażały we krwi, a stężenia IL-7 i XCL1 we krwi wzrastały, zgodnie z założeniem terapii.
Zajrzeć do immunologicznego sąsiedztwa guza
Aby zrozumieć działanie RD07 u ludzi, zespół przebadał próbki guzów w rozdzielczości pojedynczych komórek przed i po leczeniu. Zaobserwowano spadek udziału komórek nowotworowych pozytywnych na Claudin18.2 u pacjentów odpowiadających na terapię, potwierdzając, że leczenie trafia w zamierzony cel. Jednocześnie nastąpił napływ zróżnicowanych klonów komórek T, w tym aktywnych komórek zabójczych i rezydentnych komórek pamięci tkankowej, co sugeruje, że organizm uruchomił szerszy atak immunologiczny. Specjalistyczne komórki dendrytyczne wykazywały oznaki zwiększonej aktywności i silniejszych interakcji z proliferującymi komórkami T, co jest spójne z przyciąganiem ich do guza przez XCL1. Badania obrazowe wycinka guza jednego pacjenta ujawniły po leczeniu mniej komórek nowotworowych i supresyjnych komórek mieloidalnych, przy większej liczbie komórek T i B oraz reorganizacji tkanki w strefy bogate w komórki odpornościowe — cechy „gorętszego”, bardziej zapalnego mikrośrodowiska.
Co to może znaczyć dla przyszłej opieki onkologicznej
Podsumowując, wyniki przedkliniczne i wczesne kliniczne sugerują, że RD07 robi coś więcej niż tylko dodaje kolejny ukierunkowany lek do arsenału onkologicznego. Łącząc rozpoznawanie guza z wbudowanym wsparciem immunologicznym, te zmodyfikowane komórki T potrafią przetrwać dłużej, rekrutować kluczowe komórki partnerskie i pomagać w „wyszkoleniu” własnego układu odpornościowego pacjenta do kontrolowania nowotworu, nawet gdy pierwotny cel zostanie utracony. Chociaż badanie było małe i przeprowadzone u pacjentów silnie wcześniej leczonych, konsekwentne zmniejszanie guzów, akceptowalna tolerancja i głęboka przebudowa immunologiczna są obiecujące. Jeśli potwierdzą to większe badania, podejście to może otworzyć nowy rozdział w leczeniu nowotworów przewodu pokarmowego, w którym wzmocnienie ekosystemu odpornościowego wewnątrz guza stanie się tak istotne, jak początkowy atak na komórki nowotworowe.
Cytowanie: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
Słowa kluczowe: terapia komórkami CAR-T, nowotwory przewodu pokarmowego, mikrośrodowisko guza, Claudin18.2, immunoterapia