Clear Sky Science · pl
Podobny do visininy białko 1 zaburza homeostazę wapniową i sprzyja migotaniu przedsionków w modelach ludzkich i gryzoni
Dlaczego ta historia o rytmie serca ma znaczenie
Migotanie przedsionków to powszechny problem rytmu serca, który zwiększa ryzyko udaru i niewydolności serca. Wiele osób z tym żyje, a lekarze wciąż mają trudności z jego zapobieganiem lub powstrzymaniem nawrotów po leczeniu. To badanie ujawnia dotąd pomijaną cząsteczkę w komórkach serca, nazwaną VILIP-1, która działa jak wadliwy przełącznik wapniowy i sprzyja migotaniu przedsionków u ludzi i zwierząt. Wskazanie tego przełącznika i wykazanie, że dostępne leki potrafią go stłumić, otwiera nową drogę do bezpieczniejszych, bardziej ukierunkowanych terapii.
Bliższe spojrzenie na chaotyczne bicie
W zdrowym sercu fale elektryczne rozchodzą się w uporządkowany sposób przez górne komory, czyli przedsionki, sterując każdym biciem. Ten porządek zależy w dużej mierze od wapnia — jonizowanego minerału, który napływa i odpływa z komórek serca, koordynując skurcz i rozkurcz. W migotaniu przedsionków ruch wapnia staje się niesforny: dodatkowe przecieki i wahania jego poziomu wywołują niepożądane sygnały elektryczne, które mogą przekształcić się w szybkie, nieregularne rytmy. Lekarze wiedzieli od lat, że zaburzenia gospodarki wapniowej są centralne dla tej choroby, lecz jej wczesne wyzwalacze pozostawały niejasne.
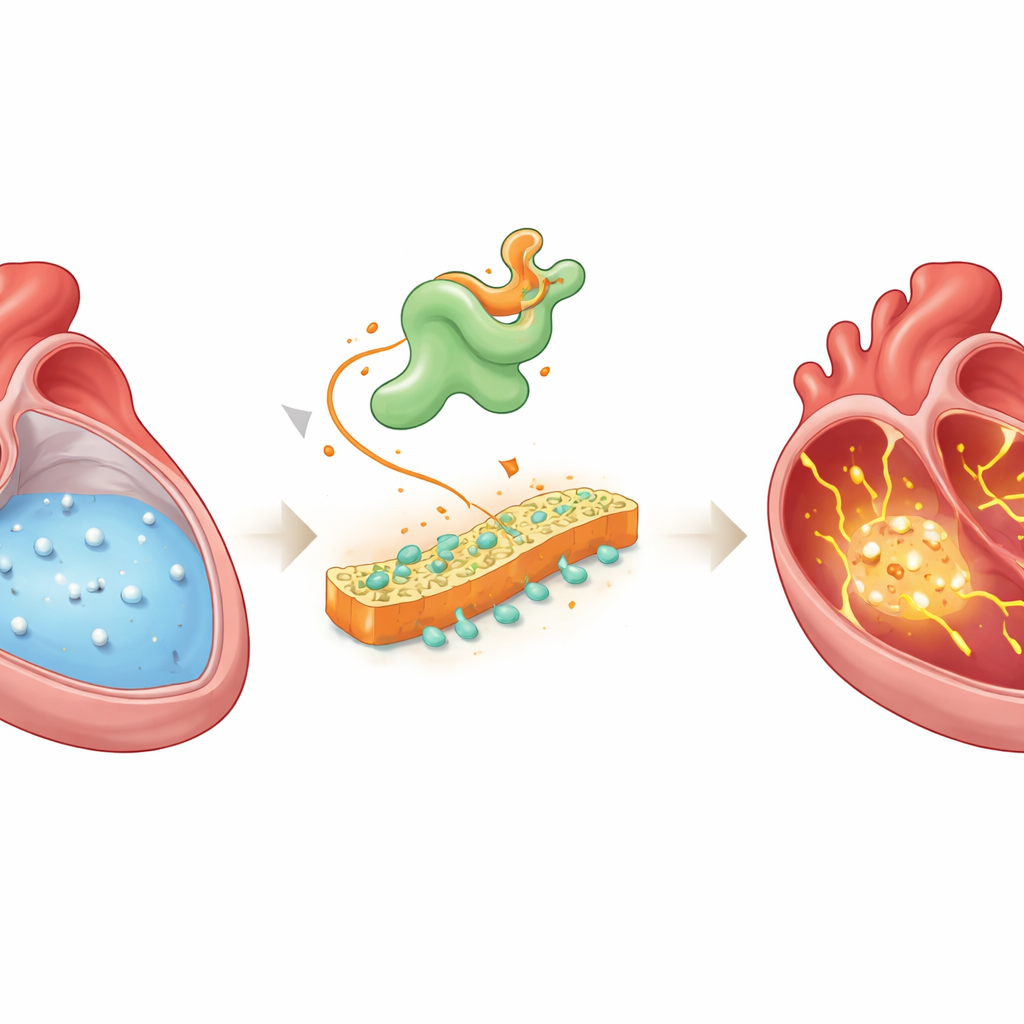
Odnalezienie ukrytego sprawcy
Naukowcy połączyli kilka zaawansowanych metod, by wyszukać cząsteczki łączące zaburzoną gospodarkę wapniową z migotaniem przedsionków. Rejestrowali sygnały wapniowe setek pojedynczych komórek przedsionkowych u szczurów z indukowanym pacingiem migotaniem przedsionków, a następnie sekwencjonowali pełny zestaw genów aktywnych w tych samych komórkach. Porównali też aktywność genów w tkance przedsionkowej pacjentów z migotaniem przedsionków i pacjentów z prawidłowym rytmem. Gdy nałożyli te zbiory danych i prześledzili, jak komórki zmieniają się na drodze od stanu zdrowia do choroby, jeden gen wyróżniał się wielokrotnie: Vsnl1, kodujący białko VILIP-1 — czujnik wapnia wcześniej badaný głównie w mózgu i trzustce, a nie w sercu.
Jak VILIP-1 zaburza równowagę wapniową
W tkance przedsionkowej zarówno u pacjentów, jak i w modelach zwierzęcych poziomy VILIP-1 były istotnie podwyższone, a białko skupiało się przy powierzchni komórki. Aby sprawdzić, czy ta zmiana jest tylko towarzysząca czy rzeczywiście napędza arytmię, zespół zmusił komórki przedsionkowe myszy do produkcji nadmiaru VILIP-1. U tych myszy nie obserwowano oczywistych uszkodzeń strukturalnych serca, ale ich przedsionki stały się znacznie bardziej podatne na wywoływane pacingiem migotanie przedsionków. Szczegółowe zapisy elektryczne wykazały więcej opóźnionych depolaryzacji następczych — nieprawidłowych wychyleń po każdym uderzeniu — oraz naprzemienność kształtu potencjału czynności z uderzenia na uderzenie, klasyczne sygnały niestabilnego zachowania elektrycznego związanego z przeciążeniem wapniowym. Wysokorozdzielcze obrazowanie wapniowe potwierdziło częste spontaniczne fale wapniowe i opróżnione wewnętrzne magazyny wapnia, co wskazuje na poważne przecieki wewnątrz komórek.
Kluczowy partner na powierzchni komórki
Aby zrozumieć, jak VILIP-1 powoduje te zaburzenia, naukowcy zmapowali, z jakimi białkami wchodzą z nim w interakcje w komórkach serca. Używając dwóch uzupełniających się metod — wyławiania partnerów wiążących z tkanki przedsionkowej oraz znakowania pobliskich białek „biotynową aureolą” w żywych komórkach — zawęzili zakres do NCX-1, głównego wymieniacza sodowo-wapniowego w błonie powierzchniowej serca. Ten wymieniacz normalnie pomaga usuwać wapń w zamian za sód, ale w pewnych warunkach może działać odwrotnie i wtłaczać wapń do wnętrza komórki. Badanie wykazało, że VILIP-1 fizycznie wiąże się z NCX-1 i zwiększa liczbę cząsteczek NCX-1 wbudowanych w błonę, nie podnosząc ogólnej produkcji NCX-1. W rezultacie prądy wymiennika stały się większe, a blokada NCX-1 selektywnym inhibitorem zmniejszała fale wapniowe i utrudniała wywoływanie migotania przedsionków u myszy z nadmiarem VILIP-1.
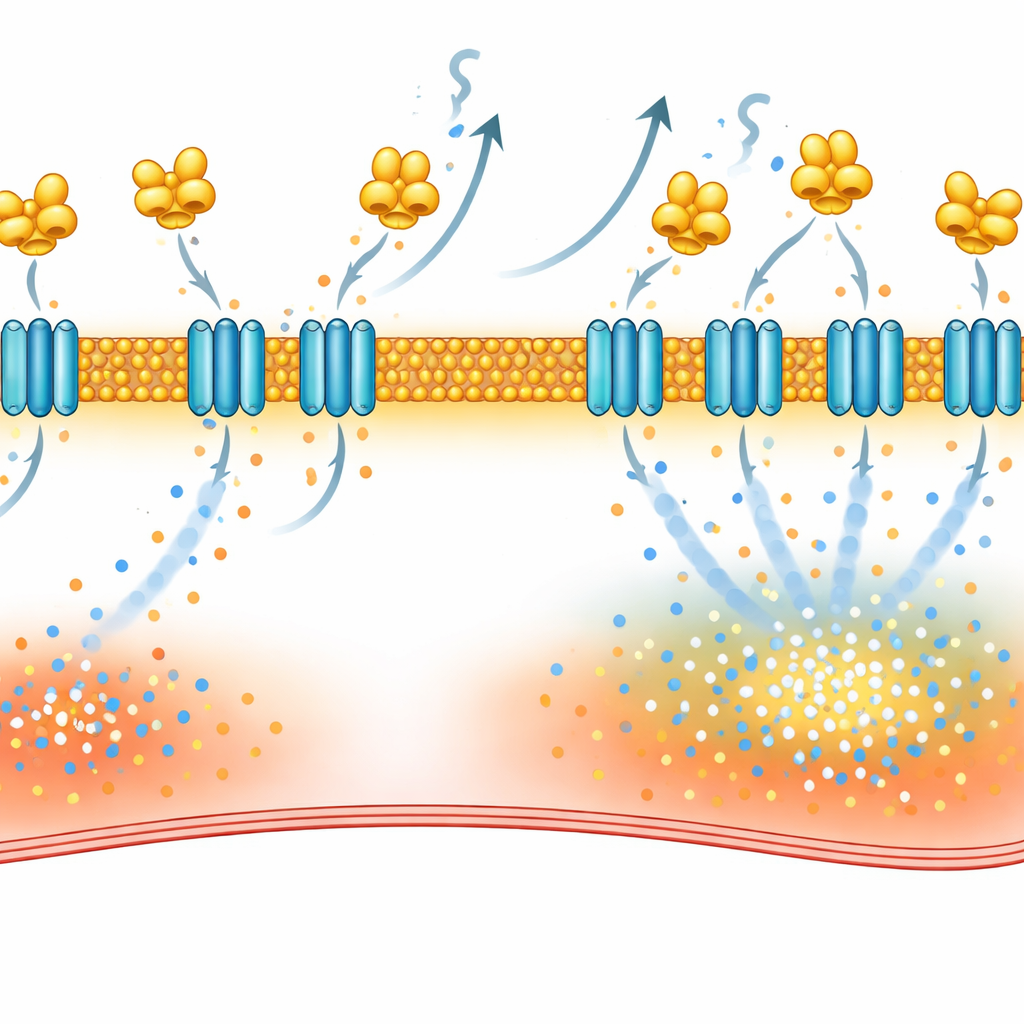
Wyłączanie wadliwego przełącznika dostępnymi lekami
VILIP-1 zakotwicza się w błonach za pomocą tłuszczowego łańcucha zwanego myrystoylem, który staje się odsłonięty, gdy wapń wiąże białko. Zespół zastosował desloratadynę, wcześniej wykazaną jako zakłócającą ten etap przyłączania, i stwierdził, że obniża ona poziom NCX-1 na powierzchni komórki, normalizuje prądy wymiennika, zmniejsza fale wapniowe i ogranicza epizody migotania przedsionków w modelach szczurzych. Testowali też repaglinidę, lek przeciwcukrzycowy znany z wiązania pokrewnych czujników wapnia. Testy biofizyczne potwierdziły, że repaglinida bezpośrednio przyłącza się do VILIP-1. U szczurów z pacingiem i w tkance przedsionkowej pacjentów z migotaniem przedsionków leczenie repaglinidą zmniejszyło NCX-1 w błonie, uspokoiło przecieki wapniowe w pojedynczych komórkach i znacząco obniżyło podatność na indukcję migotania przedsionków.
Co to oznacza dla osób z nieregularnym rytmem serca
W sumie badanie opisuje samonapędzającą pętlę: rosnące poziomy wapnia rekrutują VILIP-1 do powierzchni komórki, gdzie zwiększa on NCX-1, co z kolei napędza dalsze przeciążenie wapniowe i tworzy warunki sprzyjające migotaniu przedsionków. Przerywając tę pętlę na poziomie VILIP-1 — albo blokując jego tłuszczowy kotwicę, albo wiążąc centrum czujnika wapnia — istniejące leki mogą przywrócić stabilniejszą równowagę wapniową i zmniejszyć podatność na arytmię w ludzkiej i gryzoniowej tkance serca. Choć potrzebne są dalsze prace nad poprawą swoistości leków i przetestowaniem tych strategii w większych modelach zwierzęcych oraz w badaniach klinicznych, VILIP-1 wyłania się teraz jako obiecujący nowy cel prewencji i leczenia tej rozpowszechnionej i często opornej arytmii serca.
Cytowanie: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
Słowa kluczowe: migotanie przedsionków, sygnalizacja wapniowa, arytmia serca, wymieniacz sodowo-wapniowy, cele terapeutyczne