Clear Sky Science · pl
Sygnalizacja fibrynogenu–Bmal1 jako cel terapeutyczny ograniczający rozwarstwienie aorty przez zachowanie kurczliwości VSMC
Dlaczego ukryty strażnik aorty ma znaczenie
Rozwarstwienie aorty to jedno z najbardziej przerażających nagłych stanów w medycynie: główna tętnica wypływająca z serca może nagle się rozerwać, często bez ostrzeżenia, a wielu pacjentów umiera w ciągu kilku godzin. Operacja może uratować życie, ale niesie ryzyko i nie zawsze jest możliwa od razu. W tym badaniu autorzy analizują niespodziewanego sprzymierzeńca krążącego już we krwi — fibrynogen, białko krzepnięcia — i pokazują, że poza rolą w zatrzymywaniu krwawienia może ono także pomagać złączyć aortę i spowalniać postęp choroby, potencjalnie zyskując lekarzom cenny czas na działanie.
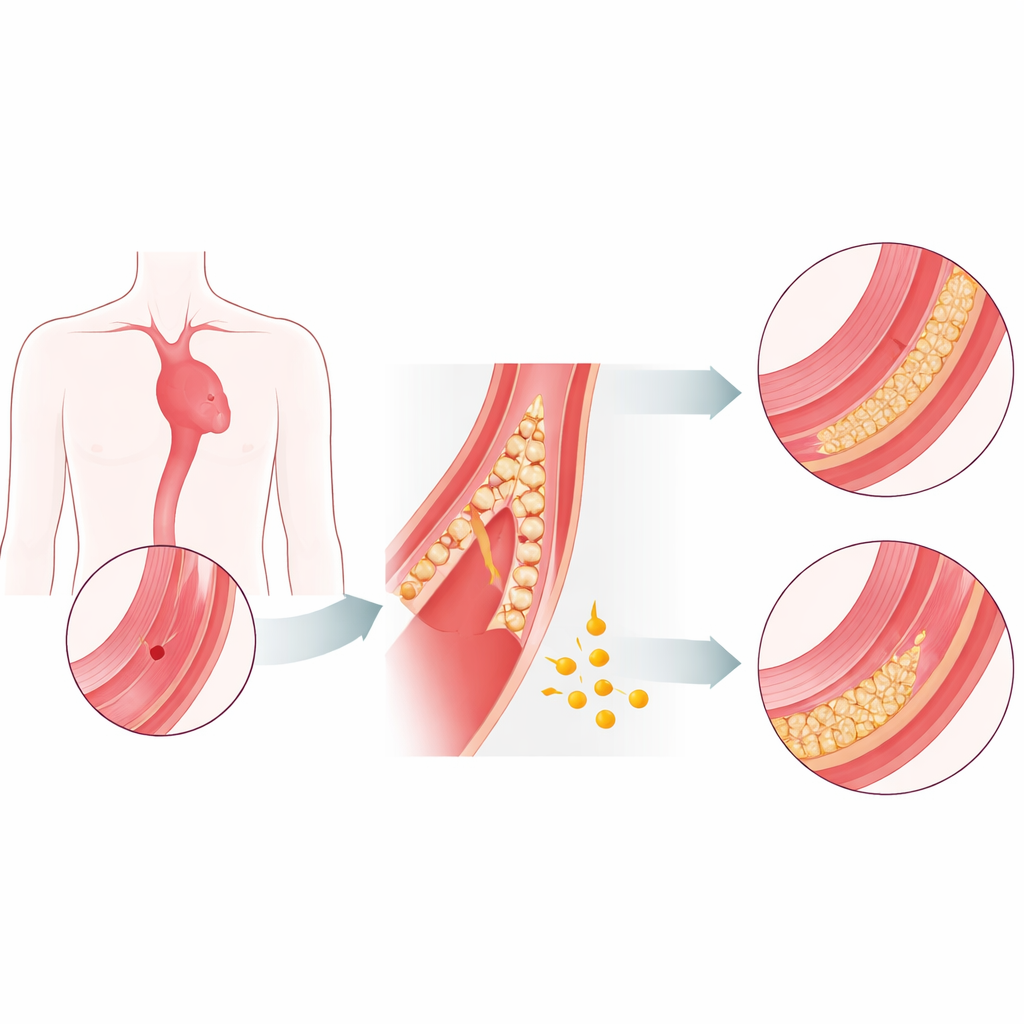
Cichy zabójca potrzebujący nowych możliwości
Aorta zbudowana jest jak wytrzymały, wielowarstwowy wąż. Gdy jej wewnętrzne warstwy słabną i rozdzierają się, krew może wcisnąć się w ścianę i rozwarstwić ją — to rozwarstwienie aorty. W niebezpiecznej wczesnej fazie ryzyko śmierci rośnie z godziny na godzinę i często jedyną opcją jest pilna operacja. Pacjenci, którzy przeżyją na tyle długo, by osiągnąć stabilniejszą, przewlekłą fazę, radzą sobie znacznie lepiej. Obecnie brak sprawdzonych leków, które niezawodnie spowalniałyby proces rozdzierania lub wzmacniały ścianę aorty. Autorzy postawili hipotezę, czy fibrynogen — powszechne białko krwi znane przede wszystkim z roli w krzepnięciu — może także działać jako naturalny stabilizator aorty.
Wskazówki od pacjentów: więcej fibrynogenu, lepsze przeżycie
Zespół najpierw przebadał 310 pacjentów z ostrym rozwarstwieniem aorty, którzy nie mogli przejść operacji i byli leczeni wyłącznie farmakologicznie. Porównano tych, którzy przeżyli pobyt w szpitalu, z tymi, którzy zmarli. Pacjenci, którzy zmarli, zwykle mieli znacznie niższe stężenia fibrynogenu we krwi. Kiedy badacze pogrupowali pacjentów według poziomu fibrynogenu, stwierdzili, że bardzo niskie wartości (poniżej 2 g/l) wiązały się ze znacznie wyższą śmiertelnością, podczas gdy wysokie poziomy (powyżej 4 g/l) korelowały z lepszym przeżyciem. Ten wzorzec sugerował, że fibrynogen nie jest tylko biernym towarzyszem, lecz może aktywnie pomagać aorcie opierać się dalszemu rozdarciu.
Obserwowanie pękania i gojenia aorty u myszy
Aby wyjść poza korelacje i zbadać zależność przyczynowo-skutkową, naukowcy użyli modeli myszowych, w których można wywołać osłabienie i rozwarstwienie aorty. U tych zwierząt fibrynogen normalnie nie występował w zdrowej ścianie aorty, lecz w miarę rozwoju choroby zaczynał przenikać do warstwy środkowej, gdzie znajdują się komórki mięśni gładkich. Co istotne, największe nagromadzenie fibrynogenu obserwowano w silnie uszkodzonych, lecz jeszcze nie pękniętych odcinkach, co sugerowało, że jego obecność może pomagać zapobiegać ostatecznemu pęknięciu. Gdy naukowcy zastosowali terapię genową zmniejszającą produkcję fibrynogenu w wątrobie, rozwarstwienia się pogorszyły: aorty ulegały większemu poszerzeniu, uszkodzenia strukturalne się nasilały, a więcej myszy umierało. Podanie oczyszczonego fibrynogenu odwracało te efekty. Niezależne eksperymenty w innym modelu tętniaka aorty wykazały podobny trend ochronny, co wzmacnia argument, że fibrynogen aktywnie chroni ścianę naczynia.
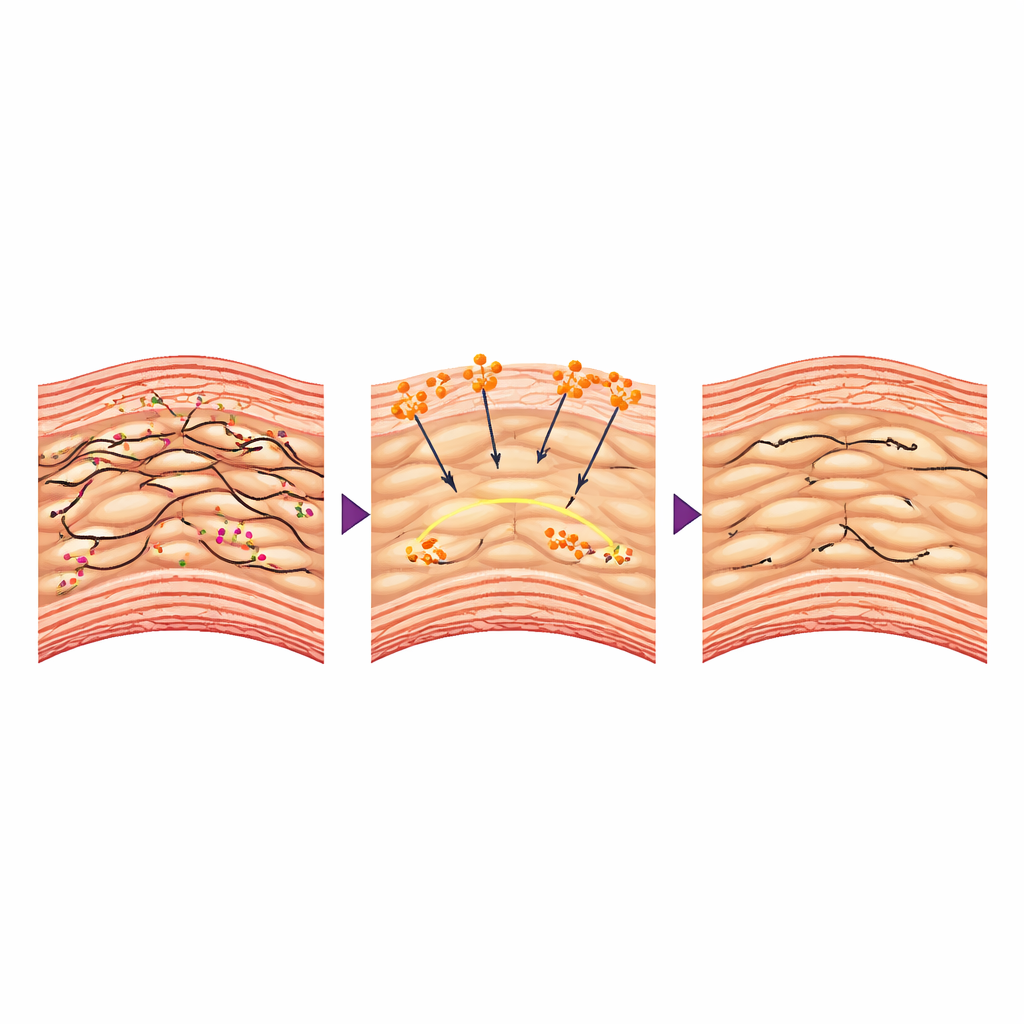
Ukryty dialog między białkiem krwi a komórkami mięśnia
Jak białko krzepnięcia mogłoby chronić aortę od wewnątrz? Autorzy skupili się na naczyniowych komórkach mięśni gładkich — komórkach kurczliwych tworzących warstwę środkową aorty i pełniących rolę jej żywych „pierścieni wzmacniających”. W przebiegu choroby te komórki często tracą zwartą, kurczliwą tożsamość i przechodzą w luźniejszy, bardziej syntetyczny stan, który degradując otaczające tkanki sprzyja uszkodzeniom. Badanie wykazało, że gdy fibrynogen wnikał do ściany aorty, wchodził w interakcję ze specyficznymi receptorami na tych komórkach i pomagał zachować ich wewnętrzny rusztowanie z filamentów aktynowych. Komórki mięśniowe z leczonych zwierząt były sztywniejsze, kurczyły się silniej w testach i wykazywały wyższe poziomy markerów „kurczliwych” oraz niższe poziomy białek rozkładających macierz podporową. Na poziomie genów fibrynogen tłumił aktywność Bmal1, głównego regulatora związanego z zegarem biologicznym, który w tym kontekście napędzał szkodliwe zmiany zachowania komórek mięśniowych. Wymuszenie ponownej aktywacji Bmal1 znosiło korzyści płynące z fibrynogenu, co dowodzi, że ta droga sygnałowa była kluczowa dla efektu ochronnego.
Od mechanizmu do potencjalnego leczenia
Ponieważ fibrynogen także pobudza krzepnięcie, zespół sprawdził, czy jego korzyść wynika wyłącznie z tworzenia mocniejszych skrzepów. Przy użyciu silnego leku rozrzedzającego krew blokującego trombinę — enzym przekształcający fibrynogen w stały skrzep — wykazano, że fibrynogen nadal chronił aortę, nawet gdy tworzenie skrzepów było w dużej mierze wyłączone. Na koniec przetestowano różne dawki i stwierdzono, że tylko wystarczająco wysokie ilości podanego fibrynogenu spowalniały rozwój choroby, zmniejszały pęknięcia i zachowywały strukturę tkanki. Razem te wyniki ukazują fibrynogen jako cząsteczkę o podwójnej funkcji: przy wyższych stężeniach niezmieniony fibrynogen może przenikać do osłabionej ściany aorty, tłumić szkodliwą ścieżkę sygnałową w komórkach mięśni gładkich i pomagać im pozostać silnymi i kurczliwymi. Dla pacjentów rodzi to perspektywę, że starannie dawkowane wlewy fibrynogenu mogłyby w przyszłości stać się leczeniem podobnym do leku, spowalniającym rozwarstwienie aorty i bezpiecznie wydłużającym czas na ratującą życie, planową operację.
Cytowanie: Zhong, X., Li, D., Zhao, Y. et al. Fibrinogen–Bmal1 signaling as a therapeutic target to limit aortic dissection by preserving VSMC contractility. Sig Transduct Target Ther 11, 103 (2026). https://doi.org/10.1038/s41392-026-02610-x
Słowa kluczowe: rozwarstwienie aorty, fibrynogen, mięśniowe komórki gładkie naczyń, sygnalizacja Bmal1, aorta tętniak