Clear Sky Science · pl
M6A-zmienione circArhgap26 łagodzi uszkodzenie serca po niedokrwieniu‒reperfuzji przez hamowanie palmitylowania plakofiliny-1
Dlaczego ochrona serca po zawale ma znaczenie
Kiedy ktoś ma zawał serca, lekarze spieszą się, by udrożnić zablokowaną tętnicę i przywrócić przepływ krwi. Ten ratunkowy zabieg ratuje życie, ale ma też mroczną stronę: nagły powrót krwi może dodatkowo uszkodzić serce — to zjawisko znane jako uszkodzenie niedokrwieniowo‑reperfuzyjne. Omówione tu badanie bada niespodziewanego, naturalnego obrońcę wewnątrz komórek serca — kolistego RNA nazwanego circArhgap26 — który pomaga chronić mięsień sercowy przed tą wtórną falą uszkodzeń. Zrozumienie, jak działa ta niewielka cząsteczka, może wskazać drogę do nowych terapii i badań krwi dla osób z chorobami serca.
Ukryte kółko w zapisie genetycznym serca
Większość z nas myśli o genach jak o prostych niciach DNA i RNA, ale komórki wytwarzają też cząsteczki RNA w kształcie pierścienia, zwane RNA kolistymi, które są wyjątkowo stabilne i mogą subtelnie regulować wiele procesów komórkowych. Naukowcy przeszukali serca myszy pod kątem RNA kolistych, które zmieniają się podczas uszkodzenia serca, i skupili się na jednym — circArhgap26 — którego poziomy gwałtownie spadły po odcięciu i przywróceniu przepływu krwi. Potwierdzili, że to RNA tworzy zamkniętą pętlę, występuje głównie w płynnej części komórki i nie służy jako matryca do syntezy białka. Zamiast tego wydaje się działać jako regulator, wchodząc w interakcje z innymi cząstkami i wpływając na to, czy komórka serca przeżyje czy zginie po stresie. 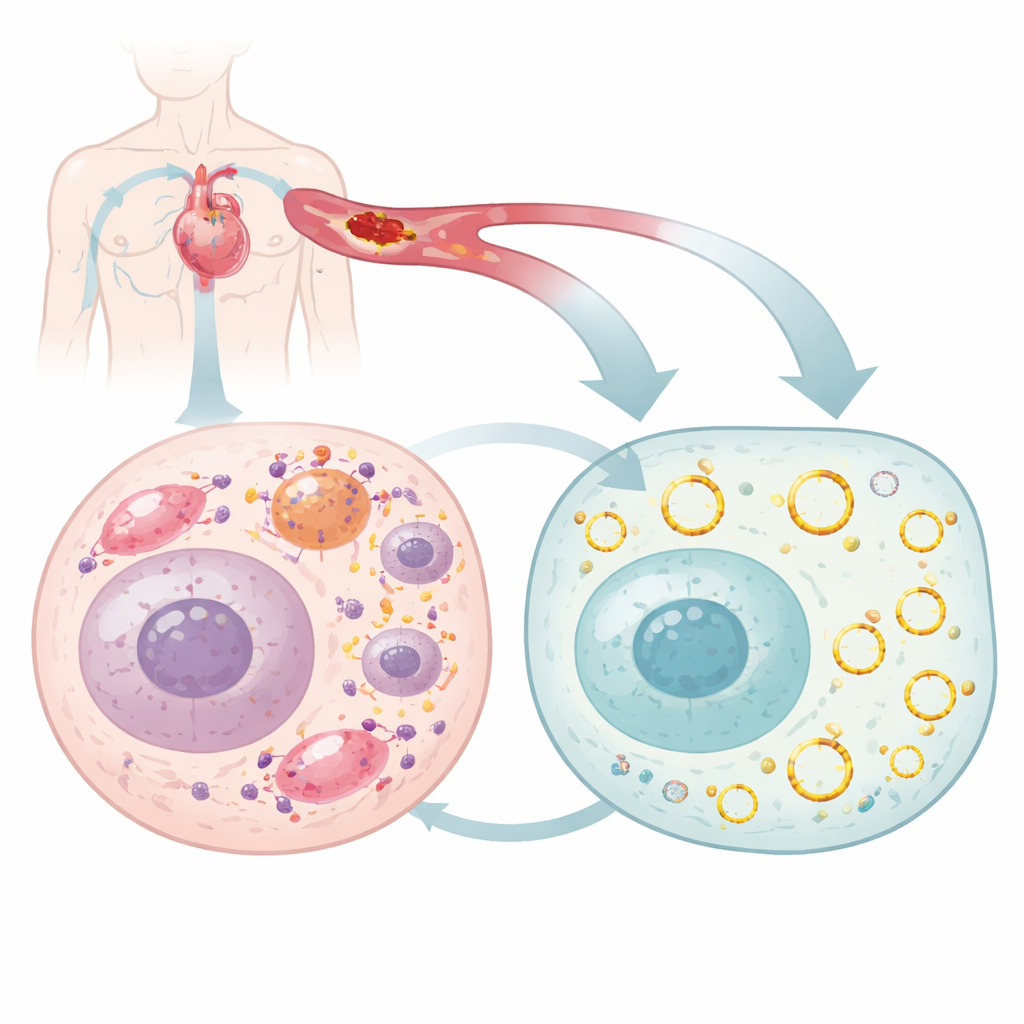
Dowód, że RNA koliste chroni serce
Aby sprawdzić, co circArhgap26 faktycznie robi, zespół zwiększał lub zmniejszał jego poziomy w sercach myszy. Gdy użyto wirusa do podwyższenia circArhgap26 specyficznie w komórkach mięśnia sercowego, zwierzęta poddane tymczasowemu zamknięciu tętnicy wieńcowej, a następnie przywróceniu przepływu krwi, miały silniejszą frakcję wyrzutową, mniejsze obszary uszkodzenia i mniej umierających komórek. Klasyczne markery uszkodzenia we krwi i tkance serca również były niższe. Przeciwnie, gdy RNA koliste zostało wygaszone, nawet bez wywołanego zawału funkcja serca pogarszała się, a śmierć komórek wzrastała — a problemy te nasilały się po dodaniu niedokrwienia‑reperfuzji. Podobne ochronne efekty zaobserwowano w ludzkich komórkach przypominających serce w laboratorium, co sugeruje, że mechanizm jest zachowany między myszami a ludźmi.
Szkodliwy partner białkowy trzymany w ryzach
Idąc dalej, badacze pytali, jak circArhgap26 wywiera tę ochronę. Stosując biochemiczne techniki „łowienia”, odkryli, że wiąże się on bezpośrednio z białkiem strukturalnym o nazwie plakofilina‑1 (PKP1), które może wpływać na siłę przylegania komórek i ich skłonność do programowanej śmierci. W uszkodzonych sercach i zestresowanych komórkach serca poziomy PKP1 wzrastały i korelowały z gorszymi uszkodzeniami. Wyciszenie PKP1 łagodziło uraz serca i śmierć komórek, podczas gdy wymuszenie jego produkcji pogarszało wyniki. Gdy circArhgap26 był podwyższony, ilość białka PKP1 malała, mimo że aktywność jego genu się nie zmieniała — co wskazuje na kontrolę po powstaniu komunikatu RNA. Eksperymenty wykazały, że circArhgap26 przyspiesza rozkład białka PKP1 przez zakłócanie procesu modyfikacji tłuszczowej zwanej palmitylowaniem, który normalnie stabilizuje PKP1.
Molekularna przepychanka o sygnały śmierci komórkowej
Palmitylowanie jest przeprowadzane przez rodzinę enzymów; jeden z nich, ZDHHC1, okazał się przyłączać grupy tłuszczowe do PKP1 i wydłużać jego żywotność. CircArhgap26 wiąże PKP1 w tym samym rejonie, którego używa ZDHHC1, tworząc molekularną przepychankę. Gdy RNA koliste „wygrywa”, PKP1 otrzymuje mniej tłuszczowych znaczników, staje się mniej stabilny i jest szybciej usuwany. Ma to dalsze konsekwencje: PKP1 zwykle zwiększa wytwarzanie innego białka, APAF1, przez interakcję z kontrolnym odcinkiem jego RNA. APAF1 jest kluczowym elementem maszyny aktywującej enzymy kaspazy‑9 i kaspazy‑3, centralnych egzekutorów śmierci komórkowej. Przy mniej stabilnym PKP1 produkcja białka APAF1 spada, kaskada sygnałów prowadzących do śmierci jest stłumiona, a komórki serca są bardziej skłonne przetrwać stres związany z przywróceniem przepływu krwi. 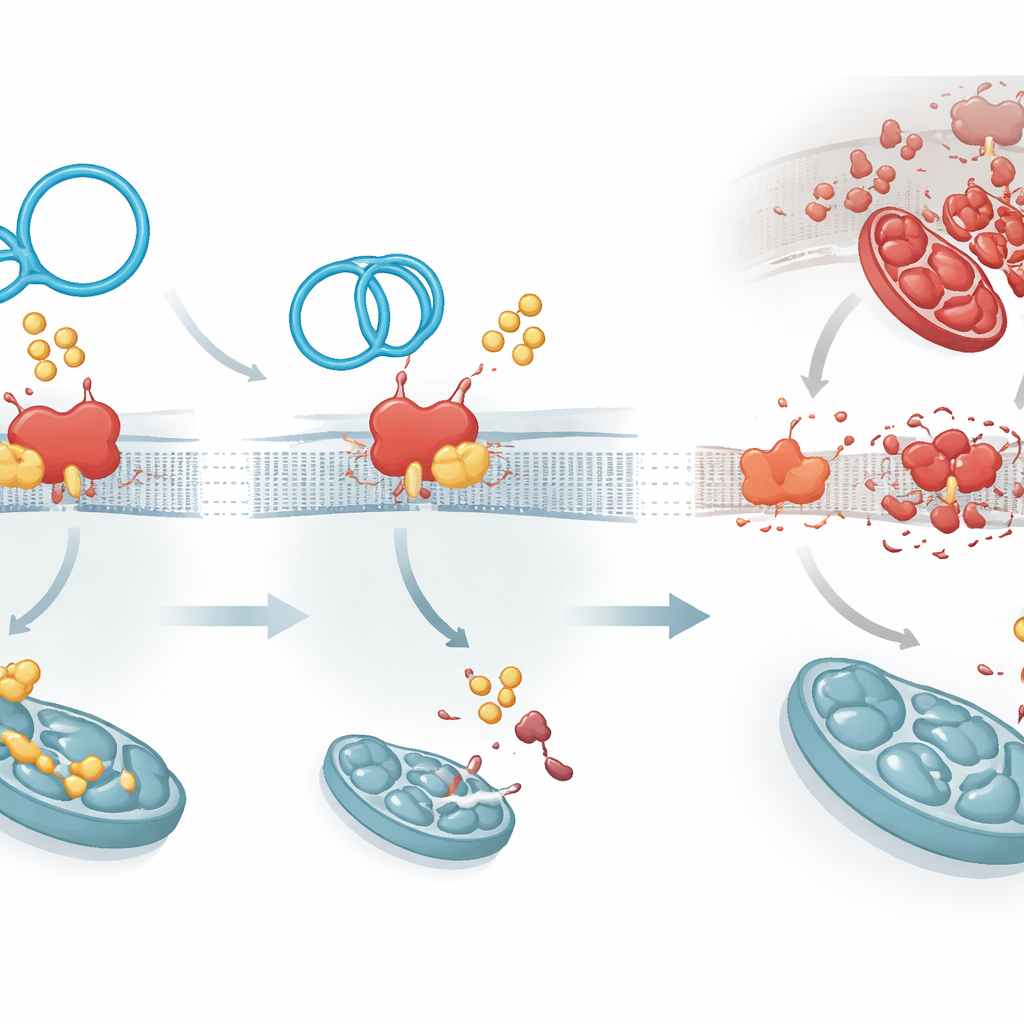
Dostrajanie kółka i jego obietnica dla pacjentów
Badanie ujawnia także, jak sam circArhgap26 jest tłumiony podczas urazu. Powszechny chemiczny znak na RNA, zwany m6A, gromadzi się na tym kółkowym RNA w zestresowanych sercach. Białko‑czytnik o nazwie YTHDF2 rozpoznaje tę modyfikację i promuje degradację circArhgap26, osłabiając naturalną obronę serca właśnie wtedy, gdy jest ona najbardziej potrzebna. Co ważne, ludzka wersja tego RNA kolistego jest bardzo podobna do mysiej wersji i jest wyraźnie niższa we krwi pacjentów poddawanych zabiegom udrożniania tętnic w porównaniu ze zdrowymi ochotnikami. Razem te ustalenia sugerują, że przywrócenie lub naśladowanie circArhgap26 mogłoby służyć zarówno jako marker ryzyka w badaniu krwi, jak i jako nowa terapia. Mówiąc prościej, praca ujawnia małą kolistą cząsteczkę, która działa jak strażnik przeciwko uszkodzeniom po reperfuzji, rozbrajając śmiertelną kaskadę wewnątrz komórek serca.
Cytowanie: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Słowa kluczowe: uszkodzenie niedokrwieniowo‑reperfuzyjne, RNA koliste, atak serca, apoptoza kardiomiocytów, terapia oparta na RNA