Clear Sky Science · pl
Synergia chemo‑fototermiczna wywołuje odporność przeciwnowotworową poprzez ferroptoza
Wykorzystywanie ciepła i światła ciała jako broń przeciw rakowi
Leki chemioterapeutyczne mogą zmniejszać guzy, ale często wiążą się z silnymi skutkami ubocznymi i nie zawsze zapobiegają nawrotom choroby. W tym badaniu analizuje się nowy sposób, by sprawić, że istniejący lek — docetaksel — działa silniej i mądrzej, pakując go w malutkie cząstki reagujące na ciepło i aktywując je światłem bliskiej podczerwieni. Celem jest nie tylko precyzyjniejsze zabijanie komórek nowotworowych, lecz także pobudzenie układu odpornościowego, aby rozpoznawał i wyłapywał raka w całym organizmie oraz zapobiegał przyszłym nawrotom. 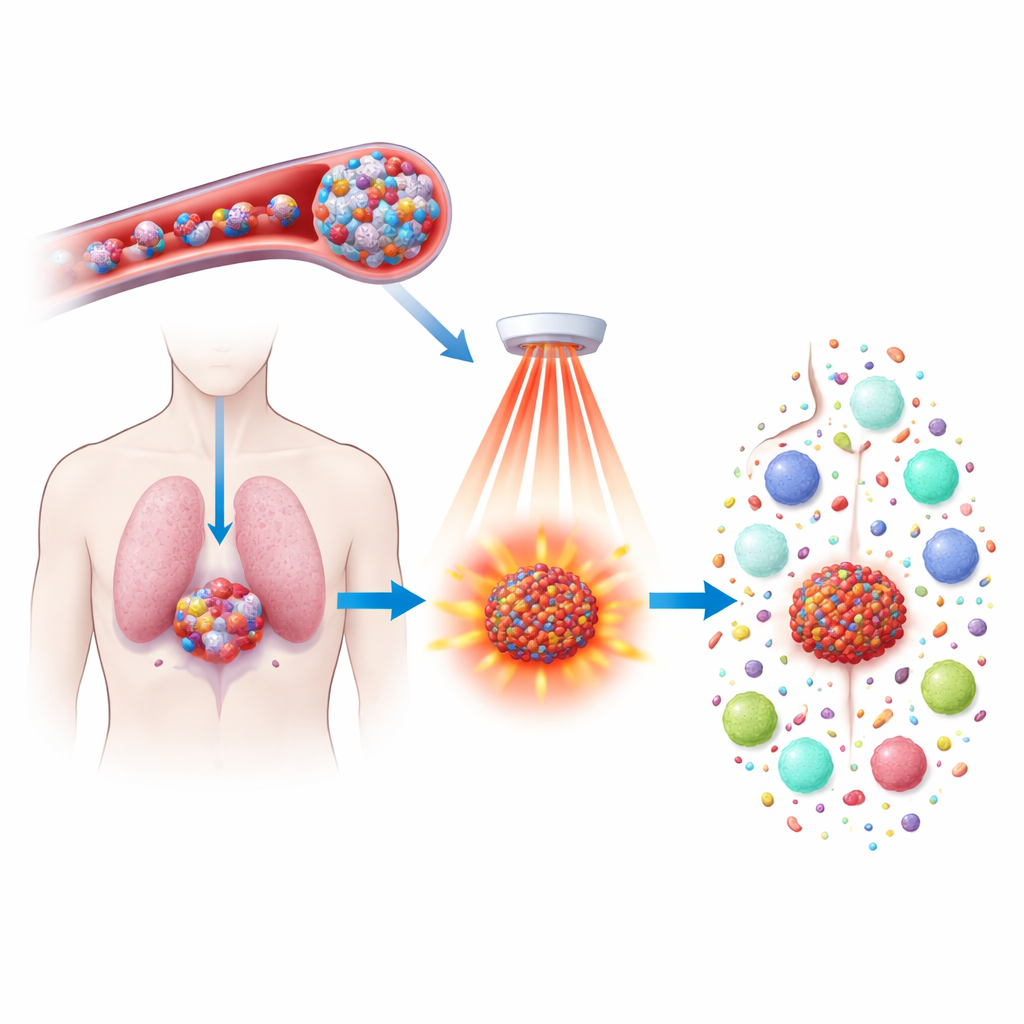
Maleńcy kurierzy, którzy trafiają tam, gdzie trzeba
Naukowcy skonstruowali nowy rodzaj nanocząstek z polimeru zawierającego ferrocen — cząsteczkę z żelazem, która silnie reaguje z nadtlenkiem wodoru, utleniaczem występującym w wyższych stężeniach w guzach niż w tkankach zdrowych. Polimery te samoistnie tworzą hydrofilowe kuleczki, które mogą przenosić zarówno docetaksel, jak i barwnik pochłaniający światło, IR808. Po wstrzyknięciu do krwiobiegu cząstki są na tyle małe i stabilne, że krążą i mogą przeciekać do guzów, gdzie nieszczelne naczynia krwionośne oraz wysokie stężenia nadtlenku wodoru zaczynają osłabiać cząstki i stopniowo uwalniać ich ładunek. Takie rozwiązanie koncentruje terapię w guzie, ograniczając uszkodzenia zdrowych narządów.
Wykorzystanie światła do wzmocnienia lokalnego uszkodzenia
Światło bliskiej podczerwieni, które bezpiecznie penetruje tkanki, jest następnie skierowane na okolice guza. IR808 wewnątrz nanocząstek absorbuje to światło i przekształca je w ciepło, a także generuje reaktywne formy tlenu. Połączenie nadtlenku wodoru produkowanego przez guz i utleniaczy tworzonych przez światło powoduje szybsze rozpady cząstek i uwalnianie leku dokładnie tam, gdzie jest potrzebny. Równocześnie żelazo obecne w segmencie ferrocenu przekształca te utleniacze w szczególnie agresywne formy, które atakują lipidowe składniki błon komórkowych. Ten ukierunkowany atak chemiczny i termiczny znacznie zwiększa moc zabijania w porównaniu z samym docetakselem lub samą terapią światłem. 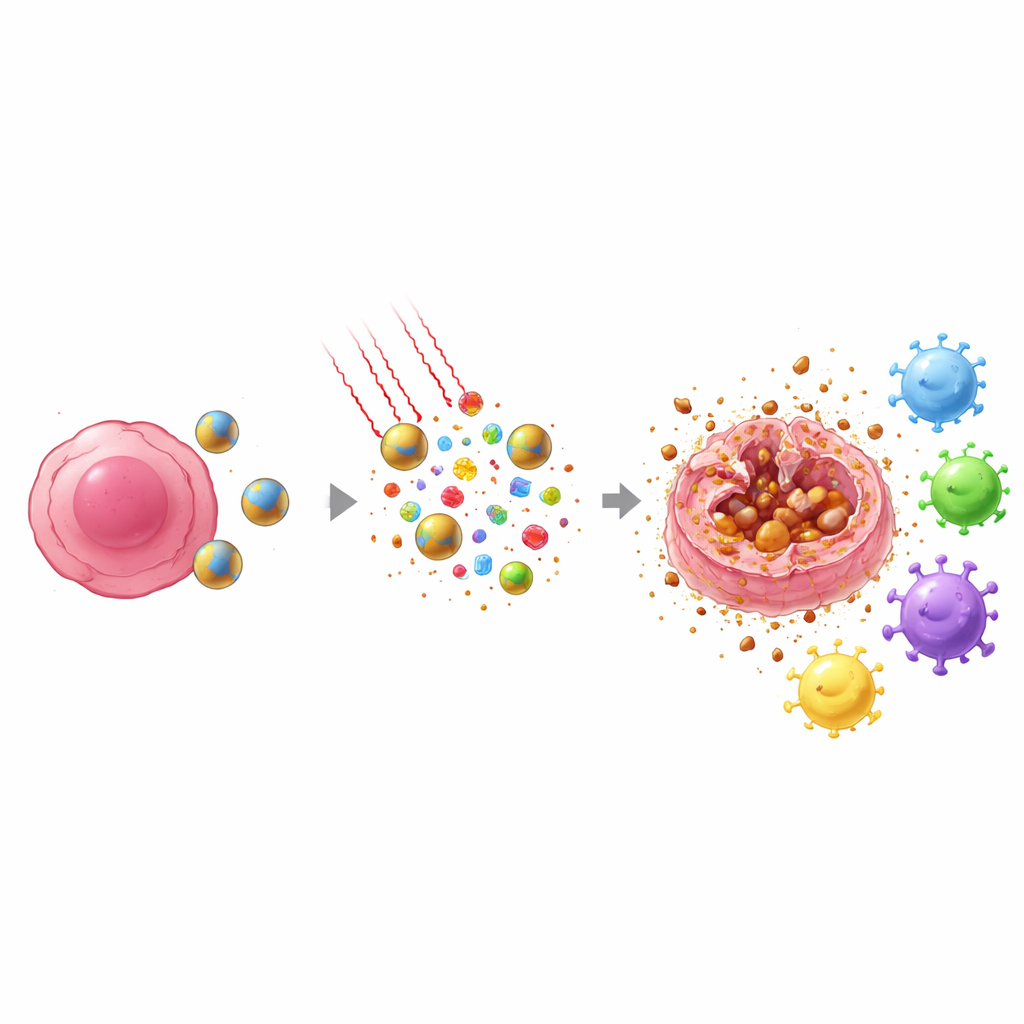
Kontrolowane spalanie, które alarmuje układ odpornościowy
Co ważne, sposób, w jaki komórki nowotworowe umierają pod wpływem tego leczenia, różni się od zwykłej chemioterapii. Zamiast cicho rozpadać się na drobne fragmenty, wiele komórek przechodzi proces zwany ferroptozą — formę śmierci napędzaną przez żelazo, która niszczy lipidy i prowadzi do pęknięcia błony zewnętrznej. Wówczas komórki uwalniają wewnętrzne sygnały alarmowe i fragmenty specyficzne dla guza do otoczenia. Równocześnie docetaksel przesuwa kluczowy białkowy składnik jądra, HMGB1, w kierunku krawędzi komórki, przygotowując go do uwolnienia. Razem ciepło, utleniacze i działanie leku tworzą wybuch sygnałów niebezpieczeństwa i antygenów, które pobliskie strażnicze komórki układu odpornościowego — komórki dendrytyczne — wychwytują i przenoszą do węzłów chłonnych.
Od lokalnego ataku do obrony całego organizmu
W modelach mysich z guzami to skojarzone leczenie chemo‑fototermiczne nie tylko skuteczniej zmniejszało bezpośrednio podgrzewane guzy niż którykolwiek z pojedynczych składników, lecz także zmieniało krajobraz immunologiczny. Guzy wykazywały więcej dojrzałych komórek dendrytycznych i większą liczbę komórek T‑zabójców, zarówno w samym guzie, jak i w drenujących węzłach chłonnych. U niektórych myszy z prawidłowym układem odpornościowym guzy pierwotne zniknęły po zaledwie dwóch cyklach leczenia. Gdy badacze później wszczepili nowe guzy w odległych miejscach lub po przeciwnej stronie, wtórne rozrosty były spowolnione lub zahamowane, co wskazuje, że zwierzęta wytworzyły formę odporności pamięciowej specyficznej dla nowotworu. Dodanie przeciwciała blokującego punkt kontrolny, które zapobiega wyczerpaniu komórek T, dodatkowo zmniejszyło przerzuty do płuc i wydłużyło przeżycie, sugerując, że to lokalne leczenie można łączyć z nowoczesnymi immunoterapiami.
Dlaczego to ma znaczenie dla przyszłej opieki onkologicznej
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że podejście to przekształca docetaksel z ogólnoustrojowej trucizny w element inteligentnej, wieloetapowej strategii przeciwnowotworowej. Poprzez zapakowanie leku w cząstki aktywowane światłem, zawierające żelazo i reagujące na chemię guza, terapia dostarcza więcej uszkodzeń wewnątrz nowotworów przy jednoczesnym oszczędzaniu tkanek zdrowych. Szczególny wzorzec śmierci komórek, jaki wywołuje, działa niczym wewnętrzna szczepionka, ucząc układ odpornościowy rozpoznawania i zapamiętywania raka. Jeśli te wyniki przełożą się na ludzi, takie systemy chemo‑fototermiczne mogłyby pomóc przekształcić oporne „zimne” guzy w „gorące”, lepiej reagujące na terapie oparte na odporności, co potencjalnie zmniejszy liczbę nawrotów i poprawi długoterminową kontrolę choroby.
Cytowanie: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Słowa kluczowe: nanomedycyna nowotworowa, terapia fototermiczna, ferroptoza, immunoterapia nowotworów, dostawa docetakselu