Clear Sky Science · pl
Nanoreaktory enzymatyczne w ograniczonej kaskadzie inspirowane naturą do celowanej terapii miażdżycy
Walka z zatorami w tętnicach przy pomocy sprytnych, maleńkich pomocników
Miażdżyca — zatkane, zapalone tętnice — jest jedną z głównych przyczyn zawałów serca i udarów. Wiele osób przyjmuje leki obniżające poziom cholesterolu, a mimo to niebezpieczne blaszki mogą nadal narastać i pozostawać w stanie zapalnym. W tym badaniu opisano nanoreaktor inspirowany naturą — maleńką, zaprojektowaną cząsteczkę naśladującą własne mechanizmy antyoksydacyjne organizmu, mającą za zadanie uspokoić zapalne blaszki, usunąć szkodliwe cząsteczki i spowolnić starzenie się naczyń w modelach zwierzęcych. 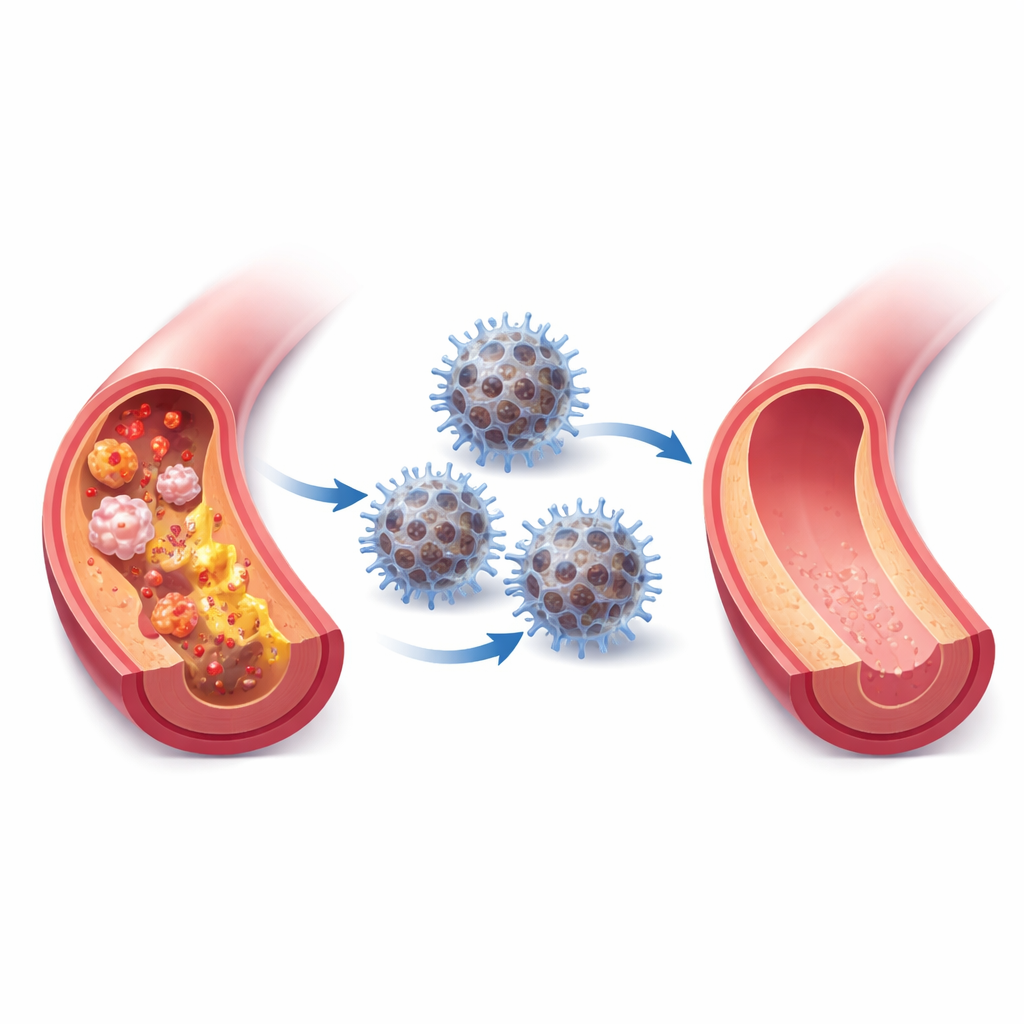
Dlaczego blaszki to coś więcej niż tylko tłuszcz
Kiedyś uważano, że blaszki miażdżycowe to głównie nagromadzenie cholesterolu. Dziś wiemy, że napędza je także stres oksydacyjny i przewlekłe zapalenie. W chorujących tętnicach niestabilne cząsteczki zwane reaktywnymi formami tlenu uszkadzają lipidy, przekształcając zwykły cholesterol w bardziej szkodliwą postać, którą komórki odpornościowe pochłaniają, tworząc „komórki piankowate” i niestabilne blaszki. Starzejące się i zestresowane komórki wyściełające naczynia dokładają paliwa do ognia, wydzielając dodatkowe sygnały zapalne. Naturalne enzymy w zdrowych tkankach zwykle utrzymują te reaktywne cząsteczki w ryzach, ale w blaszkach równowaga jest zaburzona, a podawanie pojedynczych antyoksydantów nie przyniosło dotąd dobrych efektów u pacjentów.
Zapożyczając strategie z naturalnych „fabryk” enzymów
W komórkach enzymy ochronne neutralizujące reaktywne formy tlenu często działają obok siebie w ściśle zgranych zespołach, przekazując szkodliwe pośredniki z jednej jednostki do drugiej w szybkim kaskadowym procesie. Badacze postanowili skopiować tę strategię przy użyciu materiałów syntetycznych. Zbudowali nanoreaktor w „ograniczonej kaskadzie”, pakując ultramałe cząstki błękitu pruskiego — wykazujące aktywność podobną do kilku enzymów antyoksydacyjnych — wewnątrz dendrytycznej, gąbczastej kuli krzemionkowej domieszkowanej selenem, istotnym składnikiem innego naturalnego enzymu antyoksydacyjnego. Ta porowata struktura koncentruje zarówno katalizatory, jak i ich cele, umożliwiając etapowe detoksykowanie reaktywnych form tlenu wydajniej niż gdyby każdy składnik krążył osobno w krwiobiegu. 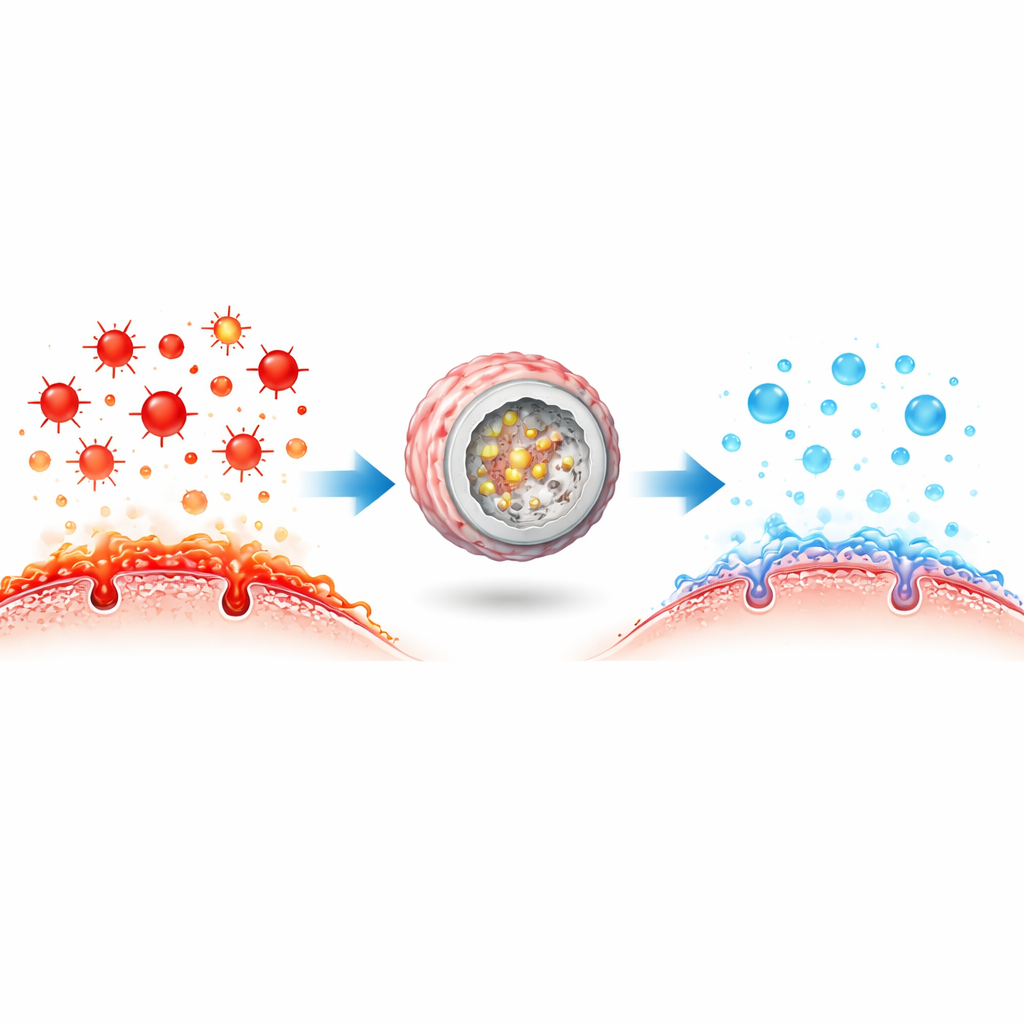
Nadanie nanoreaktorom kamuflażu neutrofilowego
Dostarczenie leku w odpowiednie miejsce to duże wyzwanie. Zespół otoczył swoje nanoreaktory membranami pobranymi z neutrofili — rodzaju białych krwinek naturalnie przyciąganych do miejsc zapalenia. Ten kamuflaż pomaga cząstkom krążyć dłużej, unikać szybkiego usuwania i kierować się ku blaszkom, gdzie chore komórki naczyniowe i komórki odpornościowe wykazują zgodne markery adhezyjne. W eksperymentach komórkowych te powlekane nanoreaktory były chętniej pobierane przez zapalone komórki śródbłonka i makrofagi niż kontrolne, niepowlekane cząstki, co pokazuje, że biologiczna „powłoka” aktywnie naprowadza je na obszary problemowe.
Uspokajanie zapalenia, komórek piankowatych i starzenia komórek
W badaniach in vitro nanoreaktory imitowały działalność kilku enzymów jednocześnie, rozkładając różne typy reaktywnych form tlenu i przekształcając je w nieszkodliwe produkty. Po dodaniu do zapalnych komórek odpornościowych i wyściełających naczynia, znacznie obniżały stres oksydacyjny, zmniejszały wydzielanie kluczowych mediatorów zapalnych i skłaniały makrofagi ze stanu sprzyjającego uszkodzeniom w kierunku stanu wspierającego gojenie. Ograniczały też gromadzenie tłuszczu wewnątrz makrofagów, zmniejszając tworzenie komórek piankowatych, oraz chroniły komórki śródbłonka przed uszkodzeniami DNA i markerami starzenia. Efekty te były silniejsze niż obserwowane przy użyciu jakiegokolwiek pojedynczego składnika, co podkreśla znaczenie ograniczonego, wielostopniowego projektu.
Ochrona tętnic w modelu myszy
Zespół przetestował następnie neutrofilowo powlekane nanoreaktory u myszy genetycznie predysponowanych do miażdżycy i karmionych dietą wysokotłuszczową. Cząstki krążyły we krwi przez wiele godzin, gromadziły się w blaszkach i wykazywały ograniczone odkładanie w zdrowych narządach. Po kilku tygodniach leczenia myszy otrzymujące pełny nanoreaktor miały mniejsze powierzchnie blaszek, mniej komórek zapalnych, więcej stabilizującej kolagenu i niższe poziomy enzymów związanych z pękaniem blaszek w porównaniu z grupami kontrolnymi lub zwierzętami otrzymującymi prostsze formulacje. Barwienia tkanek wykazały zmniejszony stres oksydacyjny i mniej komórek senescentnych w ścianie naczynia, wszystko bez wyraźnych objawów toksyczności czy utraty masy ciała.
Co to może oznaczać dla przyszłych terapii serca
Dla laika praca ta sugeruje nowy sposób radzenia sobie z chorobą naczyń: zamiast jedynie obniżać cholesterol lub blokować pojedynczy trigger zapalny, wykorzystuje maleńkie, inspirowane naturą „maszyny”, które cicho usuwają szkodliwe cząsteczki, łagodzą zapalenie i spowalniają starzenie komórek bezpośrednio wewnątrz blaszek. Choć daleko jeszcze do zastosowań u ludzi, te nanoreaktory w ograniczonej kaskadzie pokazują, że łączenie inteligentnych materiałów z biologicznym kamuflażem może zaoferować potężniejsze, bardziej celowane podejście do stabilizowania zatkanych tętnic i — być może kiedyś — zmniejszania ryzyka zawałów i udarów.
Cytowanie: Wu, Y., Xia, H., Ding, H. et al. Nature-inspired confined cascade enzyme nanoreactors for targeted atherosclerosis therapy. Sig Transduct Target Ther 11, 84 (2026). https://doi.org/10.1038/s41392-026-02598-4
Słowa kluczowe: miażdżyca, nanomedycyna, stres oksydacyjny, zapalenie, nanozym